
能正确表示下列反应的离子方程式是
A.碳酸氢钙溶液和氢氧化钠溶液混合:HCO3—+OH—==CO32—+H2O
B.醋酸钠溶液和盐酸混合:CH3COONa+H+ == CH3COOH + Na+
C.少量金属钠放入冷水中:Na+ 2H2O== Na++2OH—+H2↑
D.硫酸铜溶液和氢氧化钡溶液混合:
Cu2+ + SO42— +Ba2+ + 2OH—== Cu(OH)2↓+ BaSO4↓
 快捷英语周周练系列答案
快捷英语周周练系列答案科目:高中化学 来源: 题型:
甲酸甲酯水解反应方程式为:
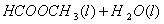 ≒
≒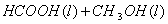
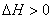
某小组通过实验研究该反应(反应过程中体积变化忽略不计)。反应体系中各组分的起始量如下表:

甲酸甲酯转化率在温度T1下随反应时间(t)的变化如下图:

(1)根据上述条件,计算不同时间范围内甲酸甲酯的平均反应速率,结果见下表:

请计算15-20min范围内甲酸甲酯的减少量为 mol,甲酸甲酯的平均反应速率
为 mol·min-1(不要求写出计算过程)。
(2)依据以上数据,写出该反应的反应速率在不同阶段的变化规律及其原因: 。
(3)上述反应的平衡常数表达式为: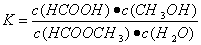 ,则该反应在温度
,则该反应在温度
T1下的K值为 。
(4)其他条件不变,仅改变温度为T2(T2大于T1),在答题卡框图中画出温度T2下甲酸甲酯转化率随反应时间变化的预期结果示意图。
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,用0.1000 mol·L-1 NaOH溶液滴定20.00 mL 0.1000 mol·L-1HClO溶液所得滴定曲线如下图。下列说法正确的是

A.点①所示溶液中:c(ClO-)+c(OH-)=c(HClO)+c(H+)
B.点②所示溶液中:c(Na+)=c(HClO)+c(ClO-)
C.点③所示溶液中:c(Na+)>c(OH-)>c(ClO-)>c(H+)
D.滴定过程中可能出现:c(HClO)>c(ClO-)>c(H+)>c(Na+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)海水中锂元素储量非常丰富,从海水中提取锂的研究极具潜力。锂是制造化学电源的重要原料。如LiFePO4电池某电极的工作原理如下图所示:
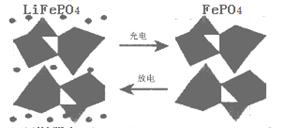
该电池的电解质为能传导Li+的固体材料。放电时该电极是电池的 极(填“正”或“负”),该电极反应式为 。
(2)用此电池电解含有0. 1 mol/L CuSO4和0. 1 mol/L NaCl的混合溶液100 mL,假如电路中转移了0.02 mol e-,且电解池的电极均为惰性电极,阳极产生的气体在标准状况下的体积是________L,将电解后的溶液加水稀释至1 L,此时溶液的pH=____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
分析下列材料,选择将乙二醇和丙三醇的混合物分离的适宜方法是( )
| 物质 | 熔点/℃ | 沸点/℃ | 密度/g•cm-3 | 溶解性 |
| 乙二醇(C2H6O2) | -11.5 | 198 | 1.11 | 与水和酒精等混溶 |
| 丙三醇(C3H8O3) | 17.9 | 290 | 1.26 | 与水和酒精等混溶 |
A.蒸馏法 B.萃取法 C.“溶解、结晶、过滤” 的方法 D.分液法
查看答案和解析>>
科目:高中化学 来源: 题型:
|
|
(1) 若在滴加NaOH溶液的过程中,沉淀质量随加入NaOH溶液的体积V变化如下图所示。当V1=200 mL时,则金属粉末中,n(Mg)=_________mol,V2=__________mL。
(2) 若在滴加NaOH溶液的过程中,欲使Mg2+、A13+刚好沉淀完全,则滴入NaOH溶液的体积为__________mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述不正确的是( )
A. NH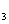 易液化,氨常用作制冷剂 B. 铝盐和铁盐可以用于净水
易液化,氨常用作制冷剂 B. 铝盐和铁盐可以用于净水
C. 与金属反应时,稀HNO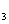 可能被还原为更低价态,则稀HNO
可能被还原为更低价态,则稀HNO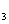 氧化性强于浓HNO
氧化性强于浓HNO
D. 淘金者利用密度的不同,用淘洗的方法将金子从沙里分出来
查看答案和解析>>
科目:高中化学 来源: 题型:
化学与生活密切相关,下列有关说法正确的是
A.维生素C具有还原性,在人体内起抗氧化作用
B.糖类、蛋白质、油脂属于天然高分子化合物
C.煤经气化和液化两个物理变化过程,可变为清洁能源
D.制作航天服的聚酯纤维和用于光缆通信的光导纤维都是新型无机非金属材料
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com