
| 难溶电解质 | Cu(OH)2 | CuS | Pb(OH)2 | PbS |
| Ksp | 4.8×10-20 | 6.3×10-36 | 1.2×10-15 | 1.0×10-28 |
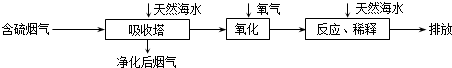

分析 (1)镁为活泼金属,可由无水氯化镁电解制取金属镁;
(2)根据题目中所给难溶电解质的Ksp,可知Cu2+和Pb2+的硫化物Ksp更小,更难溶;
(3)①强碱弱酸盐的水解呈碱性,据此书写反应的方程式;
②根据图示可知:SO2的吸收效率随着温度的升高而降低,随流速的增大而降低,
③H2SO3或HSO3-中的S显+4价,均可被O2氧化生成H++SO42-,酸性会大大增强,氧化后的“海水”需要引入大量的显碱性的海水与之混合后才能排放,主要目的是中和、稀释经氧气氧化后海水中生成的酸(H+).
解答 解:(1)电解无水氯化镁可制取金属镁,该反应的化学反应方程式为:MgCl2$\frac{\underline{\;电解\;}}{\;}$Mg+Cl2↑,
故答案为:MgCl2 $\frac{\underline{\;电解\;}}{\;}$Mg+Cl2↑;
(2)根据题目中所给难溶电解质的Ksp,可知Cu2+和Pb2+的硫化物Ksp更小,更难溶;所以用Na2S除去污水中的Cu2+和Pb2+效果更好,
故答案为:Na2S;
(3)①天然海水的pH≈8,是因为海水中有CO32-或HCO3-+它们水解使海水呈弱碱性,其离子方程式为CO32-+H2O?HCO3-+OH-或 HCO3-+H2O?H2CO3+OH-,
故答案为:CO32-+H2O?HCO3-+OH-或 HCO3-+H2O?H2CO3+OH-;
②根据图示可知:SO2的吸收效率随着温度的升高而降低,随流速的增大而降低,所以要提高含硫烟气中SO2的吸收效率,可以降低含硫烟气温度(或流速),
故答案为:降低含硫烟气温度(或流速);
③H2SO3或HSO3-中的S显+4价,均可被O2氧化生成H++SO42-,酸性会大大增强,氧化后的“海水”需要引入大量的显碱性的海水与之混合后才能排放,主要目的是中和、稀释经氧气氧化后海水中生成的酸(H+),
故答案为:2H2SO3+O2=4H++2SO42-或2HSO3-+O2=2H++2SO42-;中和、稀释经氧气氧化后海水中生成的酸(H+).
点评 本题考查了方程式的书写,氧化还原反应,沉淀溶解平衡,盐类水解等,掌握基础是关键,题目难度中等,综合性较强.


 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案科目:高中化学 来源: 题型:选择题
| A. | 5mol | B. | $\frac{5}{3}$mol | C. | $\frac{5}{6}$mol | D. | $\frac{2}{5}$mol |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题

| A. | 向品红溶液中同时通入Cl2、SO2,漂白效果会更好 | |
| B. | 加热可判断品红褪色是通入SO2还是通入Cl2引起的 | |
| C. | “无色化合物”分子中,19个碳原子都可能处在同一平面上 | |
| D. | 品红分子结构中,所有原子不可能处在同一平面上 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ②⑤ | C. | ③⑥ | D. | ④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 能使甲基橙试液变红的溶液中:Na+、K+、MnO4-、I- | |
| B. | 含Br-、K+、Na+、HSO3-的溶液,通入SO2后这些离子仍能大量共存 | |
| C. | 含K+、Na+、NO3-、CH3COO-的溶液中c(H+)=$\sqrt{{K}_{W}}$ | |
| D. | 在水电离出的c(H+)=10-13mol•L-1 的溶液中:NH4+、AlO2-、SO42-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
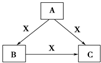 A、B、C、X均为中学化学常见物质,一定条件下有如图所示转化关系(其他产物已略去),下列说法错误的是( )
A、B、C、X均为中学化学常见物质,一定条件下有如图所示转化关系(其他产物已略去),下列说法错误的是( )| A. | 若X为Cl2,则C可为FeCl3 | |
| B. | 若X为KOH溶液,则A可为AlCl3 | |
| C. | 若X为O2,则A可为碳 | |
| D. | 若A、B、C均为焰色反应呈黄色的化合物,则X可为CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,28g乙烯和环丁烷(C4H8)的混合气体中含有的碳原子数为2NA | |
| B. | 室温下,1LpH=13的Ba(OH)2溶液中含有的Ba2+个数为0.1NA | |
| C. | 1molFeI2与足量氯气反应时转移的电子数为2NA | |
| D. | 78g苯含有C=C键的数目为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
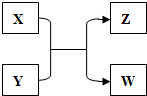 X、Y、Z、W四种物质有如下相互转化关系(其中X、W为单质,Y、Z为化合物,未列出反应条件).
X、Y、Z、W四种物质有如下相互转化关系(其中X、W为单质,Y、Z为化合物,未列出反应条件). .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com