
(18分)实验室测定碳酸钠和碳酸氢钠混合物中碳酸钠的质量分数w(Na2CO3),称取此混合物5.0g,溶于水中,配成250mL溶液。
方案一:沉淀法。利用化学反应把HCO3-、CO32-完全转化为沉淀,称量干燥沉淀的质量,由此计算混合物中w (Na2CO3)。
(1)量取100 mL配制好的溶液于烧杯中,滴加足量沉淀剂,把溶液中HCO3-、CO32-完全转化为沉淀,应选用的试剂是___________ (填编号)。
A.CaCl2溶液 B.MgSO4溶液 C.NaCl溶液 D.Ba(OH)2溶液
(2) 简述证明HCO3-、CO32-已完全沉淀的实验操作_________________________。
(3) 过滤,提取沉淀,则过滤操作所需要的玻璃仪器除烧杯外,还有________________________。
(4) 将沉淀洗涤,并充分干燥,称量沉淀的质量为mg,由此可以计算w(Na2CO3)。如果此步中,沉淀未干燥充分就称量,则测得w (Na2CO3)________________(填偏大或偏小、无影响)。
方案二:量气法。量取10.00mL配制好的溶液与足量稀硫酸溶液反应,测定生成气体在通常状况(约20℃,1.01×105Pa)的体积,由此计算混合物中w (Na2CO3)。
(1) 装置中导管a的作用是 。
(2) 反应结束后,为了准确地测量气体体积,量气管在读数时应注意:
①_______________________________,
②_________________________________,
③眼睛视线与液面最低处相平。
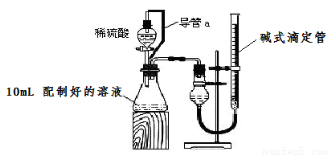
(3)实验前后碱式滴定管中液面读数分别为V1 mL、V2 mL。则 产生CO2的体积为 mL。
方案三:滴定法。量取25.00 mL配制好的溶液加入锥形瓶中,滴加2滴酚酞试剂,摇匀,用0.2000 mol/L盐酸进行滴定到终点(已知终点时反应H++CO32- =HCO3-恰好完全)。重复此操作2次,消耗盐酸的体积平均值为20.00 mL。
(1)量取25.00 mL配制好的溶液,应选择_______________仪器来完成。
(2)判断滴定终点的依据是_____________________。
(3)此法测得w(Na2CO3)= %。
方案一:(1)D(2分)
(2)静置、澄清,在澄清溶液中继续加Ba(OH)2溶液,不浑浊,则HCO3—、CO32-已沉淀完全;反之,未沉淀完全(在取出澄清溶液中继续滴加Ba(OH)2溶液,如果未答出现浑浊时把取出液全部倒回原液中,不给分)(2分)
(3)玻璃棒、普通漏斗(漏斗)(2分) (4)偏小(2分)
方案二:(1)平衡压强、使液体顺利滴下;消除加入稀硫酸引起的氢气体积误差(2分)
(2)①待冷却至室温才开始读数 (1分) ②读数前左右液面相平(1分) (3)V1-V2(2分)
方案三:(1)碱式滴定管(1分) (2)由红色突变为无色,且30s不恢复(1分)(3)84.8%(2分)
【解析】
试题分析:方案一、(1)A、CaCl2溶液只能与碳酸根反应转化为碳酸根沉淀,A不正确;B.MgSO4溶液与二者均不反应,B不正确;C.NaCl溶液与二者均不反应,C不正确;D.Ba(OH)2溶液与二者均反应,生成碳酸钡沉淀,D正确,答案选D。
(2)要证明HCO3-、CO32-已完全沉淀,则可以继续滴加氢氧化钡溶液,即正确的的实验操作是静置、澄清,在澄清溶液中继续加Ba(OH)2溶液,不浑浊,则HCO3—、CO32-已沉淀完全;反之,未沉淀完全。
(3)过滤操作所需要的玻璃仪器除烧杯外,还有玻璃棒、普通漏斗(漏斗)。
(4)如果此步中,沉淀未干燥充分就称量,则称量值偏大。由于在质量相等的条件下碳酸氢钠产生的沉淀大于碳酸钠产生的沉淀,所以如果称量值偏大,则碳酸氢钠的质量偏大,则碳酸钠的含量偏小。
方案二:(1)由于碳酸盐与酸反应产生二氧化碳气体,瓶内压强增大,所以装置中导管a的作用是平衡压强、使液体顺利滴下;消除加入稀硫酸引起的体积误差。
(2)读数是必须与外界大气压相同,因此注意事项是①待冷却至室温才开始读数,②读数前左右液面相平。
(3)碱液吸收CO2,所以前后的体积差即是二氧化碳的体积,则产生CO2的体积为(V1-V2)mL。
方案三:(1)溶液显碱性,因此应该用碱式滴定管量取。
(2)酚酞的变色范围是8.2~10.0,所以判断滴定终点的依据是由红色突变为无色,且30s不恢复。)(3)反应达到终点时,发生的离子方程式为H++CO32- =HCO3-,则根据消耗盐酸的体积可知20.00ml可知,消耗碳酸钠的物质的量是0.2000 mol/L×0.02000L=0.004mol,则原混合物中碳酸钠的物质的量是0.004mol×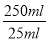 =0.04mol,质量是0.04mol×106g/mol=4.24g,所以碳酸钠质量分数为
=0.04mol,质量是0.04mol×106g/mol=4.24g,所以碳酸钠质量分数为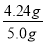 ×100%=84.8%。
×100%=84.8%。
考点:考查碳酸钠和碳酸氢钠混合物中碳酸钠含量测定的实验方案设计与评价


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2013-2014天津市第二学期期中检测高一化学试卷(解析版) 题型:选择题
可用于电动汽车的铝—空气燃料电池,通常以NaCl溶液或NaOH溶液为电解液,铝合金为负极,空气电极为正极。下列说法正确的是
A.以NaCl溶液或NaOH溶液为电解液时,正极反应式都为:O2+2H2O+4e-===4OH-
B.以NaOH溶液为电解液时,负极反应式为Al+3OH--3e-===Al(OH)3
C.以NaOH溶液为电解液时,电池在工作过程中电解液的pH保持不变
D.电池工作时,电子通过外电路从正极流向负极
查看答案和解析>>
科目:高中化学 来源:2013-2014天津市下学期期中考试高二化学试卷(解析版) 题型:选择题
下列实验中,不能达到预期目的是
①苯、浓溴水、溴化铁混合制溴苯
②乙醇和30%的硫酸共热到170℃制乙烯
③用溴水除去混在苯中的己烯,分液得到纯净的苯
④敞口久置的电石与饱和食盐水混合制乙炔
⑤将电石与水反应产生的乙炔通入溴水中,溴水褪色,证明乙炔和溴水发生了加成反应
⑥将溴乙烷和NaOH乙醇溶液混合共热,生成的气体直接通入酸性高锰酸钾溶液,酸性高锰酸钾溶液褪色,说明有乙烯生成
A. ②④⑥ B.①③⑤ C.①②④⑥ D.①②③④⑤⑥
查看答案和解析>>
科目:高中化学 来源:2013-2014天津市南开区高三第一次模拟考试理综化学试卷(解析版) 题型:选择题
根据下列物质的化学性质,判断其应用错误的是
A.酒精能使蛋白质变性,可用于杀菌消毒
B.SO2具有氧化性,可用于漂白纸浆
C.FeCl3溶液能与Cu反应,可用于蚀刻印刷电路
D.镁、锌比铁活泼,可作为牺牲阳极保护钢铁设备
查看答案和解析>>
科目:高中化学 来源:2013-2014天津市南开区高三二模试卷理综化学试卷(解析版) 题型:选择题
下列离子方程式正确的是
A.用铜作电极电解CuSO4溶液:2Cu2++2H2O电解2Cu+4H++O2↑
B.硅酸钠溶液与醋酸溶液混合:SiO32-+H+=H2SiO3↓
C.H2O2溶液中加入稀硫酸和KI溶液:H2O2+2H++2I-=I2+2H2O
D. Na2S2O3溶液中加入稀硫酸:2S2O32-+4H+=SO42-+3S↓+2H2O
查看答案和解析>>
科目:高中化学 来源:2013-2014天津市高三毕业班联考二理综化学试卷(解析版) 题型:选择题
如图是一种应用广泛的锂电池,LiPF6是电解质,SO(CH3)2是溶剂,反应原理是4Li+FeS2=Fe+2Li2S。下列说法正确的是
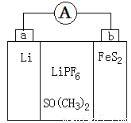
A.该装置将电能转化为化学能
B.Li+向a极移动
C.可以用水代替SO(CH3)2做溶剂
D.b极反应式是FeS2+4Li++4e-=Fe+2Li2S
查看答案和解析>>
科目:高中化学 来源:2013-2014天津市东丽区第一学期期末质量监测高一年级化学试卷(解析版) 题型:简答题
(8分)用NaCl固体配制1mol/L的NaCl溶液100mL。
(1)实验室有下列仪器:①玻璃棒;②胶头滴管;③100mL量筒;④100mL容量瓶;⑤250mL量筒;⑥托盘天平;⑦50mL烧杯;应选用的仪器(填编号) 。
(2)应称取NaCl的质量为 。
(3)在定容时,不小心滴加的蒸馏水超过了刻度线,处理的方法是 ;将NaCl溶液转移到容量瓶后,未对烧杯和玻璃棒进行洗涤,则所得溶液的浓度(填“偏高”或“偏低”或“不变”) 。
查看答案和解析>>
科目:高中化学 来源:2013-2014天津市东丽区第一学期期末质量监测高一年级化学试卷(解析版) 题型:选择题
下列有关概念间关系的说法正确的是
A.碱性氧化物一定是金属氧化物
B.氧化剂在化学反应中一定被氧化
C.酸性氧化物一定是非金属氧化物
D.摩尔质量相同的物质其摩尔体积一定相同
查看答案和解析>>
科目:高中化学 来源:2013-2014天津五区县高一下学期期末考试化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数,下列叙述正确的是
A.24 g镁的原子最外层电子数为NA
B.1 L 0.1mol·L-1乙酸溶液中H+ 数为0.1 NA
C.1 mol甲烷分子所含质子数为10 NA
D.标准状况下,22.4 L乙醇的分子数为NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com