
| A. | CO2 | B. | SO3 | C. | C12 | D. | HCl |
分析 亚硫酸盐和氯化钡反应生成亚硫酸钡沉淀;二氧化硫与氯气在溶液中发生氧化还原反应生成硫酸根离子,与钡离子反应生成硫酸钡沉淀,以此来解答.
解答 解:A.SO2和CO2气体分别通入BaCl2溶液,不发生化学反应,则观察不到沉淀生成,故A不选;
B.将SO3通入BaCl2溶液,生成硫酸钡沉淀,所以分别通入BaCl2溶液时有沉淀生成,不符合题意,故B不选;
C.SO2和C12气体分别通入BaCl2溶液,发生氧化还原反应生成硫酸根离子,与钡离子反应生成硫酸钡沉淀,故C选;
D.SO2和HCl气体分别通入BaCl2溶液,不发生化学反应,则观察不到沉淀生成,故D不选;
故选C.
点评 本题考查二氧化硫的性质,明确二氧化硫的还原性、酸性氧化物是解答本题的关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 由铁矿石炼成铁是化学变化,由生铁炼成钢是物理变化 | |
| B. | 用铁制容器盛放硫酸铜溶液,容器易被腐蚀 | |
| C. | 生铁和钢都是铁、碳合金,它们在性能和用途上差别不大 | |
| D. | 它们都能完全溶解在盐酸中 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 晶体熔点由低到高:CF4<CCl4<CBr4<CI4 | |
| B. | 硬度由大到小:金刚石>碳化硅>晶体硅 | |
| C. | 热稳定性:HF>HI>HBr>HCl | |
| D. | 熔点由高到低:NaF>NaCl>NaBr>NaI |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验操作 | 实验现象 | 实验结论 | |
| A | 将一根未打磨的铝条放入硫酸铜溶液中 | 无紫红色固体析出 | 铝不如铜活泼 |
| B | 将带火星的木条放入氧气瓶中 | 木条复燃 | 氧气能支持燃烧 |
| C | 将CO通过灼热的氧化铜 | 黑色固体变成红色 | CO具有可燃性 |
| D | 将氢氧化钠固体加入水中 | 溶液温度升高 | 该反应是放热反应 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
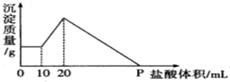 将由NaOH、AlCl3、MgCl2三种固体组成的混合物溶于足量水,充分反应后得到0.58g白色沉淀,向所得的浊液中逐滴加入0.5mol/L的盐酸,生成沉淀的质量与加入盐酸的体积的关系如图所示:
将由NaOH、AlCl3、MgCl2三种固体组成的混合物溶于足量水,充分反应后得到0.58g白色沉淀,向所得的浊液中逐滴加入0.5mol/L的盐酸,生成沉淀的质量与加入盐酸的体积的关系如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
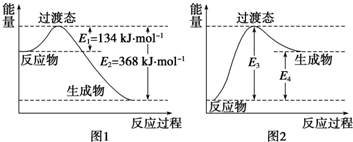
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金刚石比石墨稳定 | |
| B. | 1mol 石墨比1mol金刚石的总能量高 | |
| C. | 金刚石和石墨互为同位素 | |
| D. | 石墨比金刚石稳定 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com