
| A. | 取用试剂瓶中的Na2CO3溶液,发现取量过多,为了不浪费,又把过量的试剂倒入试剂瓶中 | |
| B. | 把NaOH固体放在托盘天平左盘的滤纸上称量 | |
| C. | 用蒸发的方法使NaCl从溶液中析出时,应将蒸发皿中NaCl溶液全部加热蒸干 | |
| D. | 用浓硫酸配制一定物质的量浓度的稀硫酸时,浓硫酸溶于水后,应冷却至室温才能转移到容量瓶中 |
分析 A.应放入指定的仪器中;
B.氢氧化钠易潮解;
C.蒸发时,为避免温度过高,不能完全蒸干;
D.容量瓶只能在常温下使用,不能用来盛装过冷或过热的液体.
解答 解:A.取药品时,多余的药品应放入指定的仪器中,一般不能直接倒回原试剂瓶,防止因变质而污染,故A错误;
B.氢氧化钠易潮解,应放在小烧杯中称,故B错误;
C.蒸发时,为避免温度过高而导致溶质分解而变质,不能完全蒸干,应有大量固体析出时停止加热,用余热蒸干,故C错误;
D.容量瓶只能在常温下使用,不能用来盛装过冷或过热的液体,浓硫酸溶于水放热,溶液的温度较高,应冷却后在转移到容量瓶中,故D正确.
故选D.
点评 本题考查化学实验方案的评价,涉及混合物分离提纯,为高频考点,把握物质的性质、性质差异及混合物分离方法为解答的关键,侧重混合物分离方法选择的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. |  制备Fe(OH)2 | B. |  实验室制备乙炔 | ||
| C. |  从碘与NaCl混合液中分离出碘 | D. |  比较白磷、红磷的着火点 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 23g Na 与足量H2O反应完全后可生成NA个H2分子 | |
| B. | 1 molCu和足量热浓硫酸反应可生成NA个SO3分子 | |
| C. | 18gD2O和18gH2O中含有的质子数均为10NA | |
| D. | 3mol单质Fe完全转变为Fe3O4,失去8NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可用澄清石灰水来区分二氧化碳和二氧化硫 | |
| B. | 可用无水硫酸铜检验酒精中是否含少量水 | |
| C. | 能使灼热的CuO由黑变红的气体一定是H2 | |
| D. | 可用石蕊试液来鉴别盐酸和醋酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2是酸性氧化物,但不与水反应 | |
| B. | 泡花碱属于盐类 | |
| C. | 明矾和漂白粉均可用于自来水的杀菌、消毒 | |
| D. | 玻璃和陶瓷都属于传统硅酸盐材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
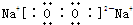
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na与氧气 | B. | 澄清石灰水与二氧化碳 | ||
| C. | 碳与氧气 | D. | 过氧化钠和水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com