
����Ŀ���ش��������⣺
��1��﮺�þ��Ԫ�����ڱ������������Խ�������ϵ�����ǵ��������ơ������й�﮼��仯�������������ȷ����___��
A.Li2SO4������ˮ
B.Li��N2��Ӧ������Li3N
C.LiOH������ˮ
D.LiOH��Li2CO3���ȶ��ֽ�
��2������λ�ڶԽ���λ�õĵڶ�����Ԫ����Be��������Be(OH)2��Mg(OH)2��һ���Լ���___����Ӧ�����ӷ���ʽΪ___��
��3���Ž��з����о�Ԫ�����ڱ�ʱ����ѧ��Ԥ����11����δ���ֵ�Ԫ�أ�Ϊ���������ڱ������¿�λ�����磬��Ԥ���������·���һ���������Ƶ�Ԫ������������������������ѧ����1875�귢�֣�����Ϊ�ء��������ڱ��е�λ����___��
��4����������ͬ����ĵ�������Ԫ�����ʵ��Ʋ��в���ȷ����___��
A.����������ɫ�����Ľ���
B.������������������������
C.�ڻ��������ԣ�3��
D.����������ķ�Ӧ��������
��5��д������������Ԫ����ԭ�Ӱ뾶����ԭ�ӵĵ����ڿ����м��������·�Ӧ����ĵ���ʽ___��
���𰸡�A NaOH��Һ��KOH��Һ ![]() ����������A�� B
����������A�� B ![]()
��������
��1��A��MgSO4Ϊ��������ݶԽ��߹����֪��Li2SO4������ˮ����A�������⣻
B��Mg����N2�ڵ�ȼ����������Mg3N2�����ݸ��ݶԽ��߹����֪��Li��N2��Ӧ������Li3N����B���������⣻
C��Mg(OH)2Ϊ��������ݸ��ݶԽ��߹����֪��LiOH������ˮ����C���������⣻
D��Mg(OH)2��MgCO3�ڼ��������¾���ֽ�����MgO�����ݸ��ݶԽ��߹����֪��LiOH��Li2CO3���ȶ��ֽ⣬��D���������⣻
�ʴ�Ϊ��A��
��2����Al(OH)3�������Կ�֪��Be(OH)2�������ԣ��ܹ���ǿ�����ʷ�Ӧ����Mg(OH)2����ǿ�Ӧ����˿ɲ���NaOH��Һ��KOH��Һ��ǿ�������Al(OH)3��ǿ�����ʷ�Ӧ�ķ���ʽ��ȿ�֪��Be(OH)2��ǿ�����ʷ�Ӧ�����ӷ���ʽΪ��![]() ��
��
��3����λ��Ԫ�����ڱ��е���������A�壬��λ�������·�Ԫ��λ�ڵ���������A�壻
��4��A������ͬ����ĵ�������Ԫ��Ϊ�裬����Ϊ����ɫ����������A���������⣻
B����������Ϊ���Ե�����λ�ڽ����ͷǽ������ٽ紦��������������ȣ��ز����������ʣ�����������Ҳ�����������������B�������⣻
C��������ͬ���壬������ͬ���������������������ڻ�������Ҳ��+3�ۣ���C���������⣻
D��ͬ����Ԫ�����ϵ��½����Ե����������ᷴӦ�ľ��ҳ̶ȵ�������D���������⣻
�ʴ�Ϊ��B��
��5������������Ԫ����ԭ�Ӱ뾶����ԭ����Na�����ڿ����м���������ΪNa2O2�������ʽΪ��![]() ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ҹ������ƾõ���ʷ,����������ʪ����ͭ(Fe��CuSO4��Cu��FeSO4)���Իش��������}��
(1)Cu2+��δ�ɶԵ�������_____����H��O��S�縺���ɴ�С��˳��Ϊ______________________��
(2)��֪[Cu(NH3)4]SO4��һ������
��[Cu(NH3)4]SO4�л�ѧ��������______________��[Cu(NH3)4]2���Ľṹ��ʽΪ_________________������������ԭ���ӻ�����Ϊ____________________��
��NH3��H2O��HF�ķе��ɸߵ���Ϊ_________________��
(3)��ͭ�Ͻ�������Ϊ________________�����ĵ���(I3)�͵���(I4)�����ֱܷ�Ϊ2957 kJ/mol��5290 kJ/mol���Ƚ����ݲ�����ԭ��________________��
(4)��ͭ�Ͻ��һ�־���ṹΪ�������ͣ���ͼ��ʾ��

�ٸúϽ�Ļ�ѧʽΪ_______________��
����֪�úϽ���ܶ�Ϊd g/cm3�������ӏ�����ֵΪNA����þ������ⳤΪ__________nm��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Fe2����Br����I����0.1 mol ����Һ��ͨ��Cl2��ͨ��Cl2�����(��״��)����Һ��ij������(��Q��ʾ)�����ʵ����Ĺ�ϵ��ͼ��ʾ������˵������ȷ����
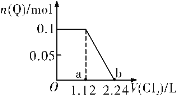
A.Q��I��
B.a��ʱ��Һ�е���������Fe2����Fe3��(������H+)
C.b��ʱ��Һ�е�������ֻ��Cl��(������OH��)
D.ab���䷢���ķ�Ӧ��2Fe2����Cl2=2Fe3����2Cl��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�ܱ������г���1mol![]() ��3mol
��3mol![]() ����һ�������·�����Ӧ
����һ�������·�����Ӧ![]() �������й�˵������ȷ����
�������й�˵������ȷ����
A.�ﵽ��ѧƽ��ʱ��![]() ��
��![]() ��
��![]() �����ʵ���֮��Ϊ1��3��2
�����ʵ���֮��Ϊ1��3��2
B.�ﵽ��ѧƽ��ʱ��![]() ��
��![]() ��
��![]() �����ʵ���Ũ�Ȳ��ٱ仯
�����ʵ���Ũ�Ȳ��ٱ仯
C.�ﵽ��ѧƽ��ʱ��![]() ������ȫת��Ϊ
������ȫת��Ϊ![]()
D.�ﵽ��ѧƽ��ʱ���������������ѹǿ���ٷ����仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�Ǽ��ֳ����л����ת����ϵ������˵����ȷ����
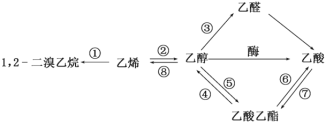
A. ��Ӧ���Ǽӳɷ�Ӧ����Ӧ������ȥ��Ӧ�������������ķ�Ӧ����ȡ����Ӧ
B. ��������������NaOH��Һ��Ӧ��ֻ������
C. 1��2-�������顢��ϩ���Ҵ������ϵ���ԭ�ӱ���ԭ��ȡ������һ��ȡ�����ﶼ��һ��
D. �����ʵ�������ϩ���Ҵ�������������Ӧʱ��������ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼʾ���Ӧ������������ǣ�
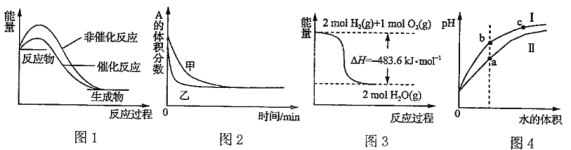
A. ͼ1��ʾij���ȷ�Ӧ�ֱ����С�����������·�Ӧ�����е������仯
B. ͼ2��ʾѹǿ�Կ��淴Ӧ2A(g)+2B(g) ![]() 3C(g)+D(s)��Ӱ�죬�ҵ�ѹǿ��
3C(g)+D(s)��Ӱ�죬�ҵ�ѹǿ��
C. ͼ3��ʾH2��O2������Ӧ�����е������仯����������ȼ����Ϊ241.8kJ��mo1��1
D. ͼ4��ʾ��ˮϡ�͵������pH��ͬ������ʹ��ᣬ��Һ�����ԣ�a>b>c
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1������HI(g)�����ܱ������У�ij�¶��·������б仯��2HI(g) ![]() H2(g)+I2(g) ��H<0
H2(g)+I2(g) ��H<0
���÷�Ӧƽ�ⳣ���ı���ʽΪK=__________��
������Ӧ�ﵽƽ��ʱc(I2)=0.5mol/L��c(HI)=4mol/L����c(H2)Ϊ________��HI�ķֽ���Ϊ_________��
��2����һ�������£�A������B���巴Ӧ����C����,��Ӧ�����У���Ӧ�����������Ũ����ʱ��仯��������ͼ����
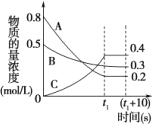
���÷�Ӧ�Ļ�ѧ����ʽΪ��______________
��t1 sʱ��Ӧ��A��ת����Ϊ��__________
��0��t1 s��A�ķ�Ӧ����Ϊv��A��=______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��![]() �£�ij��Ӧ�ﵽƽ�⣬ƽ�ⳣ��
�£�ij��Ӧ�ﵽƽ�⣬ƽ�ⳣ��![]() ����ʱ�������¶ȣ�NOŨ�ȼ�С������˵����ȷ����
����ʱ�������¶ȣ�NOŨ�ȼ�С������˵����ȷ����
A.�÷�Ӧ���ʱ�Ϊ��ֵ
B.�����¼�Сѹǿ����Ӧ��ϵ����ɫ����
C.�����¶ȣ��淴Ӧ���ʼ�С
D.�÷�Ӧ��ѧ����ʽΪ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
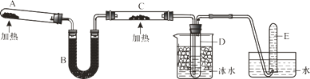
����Ŀ����֪�����������ȵ�����ͭ��Ӧ�õ������ͽ���ͭ����Ӧ����ʽΪ2NH3��3CuO![]() N2��3H2O��3Cu������ͼ��ʾװ�ÿ���ʵ�ָ÷�Ӧ��A�мӵ����Ȼ�狀��������ƹ��壬C �еĹ���������ͭ��
N2��3H2O��3Cu������ͼ��ʾװ�ÿ���ʵ�ָ÷�Ӧ��A�мӵ����Ȼ�狀��������ƹ��壬C �еĹ���������ͭ��
�ش��������⣺
��1��A�з�����Ӧ�Ļ�ѧ����ʽ��_____��
��2��B����������_____��
��3��ʵ��ʱ��C�й۲쵽��������_____���÷�Ӧ�а���������_____������������ԭ������
��4������ʵ����Թ�D�����ʵķ�����������_____��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com