
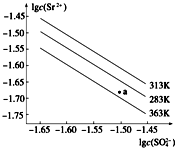
| A、283 K时,图中a点对应的溶液是不饱和溶液 |
| B、三个不同温度下,363 K时Ksp(SrSO4)最大 |
| C、温度一定时,Ksp(SrSO4)随c(SO42-)的增大而减小 |
| D、283 K下的SrSO4饱和溶液升温到363 K后变为不饱和溶液 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、35Cl原子所含质子数为18 |
| B、0.1 mol HCl所分子数约为6.02×1022 |
| C、3.5 g的35Cl2气体的体积为2.24 L |
| D、2 mol35Cl2气体的质量为140 g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | 浓硝酸有挥发性 | 浓硝酸应保存着棕色瓶中 |
| B | 氧化铝的熔点很高 | 氧化铝用来制造耐火坩埚 |
| C | 氯气有强氧化性 | 氯气可用作漂白剂 |
| D | NH4Cl溶液和氨水均能导电 | NH4Cl和氨水均是电解质 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钠和钾的合金具有导电性,可用于快中子反应堆热交换剂 |
| B、明矾溶于水能产生Al(OH)3胶体,可用作净水剂 |
| C、甲醛能使蛋白质变性,可用于食品防腐剂 |
| D、水玻璃易溶于水,可用于生产黏合剂和防火剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com