
下列化学方程式中,属于水解反应的是
A.HCOOH+H2O HCOO-+H3O+ B.HS-+H2O
HCOO-+H3O+ B.HS-+H2O S2-+H3O+
S2-+H3O+
C.CO2+H2O HCO3-+H+ D.CO32-+H2O
HCO3-+H+ D.CO32-+H2O HCO3-+OH-
HCO3-+OH-
 导学全程练创优训练系列答案
导学全程练创优训练系列答案科目:高中化学 来源: 题型:
下列能说明氯元素原子得电子能力比硫强的是( )
①HCl的溶解度比H2S大 ②HCl的酸性比H2S强③HCl的稳定性比H2S强 ④HCl的还原性比H2S强⑤HClO的酸性比H2SO4强 ⑥Cl2能与H2S反应生成S ⑦Cl2与铁反应生成FeCl3,而S与铁反应生成FeS ⑧还原性:Cl- <S2-
A.③④⑤⑧ B.③⑥⑦ C.③⑥⑦⑧ D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
[化学——选修3物质结构与性质](15分)
M是原子序数<30的一种金属,常用于航空、宇航、电器及仪表等工业部门,M原子的最外层有空轨道,且有两个能级处于电子半充满状态。
(1)M原子的外围电子排布式为_____________________,在周期表中属于 区元素。
(2)M的堆积方式属于钾型,其晶胞示意图为______(填序号)。

(3)MCl3·6H2O有三种不同颜色的异构体
A、[M(H2O)6]Cl3,B、[M(H2O)5Cl]Cl2·H2O和C、[M(H2O)4Cl2]Cl·2H2O。为测定蒸发MCl3溶液析出的暗绿色晶体是哪种异构体,取0.010 mol MCl3·6H2O配成溶液,滴加足量AgNO3溶液,得到沉淀2.870 g。该异构体为_______________ (填A或B或C)。
(4) MO2Cl2常温下为暗红色液体,熔点-96.5℃,沸点117℃,能与丙酮(CH3COCH3)、CCl4、CS2等互溶。
①固态MO2Cl2属于________晶体;
②CS2中碳原子和丙酮(CH3COCH3)羰基中的碳原子分别采取的杂化方式为______杂化和________杂化。
(5)+3价M的配合物K[M(C2O4)2(H2O)2]中,配体是______,与C2O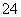 互为等电子体的分子是(填化学式)__________。
互为等电子体的分子是(填化学式)__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知滤渣2的主要成分是Fe(OH)3和Al(OH)3,由滤渣2制取Al2(SO4)3·18H2O,该探究小组设计了如下实验方案:

下列关于此方案的说法,错误的是
A.加入NaOH溶液后过滤,滤渣为Fe(OH)3
B.也可以先加硫酸,再加NaOH溶液后蒸发、冷却、结晶、过滤
C.加硫酸后,溶液中的盐除含有硫酸铝外,还有硫酸钠
D.如果滤渣2中含1molAl(OH)3,则至少需要1molNaOH才能使Al(OH)3完全溶解
查看答案和解析>>
科目:高中化学 来源: 题型:
硫酸、盐酸和硝酸并称为工业上的“三大酸”,实验室中也常用三大酸制取某些气体,制取、收集及尾气处理装置如图所示(省略加热装置、夹持和净化装置)。仅用此装置和表中提供的部分物质完成相关实验。
| 序号 | a中的物质 | b中的物质 | c中收集的气体 |
|
| 甲 | 浓硫酸 | Na2SO3 | ① | ② |
| 乙 | 浓硝酸 | Cu | ③ | NaOH |
| 丙 | 浓盐酸 | MnO2 | Cl2 | NaOH溶液 |
按要求回答下列问题:
(1)表格中①②③三种物质分别是__________、__________、________(填化学式)。
(2)实验乙中生成气体③的离子反应方程式为________________________;某同学认为将浓硝酸改为稀硝酸,即可以利用本套装置制取NO气体,该同学的设计________(填“正确”或“不正确”)。
(3)已知实验丙中生成氯气的化学方程式为4HCl(浓)+MnO2  MnCl2+ Cl2↑+2H2O,在该反应中每生成22.4L(标准状况下)氯气,被氧化HCl的物质的量为__________,转移电子的物质的量为________;d装置中发生反应的离子方程式为_________________。实验室还可以用高锰酸钾和浓盐酸反应制取氯气,完成并配平该反应的离子方程式:
MnCl2+ Cl2↑+2H2O,在该反应中每生成22.4L(标准状况下)氯气,被氧化HCl的物质的量为__________,转移电子的物质的量为________;d装置中发生反应的离子方程式为_________________。实验室还可以用高锰酸钾和浓盐酸反应制取氯气,完成并配平该反应的离子方程式:
____ MnO4-+ ____ H+ + ____ Cl- ____ Mn2+ + ____ Cl2↑+ ____ _________
____ Mn2+ + ____ Cl2↑+ ____ _________
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,通过下列反应可实现燃煤烟气中硫的回收:
SO2(g)+2CO(g) 2CO2(g)+S(l) △H<0 若反应在恒容的密闭容器中进行,下列有关说法正确的是
2CO2(g)+S(l) △H<0 若反应在恒容的密闭容器中进行,下列有关说法正确的是
A.平衡前,随着反应的进行,容器内压强始终不变
B.平衡时,其他条件不变,分离出硫,正反应速率加快
C.平衡时,其他条件不变,升高温度可提高SO2的转化率
D.其他条件不变,使用不同催化剂,该反应的平衡常数不变
查看答案和解析>>
科目:高中化学 来源: 题型:
在密闭容器中进行如下反应:H2(g)+I2(g) 2HI(g),在温度T1和T2时,产物的量与反应时间的关系如下图所示,符合图示的正确判断是
2HI(g),在温度T1和T2时,产物的量与反应时间的关系如下图所示,符合图示的正确判断是
A.T1>T2,△H>0
B.T1> T2,△H<0
C.T1 <T2,△H>0
D.T1 < T2,△H<0
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、L、M、N六种元素的原子序数依次增大。X、Y、Z、L是组成蛋白质的基础元素,M是短周期原子半径最大的元素,N是地壳中含量最高的金属元素。
用化学用语回答下列问题:
(1) M在元素周期表中的位置为 ;六种元素的原子半径从大到小的顺序是
(2)Z、X两元素按原子数目比l∶3构成分子A, A的电子式为
Y、L两元素按原子数目比l∶2构成分子B,B中所含的化学键类型为
(3)硒(se)是人体必需的微量元素,已知非金属性:34Se<L。请结合原子结构解释原因
(4)用Y、L、M构成的正盐溶液可以清除油污,请结合离子方程式以及必要的文字解释原因
(5)用石墨作电极,NCl3溶液作电解液进行电解,生成难溶物R,R受热分解生成化合物Q。写出电解熔融Q制取N的电极方程式:阳极: ;阴极:
查看答案和解析>>
科目:高中化学 来源: 题型:
已知常温下氯酸钾与浓盐酸反应能放出氯气,现按右下图进行氯气的性质实验。玻璃管内分别装有滴有少量不同溶液的白色棉球,反应—段时间后,对图中指定部位颜色描述正确的是

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com