
| A. | 化学是在原子、分子水平上研究物质的组成、结构、性质、制备等的自然科学 | |
| B. | 化学是一门具有创造性的科学,可以利用化学知识创造出自然界中不存在的物质 | |
| C. | 化学的发展经过了从宏观到微观,从感性到理性的逐步深化的过程 | |
| D. | 随着化学的发展,人们最终会实现通过化学变化使水变油的梦想 |
分析 A.化学在微观水平上研究物质的组成、结构、性质、变化、制备和应用等方面;
B.化学科学具有创造性;
C.化学的发展从宏观到微观,从感性到理性;
D.根据质量守恒定律进行解答.
解答 解:A.化学科学是一门重要的自然科学,是在微观水平上研究物质的组成、结构、性质、变化、制备和应用等方面,故A正确;
B.化学科学具有创造性,认识分子和制造分子是化学的特征,故B正确;
C.化学的发展从宏观到微观,从感性到理性,逐步深化,故C正确;
D.水中不含有碳元素,而油主要成分为碳氢化合物,所以由质量守恒定律可知,水变油(主要成分为碳氢化合物)理论上不可以通过化学变化实现,故D错误.
故选D.
点评 本题考查了化学的概念、化学的外延、化学与生产生活的关系等知识点,根据其概念的内涵、化学的作用等知识点来分析解答即可,难度不大.


 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案科目:高中化学 来源: 题型:解答题
 ,不考虑立体异构)是临床上使用广泛的药物.下图所示的为其多条合成路线中的一条(反应试剂和反应条件均未标出)
,不考虑立体异构)是临床上使用广泛的药物.下图所示的为其多条合成路线中的一条(反应试剂和反应条件均未标出)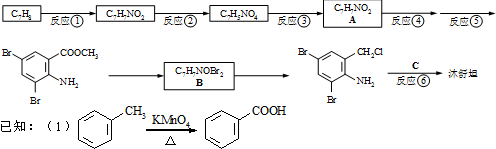
 +2
+2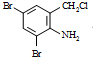 +K2CO3→2
+K2CO3→2 +2KCl+CO2↑+H2O
+2KCl+CO2↑+H2O B
B
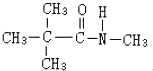 、
、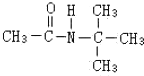
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
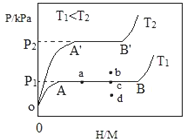 合金贮氢材料具有优异的吸收氢性能,在配合氢能的开发中起到重要作用.
合金贮氢材料具有优异的吸收氢性能,在配合氢能的开发中起到重要作用.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(H+)=10-13mol/L的溶液中:NO3-、S2O32-、K+、Na+ | |
| B. | 酸性高锰酸钾溶液中:Na+、C2O42-、CH3COO -、NH4+ | |
| C. | 澄清石灰水中:HCO3-、Ba2+、Cl-、NO3- | |
| D. | 空气中:SO2、NO、N2、NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向碳酸氢钙溶液中加过量氢氧化钠Ca2++2HCO3-+2OH-═CaCO3↓+2H2O+CO32- | |
| B. | 等体积等物质的量浓度的氢氧化钡溶液与碳酸氢铵溶液混合Ba2++OH-+HCO3-═BaCO3↓+H2O | |
| C. | 氯化铝与过量氨水反应 Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | |
| D. | 过量CO2通入氢氧化钡的稀溶液中 CO2+OH-═HCO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com