
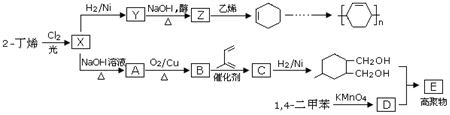
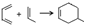 .
.分析 2-丁烯和氯气在光照条件下发生取代反应生成X,Z和乙烯发生加成反应生成环己烯,则Z为CH2=CHCH=CH2,Y和氢氧化钠的醇溶液发生消去反应生成Z,X和氢气发生加成反应生成Y,则Y为CH2ClCH2CH2CH2Cl,X为CH2ClCH=CHCH2Cl,X和氢氧化钠水溶液发生取代反应生成A,A为HOCH2CH=CHCH2OH,A发生催化氧化反应生成B,B为OHCCH=CHCHO,B和2-甲基-1,3-丁二烯发生加成反应生成C,C为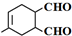 ,1,4-二甲苯被酸性高锰酸钾溶液氧化生成D,D结构简式为1,4-二苯甲酸,发生缩聚反应生成高聚物E,E结构简式为
,1,4-二甲苯被酸性高锰酸钾溶液氧化生成D,D结构简式为1,4-二苯甲酸,发生缩聚反应生成高聚物E,E结构简式为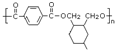 ,以此来解答.
,以此来解答.
解答 解:(1)X为CH2ClCH=CHCH2Cl,含有的官能团名称为氯原子、碳碳双键,
故答案为:氯原子、碳碳双键;
(2)Y发生消去反应生成Z,反应方程式为ClCH2CH2CH2CH2Cl+2NaOH$→_{△}^{醇}$CH2=CH-CH=CH2+2NaCl+2H2O;甲是A的一种同分异构体,A结构简式为HOCH2CH=CHCH2OH,能实现转化:甲$\stackrel{H_{2}O}{→}$乙+丙,甲能发生水解反应,则甲是酯,甲水解生成乙和丙,乙能被氧化生成丁,丁能被氧化生成丙,则乙、丙、丁中C原子个数相等,乙为CH3CH2OH、丁为CH3CHO、丙为CH3COOH,则甲是乙酸乙酯,
故答案为:ClCH2CH2CH2CH2Cl+2NaOH$→_{△}^{醇}$CH2=CH-CH=CH2+2NaCl+2H2O;乙酸乙酯;
(3)Y为CH2ClCH2CH2CH2Cl,Y中官能团的检验方法为向Y中加入NaOH水溶液(或NaOH醇溶液)、加热后,冷却,再加硝酸至酸性,滴加硝酸银溶液观察生成白色沉淀,
故答案为:向Y中加入NaOH水溶液(或NaOH醇溶液)、加热后,冷却,再加硝酸至酸性,滴加硝酸银溶液观察生成白色沉淀.
点评 本题考查有机物的合成,为高频考点,把握官能团的变化、碳链变化、有机反应为解答的关键,侧重分析与应用能力的考查,注意有机物性质的应用,题目难度不大.


科目:高中化学 来源: 题型:实验题
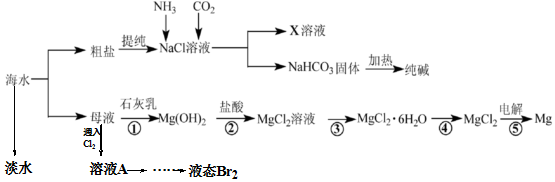
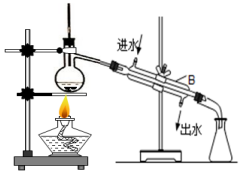
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蒸馏法是海水谈化的方法之一 | |
| B. | 海水中的${\;}_{92}^{235}$U元素经浓缩提炼后可作核反应堆燃料 | |
| C. | 海水中的Li元素属于微量元素,提炼后可作Li电池原料 | |
| D. | 0℃以上,温度越高,水的密度越小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

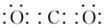 ,若在C池中生成64gCu,则整个装置中共生成H2SO42mol.
,若在C池中生成64gCu,则整个装置中共生成H2SO42mol.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 2-叔丁基对苯二酚是一种重要的食品抗氧剂,现以对苯二酚、叔丁醇为原料,一定条件下经Freidel-Crafts 烷基化反应合成.原理如下:
2-叔丁基对苯二酚是一种重要的食品抗氧剂,现以对苯二酚、叔丁醇为原料,一定条件下经Freidel-Crafts 烷基化反应合成.原理如下: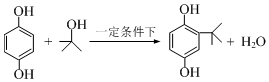
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 温度升高,Na2CO3溶液的Ksp和c(OH-)均会增大 | |
| B. | 沉淀转化的离子方程式为CO32-(aq)+CaSO4(s)?CaCO3(s)+SO42-(aq) | |
| C. | 该条件下,CaCO3的溶解度约为1×10-3g | |
| D. | CaCO3和CaSO4共存的悬浊液中,$\frac{c(S{{O}_{4}}^{2-})}{c(C{{O}_{3}}^{2-})}$=9×104 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 I2在KI溶液中存在平衡:I2(aq)+I-(aq)?I3-(aq),某I2、KI混合溶液中,c($I_3^-$)与温度T的平衡曲线图如图.下列说法不正确的是( )
I2在KI溶液中存在平衡:I2(aq)+I-(aq)?I3-(aq),某I2、KI混合溶液中,c($I_3^-$)与温度T的平衡曲线图如图.下列说法不正确的是( )| A. | 反应I2(aq)+I-(aq)?I3-(aq) 的△H>0 | |
| B. | 若温度为T1、T2,反应的平衡常数分别为 K1、K2,则K1>K2 | |
| C. | 若反应进行到状态D时,一定有v正>v逆 | |
| D. | 状态A与状态B相比,状态A的c (I2) 小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com