
| A、在密闭容器中加入1mol N2和3mol H2充分反应放热92.4kJ |
| B、N2(g)+3H2(g)?2NH3(l)△H=-QkJ?mo1-1,则Q>92.4 |
| C、增大压强,平衡向右移动,平衡常数增大 |
| D、若一定条件下反应达到平衡,N2的转化率为20%,则H2的转化率一定为60% |


 全能练考卷系列答案
全能练考卷系列答案 一课一练课时达标系列答案
一课一练课时达标系列答案科目:高中化学 来源: 题型:
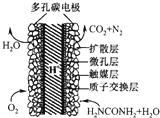 电化学化学家正在研究尿素动力燃料电池,尿液也能发电.用这种电池直接去除城市废水中的尿素,既能产生净化的水,又能发电.尿素燃料电池结构如图所示,下列关于该电池描述正确的是( )
电化学化学家正在研究尿素动力燃料电池,尿液也能发电.用这种电池直接去除城市废水中的尿素,既能产生净化的水,又能发电.尿素燃料电池结构如图所示,下列关于该电池描述正确的是( )| A、电池工作时H+移向负极 |
| B、该装置还可以将电能转化成为化学能 |
| C、电池的负极反应式为:CO(NH2)2+H2O-6e-=CO2+N2+6H+ |
| D、理论上电池工作时,每消耗67.2L O2时,可以净化2mol CO(NH2)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验器材和试剂 | 相应实验 |
| A | 洗气瓶(两只)、饱和Na2CO3溶液、浓硫酸 | 除去CO2中的HCl和水蒸气 |
| B | 滴定台(附滴定夹)、滴定管(酸式、碱式)、烧杯、胶头滴管 | 中和滴定实验 |
| C | 烧杯、酒精灯、火柴、胶头滴管、蒸馏水、FeCl3饱和溶液 | 制备Fe(OH)3胶体 |
| D | 铂丝或铁丝、蓝色钴玻璃、酒精灯、火柴、盐酸、待测液 | 焰色反应实验 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、使甲基橙变红色的溶液:K+、Al3+、MnO4-、C2O42- |
| B、加入铝产生氢气的溶液:H+、Mg2+、NO3-、SO42- |
| C、pH=12的溶液中:Na+、Ba2+、NO3-、Cl- |
| D、含Al2Fe(SO4)4的溶液:Na+、NH4+、S2O32-、ClO- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、PM2.5是指大气中直径≤2.5微米的颗粒物,只要戴普通口罩就对人体健康无影响 |
| B、绚丽缤纷的烟花中可能添加了含钾、钠、钙、铜等某些金属元素的化合物 |
| C、乙醇、过氧化氢、次氯酸钠等消毒液均可以将病毒氧化而达到消毒的目的 |
| D、地沟油的主要成分是高级脂肪酸甘油酯,可用于制肥皂和加工食用油 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙烯聚合为聚乙烯高分子材料 |
| B、甲烷与氯气制备一氯甲烷 |
| C、以铜和浓硝酸为原料生产硝酸铜 |
| D、乙醇催化氧化制乙醛 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铁粉加入稀硫酸中:2Fe+6H+═2Fe3++3H2↑ |
| B、钠投入水中:Na+H2O═Na++2OH-+H2↑ |
| C、氯化铝溶液中加入过量氨水:Al3++3NH3?H2O═Al(OH)3↓+3NH4+ |
| D、氢氧化钡溶液滴入稀硫酸中:Ba2++OH-+H++SO42-═BaSO4↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com