
工业上将苯蒸气通过赤热的铁合成一种传热载体化合物,其分子中苯环上的一氯取代物有3种,1 mol该化合物催化加氢时最多消耗6 mol H2,则该传热载体化合物的结构简式是

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016-2017学年广西桂林十八中高一上期中化学试卷(解析版) 题型:实验题
(1)所需要的仪器为:托盘天平、量筒、烧杯、玻璃棒、_________、_________。
(2)配制该溶液需要Na2CO3的质量为_________g。
(3)配制溶液的操作顺序是(填序号)_________。
①转移溶液;②轻摇使溶液混合均匀; ③洗涤并转移洗涤液; ④加盖倒转摇匀溶液; ⑤定容;⑥称量; ⑦溶解 ⑧计算
(4)正式配制前必须进行的一项实验操作是__________________。
(5)试分析下列操作对所配溶液的浓度有何影响:(填写编号)A.偏高;B.不变;C.偏低。
①配制溶液时未洗涤烧杯并转移洗涤液_________;
②定容、加盖倒转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度线_________;
③定容时俯视刻度线_________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广西桂林十八中高二上期中文化学卷(解析版) 题型:选择题
可逆反应CO(g)+H2O(g)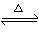 CO2(g)+H2(g),达到平衡后,有关化学反应限度的说法正确的是
CO2(g)+H2(g),达到平衡后,有关化学反应限度的说法正确的是
A.V正=0 B.V逆=0 C.V正=V逆≠0 D.V正= V逆=0
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广西桂林十八中高二上期中理化学卷(解析版) 题型:选择题
下列说法正确的是
A.室温下,在水中的溶解度:丙三醇>苯酚>1—氯丁烷
B.用核磁共振氢谱不能区分HCOOCH3和HCOOCH2CH3
C.用Na2CO3溶液不能区分CH3COOH和CH3COOCH2CH3
D.油脂在酸性或碱性条件下均能发生水解反应,且产物相同
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广西桂林十八中高二上期中理化学卷(解析版) 题型:选择题
烯烃在一定条件下发生氧化反应时,碳碳双键发生断裂,RCH==CHR1可以氧化成RCHO和R1CHO。在该条件下,下列烯烃分别被氧化后,产物中可能有乙醛的是
A.CH3CH2CH==CHC H2CH3 B.CH
H2CH3 B.CH 2==CHCH2CH2CH3
2==CHCH2CH2CH3
C.CH3CH==CHCH2CH2CH3 D.CH3CH2CH== C(CH3)2
查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上学期统练二化学试卷(解析版) 题型:填空题
工业上利用CO和水蒸气在一定条件下发生反应制取氢气:
CO(g)+H2O(g) CO2(g)+H2(g) △H=-41kJ /mol
CO2(g)+H2(g) △H=-41kJ /mol
某小组研究在相同温度下该反应过程中的能量变化。他们分別在体积均为V L的两个恒温恒容密闭容器中加入一定量的反应物,使其在相同温度下发生反应。相关数据如下:
容器 编号 | 起始时各物质物质的M/mol | 达到平衡的时间/min | 达平衡时体系能量 的变化/kJ | |||
CO | H2O | CO2 | H2 | |||
① | 1 | 4 | 0 | 0 | t1 | 放出热量: 32.8 kJ |
② | 2 | 8 | 0 | 0 | t2 | 放出热量:Q |
(1)该反应过程中,反应物分子化学键断裂时所吸收的总能量________(填“大于”、“小于”或“等于”)生成物分子化学键形成时所释放的总能量。
(2)容器①中反应达平衡时,CO的转化率为__________%。
(3)计算容器②中反应的平衡常数K=___________。
(4)下列叙述正确的是________(填字母序号)。
A.平衡时,两容器中H2的体积分数相等
B.容器②中反应达平衡状态时Q>65.6kJ
C.反应开始时,两容器中反应的化学反应速率相等
D.平衡时两容器中正反应速率相等
(5)容器①中反应进行到tmin时,测得混合气体中CO2的物质的量为0.6 mol。若用200 mL 5 mol/L的NaOH溶液将其完全吸收,反应的离子方程式为(用一个离子方程式表示)____________。
查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上学期统练二化学试卷(解析版) 题型:选择题
下列有关说法正确的是( )
A.化学平衡向正向移动,反应物浓度一定降低
B.化学平衡向正向移动,生成物的浓度一定增加
C.化学平衡向正向移动,反应物的转化率一定增大
D.化学平衡向正向移动时,正反应速率一定大于逆反应速率
查看答案和解析>>
科目:高中化学 来源:2016-2017学年云南省高二上期中化学试卷(解析版) 题型:实验题
环境监测测定水中溶解氧的方法是:
①量取a mL水样,迅速加固剂MnSO2溶液和碱性KI溶液(含KOH),立即塞好塞子并振荡摇匀,使之充分反应,其反应式为:2Mn2++O2+4OH-=2MnO(OH)2(该反应极快)
②测定:开塞后迅速加入1mL~2mL浓硫酸(提供H+),使之生成I2,再用bmol/L的Na2S2O3溶液滴定(以淀粉为指示剂),共消耗Na2S2O3溶液V mL。有关反应式为:
MnO(OH)2+2I-+4H+=Mn2++I2+2H2O;I2+2S2O32-=2I-+S4O62-
试回答:
(1)水中溶解氧的计算式是(以g/L为单位)为_____________;
(2)滴定(I2和S2O32-反应)以淀粉为指示剂,终点时溶液由___________色变为__________色;
(3)测定时,滴定管经蒸馏水洗涤后加滴定剂Na2S2O3溶液,导致测定结果_____________(填偏低、偏高、无影响);
(4)记录测定结果时,滴定前仰视刻度线,滴定到达终点时又俯视刻度线,将导致滴定结果_____________(填偏低、偏高、无影响);
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com