
2008年5月我国汶川发生地震灾害,假若你是卫生防疫人员,为配制0.01 mol/L的KMnO4消毒液,下列操作导致所配溶液浓度偏高的是
A.取KMnO4样品时不慎在表面沾了点蒸馏水
B.溶解搅拌时有液体飞溅
C.定容时俯视容量瓶刻度线
D.摇匀后见液面下降,再加水至刻度线
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
现有以下物质:①NaCl晶体, ②SO3, ③纯醋酸, ④BaSO4晶体,⑤蔗糖,⑥乙醇,⑦熔融KNO3,请回答下列问题(填序号):
(1)以上物质中能导电的是 ;
(2)以上物质中属于非电解质,但其水溶液可以导电的是________________________;
(3)以上物质中属于弱电解质的是_____________________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应既是氧化还原反应又是吸热反应的是:
A.铝片与稀硫酸的反应 B.Ba(OH)2·8H2O与NH4Cl 的反应
C. 灼热的炭与CO2 D.加热才能与氧气发生的反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
可逆反应mA(g)+nB pC(g)+qD中,A和C都是无色气体,达到平衡后,下列叙述正确的是
pC(g)+qD中,A和C都是无色气体,达到平衡后,下列叙述正确的是
A.若增加B的量,平衡体系颜色加深,说明B必是气体
B.增大压强,平衡不移动,说明m+n一定等于p+q
C.升高温度,A的转化率减小,说明正反应是吸热反应
D.若B是气体,增大A的量,A、B的转化率都增大
查看答案和解析>>
科目:高中化学 来源: 题型:
在一容积为2 L的密闭容器内加入0.2 molA和0.6 molB,在一定条件下发生反应:A(s)+3B(g) 2C(s)+3D(g) 已知该反应在不同温度下的平衡常数如下表:
2C(s)+3D(g) 已知该反应在不同温度下的平衡常数如下表:
| 温度/℃ | 1000 | 1150 | 1300 |
| 平衡常数 | 64.0 | 50.7 | 42.9 |
请回答下列问题:
⑴该反应的平衡常数表达式K= ,ΔH 0(填“>”或“<”)。
⑵1000 ℃时,4 min后达到平衡.求4 min内D的平均反应速率v(D)= ,B的平衡转化率为 ,平衡时B的体积分数 。
⑶欲提高⑵中B的平衡转化率,可采取的措施是
A.减少C的量 B.增加A的量 C.移出部分D
D.降低反应温度 E.减小容器的容积 F.加入合适的催化剂
⑷1000 ℃时, 在一容积为2 L的密闭容器内加入XmolC和0.6 molD,5 min后达到平衡,B的浓度与⑵中B的浓度相同,求X的范围
⑸下列说法中能说明反应已达到平衡状态的是
A.容器内混合气体的压强不随时间变化而变
B.B的速率不随时间的变化而变化
C.c(B)︰c(D)=1︰1
D.混合气体的密度保持不变(M(B)≠M(D))
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)下列实验操作或对实验事实的描述不正确的是 (填序号)。
A.不宜用瓷坩埚灼烧氢氧化钠或碳酸钠
B.使用容量瓶配制溶液时,俯视刻度线定容后所得溶液浓度偏大
C.分液操作时,由于分液漏斗下端已沾满下层液体,故上层液体要从上口倒出
D.用托盘天平称量11.74g氯化钠晶体
E.用结晶法分离硝酸钾和氯化钠的混合物
(2)实验室需要0.1 mol·L-1NaOH溶液450 moL和0.5 mol·L-1硫酸溶液500 mL。根据这两种溶液的配制情况回答下列问题:
①如图所示的仪器中配制溶液肯定不需要的是 (填序号);配制上述溶液还需用到的玻璃仪器是 (填仪器名称)。
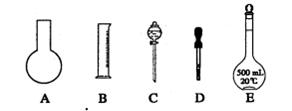
②下列操作中,容量瓶所不具备的功能有 (填序号)。
A.配制一定体积准确浓度的标准溶液
B.贮存溶液
C.测量容量瓶规格以下的任意体积的液体
D.准确稀释某一浓度的溶液
E.用来加热溶解固体溶质
③请计算需用托盘天平称取固体NaOH的质量为 g。某同学用托盘天平称量烧杯的质量,天平平衡后的状态如图.由图中可以看出,烧杯的实际质量为 g。
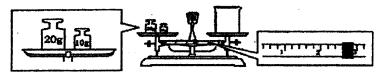
④根据计算得知,所需质量分数为98%、密度为I.84 g·cm-3的浓硫酸的体积为 mL(计算结果保留一位小数)。配制过程中需先在烧杯中将浓硫酸进行稀释,稀释时操作方法是 。
【答案】(1)D (2)①A C; 烧杯、玻璃棒 ②B C E ③ 2.0;27.4
④13.6; 将浓硫酸沿烧杯内壁缓缓注入水中,并用玻璃棒不断搅拌。
查看答案和解析>>
科目:高中化学 来源: 题型:
用标准盐酸滴定未知浓度的NaOH溶液,下列各操作中,不会引起实验误差的是
A.用蒸馏水冼净滴定管后,装入标准盐酸进行滴定
B.用蒸馏水冼净锥形瓶后,再用NaOH液润洗,而后装入一定体积的NaOH溶液
C.用甲基橙做指示剂,当溶液由黄色变成橙色,立刻读数盐酸体积。
D.用碱式滴定管取10.00 mLNaOH溶液放入用蒸馏水洗净的锥形瓶中,再加入适量蒸馏水进行滴定
查看答案和解析>>
科目:高中化学 来源: 题型:
实验成功离不开正确的操作及数据记录。实验操作、记录正确的是
A.滴定管装液前只需水洗、润洗 B.在通风橱中取用溴
C.用pH试纸测得某氯水的pH为2 D.用100 mL量筒取70.5 mL蒸馏水
查看答案和解析>>
科目:高中化学 来源: 题型:
从柑橘中炼制萜二烯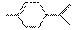 ,下列有关它的推测,不正确的是 ( )
,下列有关它的推测,不正确的是 ( )
A、它不能使酸性高锰酸钾溶液褪色
B、常温下为液态,难溶于水
C、分子式为C10H16
D、与过量的溴的CCl4溶液反应后产物如右图

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com