
下列有关热化学方程式的叙述不正确的是( )
A.已知2H2(g)+O2(g)= 2H2O(g);△H=-483.6 kJ/mol,则氢气的燃烧热为241.8 kJ/mol
B.已知C(石墨,s)= C(金刚石,s);△H>0,则石墨比金刚石稳定
C.含20.0g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量,则该反应中和热的热化学方程式为:NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l);△H=-57.4 kJ/mol
D.已知2C(s)+2O2(g)=2CO2(g);△H1,2C(s)+O2(g)=2CO(g) ;△H2。则△H1<△H2
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
“纳米材料”(1 nm=10-9m )是指研究开发直径为几纳米至几十纳米的材料。如将“纳米材料”分散到某液体中,对于所得分散系的叙述不正确的是
A.光束通过此分散系时会形成一条光亮的“通路”
B.此分散系中“纳米材料”的粒子在做不停的、无序的运动
C.用滤纸过滤的方法可以从此分散系中分离得到该“纳米材料”
D.在外加电场作用下,“纳米材料”的粒子可能向某一极做定向运动
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.胶体区别于其他分散系的本质特征是分散质微粒直径在1 nm~100 nm之间
B.NH3的沸点高于PH3,是因为N-H键能大于P-H键能
C.金属阳离子只存在于离子晶体中
D.由非金属元素组成的化合物一定是共价化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
Ⅰ 碘钨灯具有使用寿命长、节能环保等优点。一定温度下,在碘钨灯灯泡内封存的少量碘与沉积在灯泡壁上的钨可以发生如下的可逆反应:
W(s)+ I2(g)  WI2(g)
WI2(g)
为模拟上述反应,在实验室中准确称
 取0.508 g 碘、0.736 g金属钨放置于50.0
取0.508 g 碘、0.736 g金属钨放置于50.0
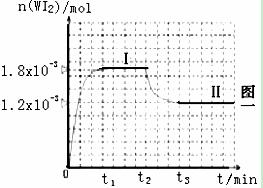
mL密闭容器中,并加热使其反应。右图一
是混合气体中的WI2蒸气的物质的量随时
间变化关系的图像[n(WI2) ~ t],其中
曲线Ⅰ(0~t2时间段)的反应温度为450℃,
曲线Ⅱ(从t2时刻开始)的反应温度为530℃。
请回答下列问题:
(1)该反应是 (填写“放热”“吸热”)反应。
(2)反应从开始到t1(t1= 3 min)时间内的平均速率υ(I2)= mol/(L.min)。
(3)在450℃时,计算该反应的平衡常数K= 。
(4)能够说明上述反应已经达到平衡状态的有 。
A.I2与WI2的浓度相等
B.单位时间内,金属钨消耗的物质的量与单质碘生成的物质的量相等
 C.容器内混合气体的密度不再增加
C.容器内混合气体的密度不再增加
D.容器内气体压强不变化
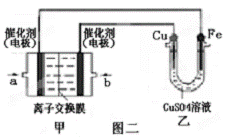
Ⅱ 图二中甲为甲醇燃料电池(电解质溶
液为KOH溶液),该同学想在乙中实
现铁上镀铜,则a处电极上发生的电
极反应式是 。
Ⅲ 已知:H2(g)、CO(g)和CH3CH2OH(l)的燃烧热
分别为285.8 kJ·mol-1、283.0 kJ·mol-1和1365.5 kJ·mol-1。
反应 2CO(g)+4H2(g) CH3CH2OH(l)+H2O(l) 的△H= 。
CH3CH2OH(l)+H2O(l) 的△H= 。
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿佛加德罗常数,下列说法正确的是( )
A. 300 mL 2 mol·L-1的蔗糖溶液中所含分子数为0.6NA
B. 在标准状况下,2.8g N2和2.8g CO所含电子数不相等
C. 0.2 mol H2O2完全分解转移的电子数为0.2NA
D.在常温常压下,2.24L SO2与O2的混合气体中所含氧原子数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
将12.8gMg、Al、Fe组成的合金溶于足量的NaOH溶液中,可产生0.3mol气体。另取等质量合金溶于过量稀硝酸中,生成NO气体,向反应后的溶液中加入NaOH溶液恰好使Mg2+、Al3+、Fe3+完全转化为沉淀,其质量为38.3g,则上述反应中生成NO气体的体积(标准状况下)为( )
A. 11.2L B. 33.6L C. 22.4L D.6.72L
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于阿伏加德罗常数的说法正确的是( )
A.阿伏加德罗常数是12 g碳中所含的碳原子数
B.阿伏加德罗常数是0.012 kg 12C中所含的原子数
C.阿伏加德罗常数是6.02×1023
D.阿伏加德罗常数的符号为NA,近似为6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
20℃时,饱和KCl溶液的密度为1.174 g·cm-3,物质的量浓度为4.0 mol·L-1,则下列说法中不正确的是( )
A.25℃时,饱和KCl溶液的浓度大于4.0 mol·L-1
B.此溶液中KCl的质量分数为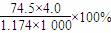
C.20℃时,密度小于1.174 g·cm-3的KCl溶液是不饱和溶液
D.将此溶液蒸发部分水,再恢复到20℃时,溶液密度一定大于1.174 g·cm-3
查看答案和解析>>
科目:高中化学 来源: 题型:
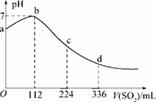
标准状况下,某同学向100 mLH2S饱和溶液中通入SO2,所得溶液pH变化如图所示,下列分析中,正确的是( )
A.ab段反应是:SO2+2H2S===3S↓+2H2O
B.亚硫酸是比氢硫酸更弱的酸
C.原H2S溶液的物质的量浓度为0.05 mol/L
D.b点对应的溶液导电性最强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com