
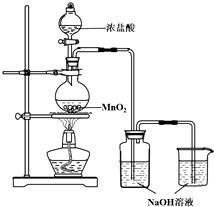
 某实验小组用如图装置制备家用消毒液,并探究其性质.
某实验小组用如图装置制备家用消毒液,并探究其性质.| 操作 | 现象 |
| a.测溶液pH,并向其中滴加2滴酚酞 | pH=13,溶液变红,5min后褪色 |
| b.向其中逐滴加入盐酸 | 溶液逐渐变成黄绿色 |
| 操作 | 现象 |
| 取5mL pH=13NaOH溶液,向其中滴加2滴酚酞 | 溶液变红,30min后褪色 |
分析 制备家用消毒液,并探究其性质:装置A:盐酸和二氧化锰在加热条件下反应生成氯气、氯化锰和水,4HCl+MnO2$\frac{\underline{\;\;△\;\;}}{\;}$Cl2↑+MnCl2+2H2O,装置B:氯气和氢氧化钠反应:
Cl2+2NaOH═NaClO+NaCl+H2O,制得消毒液,氯气有毒,尾气需用氢氧化钠吸收.
(1)制备消毒液涉及反应为制取氯气,氯气和碱反应生成消毒液;
(2)同体积、同PH=13的溶液中,30min后褪色,而消毒液,5min后褪色,通过对比实验,得出此实验小组制备的消毒液具有漂白性;
(3)①操作b中溶液变成黄绿色为氯气,是因为氯离子、次氯酸根离子在酸性条件下发生氧化还原反应,生成氯气;
②用硫酸代替盐酸,据此判断是否为氯元素的价态归中生成氯气;
(4)①碘单质遇淀粉显示蓝色,根据滴定终点碘单质消耗,判断颜色变化;
②ClO-具有强氧化性,酸性条件下,将I-氧化为I2,自身被还有为Cl-,同时生成H2O,发生离子反应为:2I-+ClO-+2H+=I2+Cl-+H2O,结合2Na2S2O3+I2=Na2S4O6+2NaI,2H++ClO-+Cl-═Cl2↑+H2O,可得关系式2Cl2~2ClO-~2I2~4Na2S2O3,据此计算单位质量的含氯消毒液在酸性条件下所能释放出氯气的质量,进而计算此消毒液有效氯含量.
解答 解:(1)消毒液的主要成分为次氯酸钠,利用上述装置制备消毒液,首先在装置A:盐酸和二氧化锰在加热条件下反应生成氯气、氯化锰和水,4HCl+MnO2$\frac{\underline{\;\;△\;\;}}{\;}$Cl2↑+MnCl2+2H2O,其次在装置B:氯气和氢氧化钠反应:Cl2+2NaOH═NaClO+NaCl+H2O,制得消毒液,
故答案为:4HCl+MnO2$\frac{\underline{\;\;△\;\;}}{\;}$Cl2↑+MnCl2+2H2O;Cl2+2NaOH═NaClO+NaCl+H2O;
(2)酚酞在强碱性溶液中红色会褪去,但同样体积、同PH值的氢氧化钠溶液,滴加2滴酚酞溶液变红,30min后褪色,而消毒液,pH=13,溶液变红,5min后褪色,褪色时间短,说明此实验小组制备的消毒液具有漂白性,
故答案为:5mL pH=13;漂白性;
(3)①次氯酸根中氯为+1价,氯离子为-1价,在酸性条件下发生归中反应,生成氯气,反应为:2H++ClO-+Cl-═Cl2↑+H2O,黄绿色气体为氯气,
故答案为:2H++ClO-+Cl-═Cl2↑+H2O;
②操作b中溶液变成黄绿色,有同学认为氯元素的价态归中生成氯气结论并不严谨,需要进一步确认此结论,可由硫酸替代酸性条件,取洗气瓶中溶液5mL,向其中逐滴加入硫酸,观察溶液是否逐渐变为黄绿色,若没有,操作b获得上述结论严谨,
故答案为:取洗气瓶中溶液5mL,向其中逐滴加入硫酸,观察溶液是否逐渐变为黄绿色;
(4)①碘单质遇淀粉显示蓝色,用0.1mol•L-1Na2S2O3溶液滴定生成的I2,溶液蓝色褪去且半分钟内不恢复,达到滴定终点,
故答案为:溶液蓝色褪去且半分钟恢复;
②ClO-具有强氧化性,酸性条件下,将I-氧化为I2,自身被还有为Cl-,同时生成H2O,发生离子反应为:2I-+ClO-+2H+=I2+Cl-+H2O,结合2Na2S2O3+I2=Na2S4O6+2NaI,可得关系式2ClO-~2I2~4Na2S2O3,有效氯指单位质量的含氯消毒液在酸性条件下所能释放出氯气的质量,2H++ClO-+Cl-═Cl2↑+H2O,根据2ClO-~2Cl2~4Na2S2O3,$\frac{0.1mol/L×20×1{0}^{-3}L}{\frac{4}{5g}}×2×71g/mol$×100%=1.42%,
故答案为:1.42%.
点评 本题以消毒液考查物质的成分及含量的探究,明确物质的性质及发生的化学反应为解答的关键,注意计算中量的关系为解答的易错点,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 司母戊鼎、定远舰甲板、有机玻璃等原材料属于合金 | |
| B. | 氯气是塑料、合成橡胶、合成纤维、农药、染料及药品的重要原料 | |
| C. | 工业上生产玻璃、水泥、漂白粉均需要用石灰石为原料 | |
| D. | 用浸泡过溴的四氯化碳溶液的硅藻土吸收水果产生的乙烯以达到保鲜目的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.15mol/L | B. | 0.10mol/L | C. | 0.50mol/L | D. | 0.20mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | 结构或性质信息 |
| T | 原子的L层上s电子数等于p电子数. |
| X | 元素的原子半径是第三周期主族元素中最大的. |
| Y | 空气中含其单质,原子的最外层未成对电子数是该元素所在周期中最多的. |
| Z | 单质常温、常压下是气体.原子的M层上有1个未成对的p电子. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
| 主要化合价 | +2 | +3 | +6,-2 | +2 | -2 |
| A. | L与Q形成的化合物化学式为LQ | |
| B. | L、M的单质与稀盐酸反应剧烈程度:M>L | |
| C. | Q、T的氢化物在常温常压下均为无色气体 | |
| D. | M的最高价氧化物的水化物不具有两性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com