
【题目】在标准状况下,ag气体x与bg气体y的分子数相同,下列说法正确的是( )
A.标准状况下,等质量的x和y体积之比为b:a
B.同温同压下,气体x和气体y的密度之比为 b:a
C.25℃时,1g气体x和1g气体y的原子数之比为b:a
D.同物质的量的气体x和气体y的质量之比为b:a
【答案】A
【解析】解:ag气体X与b g气体y的分子数相同,根据N=nNA可知,二者物质的量相等,根据M= ![]() 可知x与y的摩尔质量之比为a:b, A.同温同压下,体积之比等于物质的量之比,根据n=
可知x与y的摩尔质量之比为a:b, A.同温同压下,体积之比等于物质的量之比,根据n= ![]() 可知,相同质量时,其体积之比与其摩尔质量的反比,故标准状况下,等质量的x和y体积之比为b:a,故A正确;
可知,相同质量时,其体积之比与其摩尔质量的反比,故标准状况下,等质量的x和y体积之比为b:a,故A正确;
B.同温同压下,两气体的密度之比等于其摩尔质量之比,则二者的密度之比=a:b,故B错误;
C.不能确定每个x、y分子含有原子数目,无法计算含有原子数目之比,故C错误;
D.根据m=nM知,相同物质的量时,其质量之比=摩尔质量之比=a:b,故D错误;
故选A.
a g气体X与b g气体y的分子数相同,根据N=nNA可知,二者物质的量相等,根据M= ![]() 可知x与y的摩尔质量之比为a:b,
可知x与y的摩尔质量之比为a:b,
A.同温同压下,体积之比等于物质的量之比,结合n= ![]() 判断;
判断;
B.同温同压下,两气体的密度之比等于其摩尔质量之比;
C.不能确定每个x、y分子含有原子数目,无法计算含有原子数目之比;
D.根据m=nM判断其质量之比.


科目:高中化学 来源: 题型:
【题目】从一个关系量的单位,我们可以得出该量的计算公式,如:从摩尔质量的单位:gmol﹣1 , 可得出分子应当是质量、分母应当是物质的量,因此摩尔质量的计算公式为 M=m/n,以此类推,物质的量浓度单位是 ,其计算公式c= ;由微粒个数与物质的量的关系推出阿佛加德罗常数的公式NA= ;气体摩尔体积的单位是 ,其计算公式是Vm= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面对硝酸的认识不正确的是( )
A. 浓硝酸和稀硝酸都具有氧化性B. 铜与稀硝酸的反应属于置换反应
C. 金属与硝酸反应一定不产生氢气D. 可用铁或铝制品盛装浓硝酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1994年科学家发现一种元素,它的核内有161个中子,质量数为272,该元素原子序数是( )
A. 111B. 161C. 272D. 443
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语的表达正确的是( )
A.二氧化碳的比例模型 ![]()
B.原子核内有10个中子的原子: ![]() C
C
C.Fe3+的最外层电子排布式为3s23p63d5
D.Cu基态的外围电子排布图: ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关晶体组成结构的叙述中,正确的是( ) 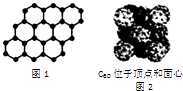
A.SiO2晶体中最小环上的原子数为6
B.在晶体中只要有阳离子就一定有阴离子
C.12g石墨烯(如图1)中含有六元环的个数为0.5NA
D.720g C60晶体(如图2)中含有0.5NA个晶胞结构单元
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在量热器中将50mL,0.50molL﹣1CH3COOH溶液与50mL、0.55molL﹣1NaOH溶液混合,温度从25.16℃升高到27.46℃.已知量热计的热容常数(量热计各部件每升高10C所需的热量)是150J0C﹣1 , C=4.18Jg﹣10C﹣1 , 溶液的密度为1gcm﹣3 . 
(1)试求CH3COOH的“中和热”.
(2)请你分析(1)中测得的实验值偏差可能是什么原因造成的? .
(3)若HNO3 (aq)+NaOH(aq)=NaNO3(aq)+H2O(l);△H=﹣57.3KJmol﹣1;
现有①稀H2SO4与Ba(OH)2(aq) ②浓H2SO4与Ba(OH)2(aq)
③HNO3与Ba(OH)2(aq)反应生成1molH2O(l) 的反应热分别为△H1、△H2、△H3 ,
则△H1、△H2、△H3三者由小到大的关系为: .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com