
 X、Y、Z、M、N、Q P为元素周期表前四周期的7种元素.其中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量最高的元素,M的内层电子数是最外层电子数的9倍,N的原子序数比M小1,Q在元素周期表的各元素中电负性最大.P元素的第三电子层处于全充满状态,第四电子层只有一个电子请回答下列问题:
X、Y、Z、M、N、Q P为元素周期表前四周期的7种元素.其中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量最高的元素,M的内层电子数是最外层电子数的9倍,N的原子序数比M小1,Q在元素周期表的各元素中电负性最大.P元素的第三电子层处于全充满状态,第四电子层只有一个电子请回答下列问题: ,P元素属于ds区元素.
,P元素属于ds区元素.分析 X、Y、Z、M、N、Q、P为元素周期表前四周期的7种元素,X原子核外的M层中只有两对成对电子,核外电子排布应为1s22s22p63s23p4,X为S元素;Y原子核外的L层电子数是K层的两倍,Y有2个电子层,最外层电子数为4,故Y为C元素;Z是地壳内含量最高的元素,为O元素;M的内层电子数是最外层电子数的9倍,M只能处于第四周期,最外层电子数只能为2,内层电子总数为18,核外电子总数为20,故M为Ca元素;N的原子序数比M小1,则N为K元素;Q在元素周期表的各元素中电负性最大,Q为F元素;P元素的第三电子层处于全充满状态,第四电子层只有一个电子,原子核外电子数=2+8+18+1=29,则P为Cu元素,据此解答.
解答 解:X、Y、Z、M、N、Q、P为元素周期表前四周期的7种元素,X原子核外的M层中只有两对成对电子,核外电子排布应为1s22s22p63s23p4,X为S元素;Y原子核外的L层电子数是K层的两倍,Y有2个电子层,最外层电子数为4,故Y为C元素;Z是地壳内含量最高的元素,为O元素;M的内层电子数是最外层电子数的9倍,M只能处于第四周期,最外层电子数只能为2,内层电子总数为18,核外电子总数为20,故M为Ca元素;N的原子序数比M小1,则N为K元素;Q在元素周期表的各元素中电负性最大,Q为F元素;P元素的第三电子层处于全充满状态,第四电子层只有一个电子,原子核外电子数=2+8+18+1=29,则P为Cu元素.
(1)X为S元素,处于周期表中第三周期ⅥA族,外围电子排布为3s23p4,它的外围电子的电子排布图为 ,P为Cu元素,价电子排布为3d104s1,属于ds区元素,
,P为Cu元素,价电子排布为3d104s1,属于ds区元素,
故答案为:第三周期ⅥA族; ;ds;
;ds;
(2)SO2分子中S原子价层电子对数=2+$\frac{6-2×2}{2}$=3,S原子含有1对孤电子对,故其立体结构是V形,
CO2分子C原子成2个σ键、没有孤电子对,C的杂化轨道类型为sp杂化,
SO2为极性分子,CO2为非极性分子,H2O为极性溶剂,极性分子易溶于极性溶剂,故SO2的溶解度较大,
故答案为:V形;sp杂化;SO2;SO2为极性分子,CO2为非极性分子,H2O为极性溶剂,极性分子易溶于极性溶剂,故SO2的溶解度较大;
(3)含有K元素的盐的焰色反应为紫色,许多金属盐都可以发生焰色反应,其原因是电子由较高能级跃迁到较低能级时,以光的形式释放能量,
故答案为:紫;电子由较高能级跃迁到较低能级时,以光的形式释放能量;
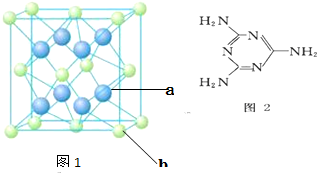
(4)元素Ca与元素F形成晶体化学式为CaF2,晶胞中绿色球数目=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4、蓝色球为8个,则绿色球为Ca,蓝色球为F,故该化合物的摩尔质量为D g/mol,晶胞质量=4×$\frac{D}{{N}_{A}}$g,晶胞边长为a pm,则晶胞体积=(a×10-10 cm)3=a3××10-30 cm3,则晶胞密度=$\frac{4×\frac{D}{{N}_{A}}g}{{a}^{3}×1{0}^{-30}c{m}^{3}}$=$\frac{4×1{0}^{30}×D}{{a}^{3}×{N}_{A}}$g/cm3,
故答案为:$\frac{4×1{0}^{30}×D}{{a}^{3}×{N}_{A}}$;
(5)三聚氰胺分子中处于环上的N原子成2个σ键,有1对孤电子对,采取sp2杂化,氨基中N原子成3个σ键,含有1对孤电子对,N原子采取sp3杂化,单键为σ键,双键含有1个σ键、1个π键,故1个三聚氰胺分子含有15个σ键,则1mol三聚氰胺分子中σ键的数目为15NA,
故答案为:sp2、sp3;15NA.
点评 本题是对物质结构的考查,涉及核外电子的排布、分子结构与性质、晶胞计算等,(4)中注意利用均摊法计算晶胞的质量,难度中等.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
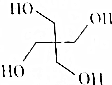 季戊四醇被大量用于涂料工业生产醇酸树脂、合成高级润滑剂、增塑剂、表面活性剂以及医药、炸药等,其结构简式如图所示.季戊四醇可由HCHO与CH3CHO两种有机物按一定比例加成得到的产物与H2再加成得到.则反应中HCHO与CH3CHO的物质的量之比为( )
季戊四醇被大量用于涂料工业生产醇酸树脂、合成高级润滑剂、增塑剂、表面活性剂以及医药、炸药等,其结构简式如图所示.季戊四醇可由HCHO与CH3CHO两种有机物按一定比例加成得到的产物与H2再加成得到.则反应中HCHO与CH3CHO的物质的量之比为( )| A. | 1:1 | B. | 1:2 | C. | 3:1 | D. | 3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | I A | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
| 1 | A | |||||||
| 2 | D | E | G | I | ||||
| 3 | B | C | F | H |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
 .
. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com