
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
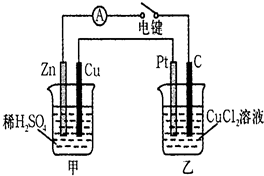 ((Ⅰ)某兴趣小组的同学用下图所示装置研究有关电化学的问题.当闭合该装置的电键时,观察到电流计的指针发生了偏转.请回答下列问题:
((Ⅰ)某兴趣小组的同学用下图所示装置研究有关电化学的问题.当闭合该装置的电键时,观察到电流计的指针发生了偏转.请回答下列问题:
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
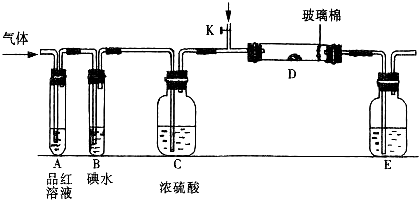
| ||
| △ |
| ||
| △ |
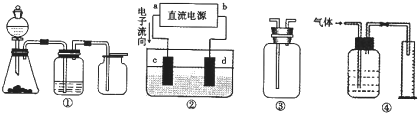
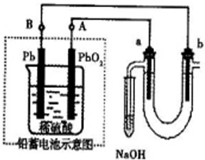
查看答案和解析>>
科目:高中化学 来源:2013-2014学年河北省遵化市高二上学期期中质量检测化学试卷(解析版) 题型:填空题
(Ⅰ)某兴趣小组的同学用下图所示装置研究有关电化学的问题。当闭合该装置的电键时,观察到电流计的指针发生了偏转。请回答下列问题:
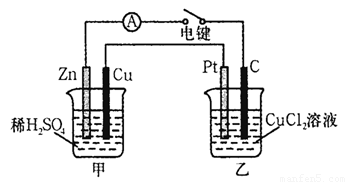
(1)甲装置的名称是____________ (填“原电池”或“电解池”)。
(2) 写出电极反应式: Pt极 ; 当甲中产生0.1 mol气体时,乙中析出铜的质量应为______________。
(3)若乙中溶液不变,将其电极都换成铜电极,电键闭合一段时间后,乙中溶液的颜色___________(填“变深”、“变浅”或“无变化”)。
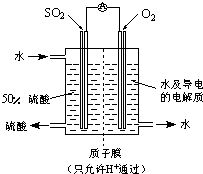
(Ⅱ)燃料电池是燃料(如CO、H2、CH4等)跟O2(或空气)反应,将化学能转化为电能的装置。对于以强碱为电解质的CH4燃料电池,负极电极反应式为: ,随着放电的进行,溶液的pH (填“变大”“变小”或“不变”)。
(Ⅲ)由Cu2+、Cl- 、Na+、SO42-四种离子中的两种离子组成的电解质溶液若干种,可选用铜电极、铂电极进行电解实验。
(1)要使电解过程中溶质的组成和质量不变,而该稀溶液的浓度增大,又无浑浊,应以_______为阳极电解 溶液,阳极电极反应式为 。
(2)以铂作阳极电解 溶液时,溶液的碱性有明显增强,且溶液保澄清,电解的总反应式为 。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年上海市闵行区高三下学期三模考试化学试卷(解析版) 题型:选择题
有关下图电化学装置的叙述中,正确的是
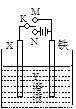
A.若X为碳棒,Y为饱和食盐水,K置于N,则铁极上析出氯气
B.若X为铂棒,Y为CuCl2溶液,K置于N,则铁棒质量将增加
C.若X为锌棒,Y为海水,K置于M,形成对铁的外加电流阴极保护
D.若X为铜棒,Y为稀硫酸,K置于M,则正极反应为:Fe−2e→Fe2+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com