
 ŌŚĢå»żĪŖ1LµÄŗćĪĀĆܱÕČŻĘ÷ÖŠ£¬³äČė1mol CO2ŗĶ3mol H2£¬Ņ»¶ØĢõ¼žĻĀ·¢Éś·“Ó¦£ŗCO2£Øg£©+3H2£Øg£©?CH3OH£Øg£©+H2O£Øg£©£¬²āµĆCO2ŗĶCH3OH£Øg£©µÄÅضČĖꏱ¼ä±ä»ÆČēĶ¼ĖłŹ¾£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
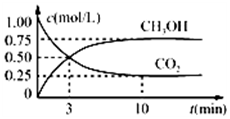
ŌŚĢå»żĪŖ1LµÄŗćĪĀĆܱÕČŻĘ÷ÖŠ£¬³äČė1mol CO2ŗĶ3mol H2£¬Ņ»¶ØĢõ¼žĻĀ·¢Éś·“Ó¦£ŗCO2£Øg£©+3H2£Øg£©?CH3OH£Øg£©+H2O£Øg£©£¬²āµĆCO2ŗĶCH3OH£Øg£©µÄÅضČĖꏱ¼ä±ä»ÆČēĶ¼ĖłŹ¾£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©| A£® | øĆ»Æѧ·“Ó¦ŌŚ3 minŹ±“ļµ½Ę½ŗāדĢ¬ | |
| B£® | ±£³ÖĘäĖūĢõ¼ž²»±ä£¬½µµĶĪĀ¶Č£¬Ę½ŗāŹ±c£ØCH3OH£©=0.85 mol•L-1£¬ŌņøĆ·“Ó¦·ÅČČ | |
| C£® | ČōĻąĶ¬ĪĀ¶ČĻĀ£¬ÉĻŹöČŻĘ÷ČŻ»żæɱ䣬±£³ÖČŻĘ÷ÄŚŃ¹Ēæ²»±ä£¬Ķ¬ŃłĻņČŻĘ÷ÖŠ³äČė1 molCO2”¢3mol H2£¬ŌņĘ½ŗāŹ±CO2µÄÅضČÓėĶ¼ÖŠĻąĶ¬ | |
| D£® | 12 minŹ±£¬ĻņÉĻŹöČŻĘ÷ÖŠŌŁ³äČė0.25 mol CO2”¢0.25 mol H2O£Øg£©£¬“ĖŹ±·“Ó¦½«ĻņÄę·“Ó¦·½Ļņ½ųŠŠ |
·ÖĪö A”¢Ę½ŗāŹ±ø÷×é·ÖÅØ¶Č²»ŌŁøı䣻
B”¢“ÓĶ¼æÉÖŖĘ½ŗāŹ±c£ØCH3OH£©=0.75 mol•L-1£¬½µµĶĪĀ¶Č£¬Ę½ŗāŹ±c£ØCH3OH£©=0.85 mol•L-1£¬ĖµĆ÷½µµĶĪĀ¶ČĘ½ŗāÕżĻņŅĘ¶Æ£»
C”¢ĻąĶ¬ĪĀ¶ČĻĀ£¬ÉĻŹöČŻĘ÷ČŻ»żæɱ䣬±£³ÖČŻĘ÷ÄŚŃ¹Ēæ²»±ä£¬Ķ¬ŃłĻņČŻĘ÷ÖŠ³äČė1 molCO2”¢3mol H2£¬Ļąµ±ÓŚ¼õŠ”ĮĖŃ¹Ē棬øł¾ŻŃ¹Ēæ¶ŌøĆ·“Ó¦µÄÓ°ĻģÅŠ¶Ļ£»
D”¢ŌŁ³äČė0.25molCO2”¢0.25molH2O£Øg£©£¬·“Ó¦ĪļÅضČŌö“ó£¬Ę½ŗāĻņ×ÅÕżĻņŅĘ¶Æ£®
½ā“š ½ā£ŗA”¢øł¾ŻĶ¼ĻóæÉÖŖ½ųŠŠµ½3·ÖÖÓŹ±£¬CO2ŗĶCH3OH£Øg£©µÄÅضČĻąĶ¬£¬µ«¼×“¼ŗĶ¶žŃõ»ÆĢ¼µÄÅضČČŌČ»·¢Éś±ä»Æ£¬ĖµĆ÷“ĖŹ±Ć»ÓŠ“ļµ½Ę½ŗāדĢ¬£¬¹ŹA“ķĪó£»
B”¢øł¾ŻĶ¼ĻóæÉÖŖ10·ÖÖÓŗó£¬CO2ŗĶCH3OH£Øg£©µÄÅØ¶Č²»ŌŁ±ä»Æ£¬“ļµ½»ÆŃ§Ę½ŗāדĢ¬£¬Ę½ŗāŹ±c£ØCH3OH£©=0.75 mol•L-1£¬½µµĶĪĀ¶Čŗóc£ØCH3OH£©=0.85 mol•L-1£¬ĖµĆ÷½µµĶĪĀ¶ČĘ½ŗāĻņ×ÅÕżĻņŅĘ¶Æ£¬ŌņøĆ·“Ó¦ĪŖ·ÅČČ·“Ó¦£¬øĆ·“Ó¦µÄ”÷H£¼0£¬¹ŹBÕżČ·£»
C”¢ĻąĶ¬ĪĀ¶ČĻĀ£¬ÉĻŹöČŻĘ÷ČŻ»żæɱ䣬±£³ÖČŻĘ÷ÄŚŃ¹Ēæ²»±ä£¬Ķ¬ŃłĻņČŻĘ÷ÖŠ³äČė1 molCO2”¢3mol H2£¬Ļąµ±ÓŚ¼õŠ”ĮĖŃ¹Ē棬øĆ·“Ó¦ĘųĢåĢå»ż¼õŠ”£¬¼õŠ”Ń¹Ēæ£¬Ę½ŗāĻņ×ÅÄęĻņŅĘ¶Æ£¬ŌņÖŲŠĀ“ļµ½Ę½ŗāŹ±CO2µÄÅضČŌö“󣬹ŹC“ķĪó£»
D”¢12minŹ±£¬ĻņÉĻŹöČŻĘ÷ÖŠŌŁ³äČė0.25molCO2”¢0.25molH2O£Øg£©£¬·“Ó¦ĪļÅضČŌö“ó£¬ŌņĘ½ŗāĻņ×ÅÕżĻņŅĘ¶Æ£¬¹ŹD“ķĪó£»
¹ŹŃ”£ŗB£®
µćĘĄ ±¾Ģāæ¼²é»ÆŃ§Ę½ŗāĶ¼Ļ󔢻ÆŃ§Ę½ŗāµÄ¼ĘĖć£¬ĢāÄæÄѶČÖŠµČ£¬“šĢāŹ±×¢Ņā¹Ū²ģĶ¼ÖŠµÄׯ×ų±źµÄŅāŅ壬Ć÷Č·»ÆŃ§Ę½ŗā¼°ĘäÓ°ĻģŅņĖŲĪŖ½ā“š¹Ų¼ü£¬ŹŌĢāÅąŃųĮĖѧɜµÄ·ÖĪö”¢Ąķ½āÄÜĮ¦¼°»Æѧ¼ĘĖćÄÜĮ¦£®


 ĒÉѧĒÉĮ·ĻµĮŠ“š°ø
ĒÉѧĒÉĮ·ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
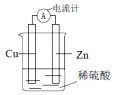
| A£® | øĆ×°ÖĆÖŠÄÜĮæ×Ŗ»Æ·½Ź½ĪŖµēÄÜ×Ŗ»ÆĪŖ»ÆѧÄÜ | |
| B£® | µē×Ó“ÓŠæʬĮ÷³ö£¬¾µ¼ĻßĮ÷ĻņĶʬ | |
| C£® | ¹¤×÷Ņ»¶ĪŹ±¼äÖ®ŗó£¬ČÜŅŗŃÕÉ«Öš½„±äĄ¶ | |
| D£® | Šæʬ·¢Éś»¹Ō·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ū¢Ü | B£® | ¢Ł¢Ś¢Ü | C£® | ¢Ł¢Ś¢Ū¢Ü | D£® | ¢Ł¢Ś¢Ū¢Ż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
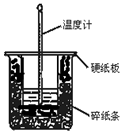 50mL 0.50mol•L-1ŃĪĖįÓė50mL 0.55mol•L-1NaOHČÜŅŗŌŚĶ¼Ź¾µÄ×°ÖĆÖŠ½ųŠŠÖŠŗĶ·“Ó¦£®Ķعż²ā¶Ø·“Ó¦¹ż³ĢÖŠĖł·Å³öµÄČČĮææɼĘĖćÖŠŗĶČČ£®»Ų“šĻĀĮŠĢā£ŗ
50mL 0.50mol•L-1ŃĪĖįÓė50mL 0.55mol•L-1NaOHČÜŅŗŌŚĶ¼Ź¾µÄ×°ÖĆÖŠ½ųŠŠÖŠŗĶ·“Ó¦£®Ķعż²ā¶Ø·“Ó¦¹ż³ĢÖŠĖł·Å³öµÄČČĮææɼĘĖćÖŠŗĶČČ£®»Ų“šĻĀĮŠĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 3øö | B£® | 4øö | C£® | 5øö | D£® | 6øö |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 “Óŗ£“ųÖŠĢįČ”µ„ÖŹµā¼°µāµÄ»ÆŗĻĪļ¼äµÄ×Ŗ»Æ¹ŲĻµČēĶ¼ĖłŹ¾£ŗ
“Óŗ£“ųÖŠĢįČ”µ„ÖŹµā¼°µāµÄ»ÆŗĻĪļ¼äµÄ×Ŗ»Æ¹ŲĻµČēĶ¼ĖłŹ¾£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
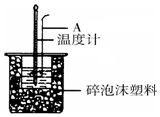 50mL 0.50mol/LŃĪĖįøś50mL 0.55mol/L NaOHČÜŅŗŌŚČēĶ¼ĖłŹ¾µÄ×°ÖĆÖŠ½ųŠŠÖŠŗĶ·“Ó¦£¬Ķعż²ā¶Ø·“Ó¦¹ż³ĢÖŠĖł·Å³öµÄČČĮææɼĘĖć·“Ó¦ČČ£®
50mL 0.50mol/LŃĪĖįøś50mL 0.55mol/L NaOHČÜŅŗŌŚČēĶ¼ĖłŹ¾µÄ×°ÖĆÖŠ½ųŠŠÖŠŗĶ·“Ó¦£¬Ķعż²ā¶Ø·“Ó¦¹ż³ĢÖŠĖł·Å³öµÄČČĮææɼĘĖć·“Ó¦ČČ£®²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com