
【题目】氯原子对O3分解有催化作用:
O3+Cl===ClO+O2 ΔH1
ClO+O===Cl+O2 ΔH2
大气臭氧层的分解反应是:O3+O===2O2 ΔH,该反应的能量变化如图:
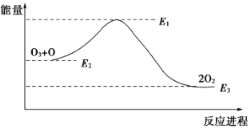
下列叙述中,正确的是
A. 反应O3+O===2O2的ΔH=E1-E3
B. O3+O===2O2是吸热反应
C. ΔH=ΔH1+ΔH2
D. ΔH=E3-E2>0
科目:高中化学 来源: 题型:
【题目】含有农药、染料、酚、氰化物,以及引起色度、臭味的废水,常用化学氧化法进行处理,所用的氧化剂有氯类(如液氯、次氯酸钙、次氯酸钠等)和氧类(如空气、臭氧、过氧化氢、高锰酸钾等)。一个典型实例是用氯氧化法处理含有剧毒的氰化物(含CN-)的废水。在碱性条件下(pH=8.5~11),氯气可将氰化物中CN-氧化为只有它毒性![]() 的氰酸盐(含CNO-)。
的氰酸盐(含CNO-)。
(1)写出含CN-废水用氯气氧化生成氰酸盐的离子方程式:_________________。
(2)若向含CNO-的废水中再通入氯气,可使CNO-转化为无毒的气体,写出这个反应的离子方程式:______________________________________________。
(3)在用液氯不便的地区,可用漂白粉处理含CN-的废水,若将其氧化为CNO-,其离子方程式为__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课题组利用CO2催化氢化制甲烷,研究发现HCOOH是CO2转化为CH4的中间体,即:![]() ,镍粉是反应I、II的催化剂。CH4、HCOOH、H2的产量和镍粉用量的关系如图所示(仅改变镍粉用量,其他条件不变):
,镍粉是反应I、II的催化剂。CH4、HCOOH、H2的产量和镍粉用量的关系如图所示(仅改变镍粉用量,其他条件不变):
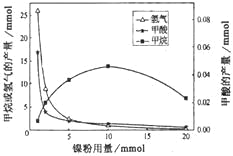
由图可知,当镍粉用量从1mmol增加到10mmol,反应速率的变化情况是( )
A.反应I的速率增加,反应II的速率不变
B.反应I的速率不变,反应II的速率增加。
C.反应I、II的速率均增加,且反应I的速率增加得快
D.反应I、II的速率均增加,且反应II的速率增加得快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求作答:
(1)有机物命名:
①![]() ______________________________(习惯命名法);
______________________________(习惯命名法);
②(CH3)2CHCH2CH(NH2)COOH_____________________________________(系统命名法)。
(2)书写化学方程式:
①ClCH2CH2COONH4与氢氧化钠的乙醇溶液共热_______________;
②对苯二甲酸(![]() )和乙二醇一定条件下的缩聚反应______________。
)和乙二醇一定条件下的缩聚反应______________。
(3)①某芳香烃的分子式为C8H10,它的一氯代物有二种,则其结构简式为_______;
②环己烷(C6H12)的属于环烷烃的同分异构体,其中含三元环(三角形)的有_______种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是铜锌原电池构造示意图,其电池反应式为 Zn(s) + CuSO4(aq) → ZnSO4(aq) + Cu(s), 下列判断不正确的是
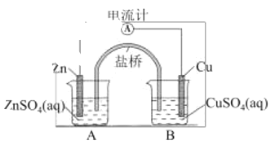
A.Zn 为负极B.盐桥中的阳离子移向B
C.移去盐桥,电流计指针不偏转D.铜棒质量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,除标出的元素外,表中的每个编号代表一种元素。请根据要求回答问题:

(1)②的元素符号是__________;该元素的最高价氧化物的电子式为__________;
(2)⑤和⑥两种元素的非金属性强弱关系是:⑤________⑥(填“>”或“<”);
(3)①和③两种元素组成的化合物中含有的化学键为__________(填“离子键”或“共价键”)
(4)④和⑥两种元素组成的化合物与AgNO3溶液反应的离子方程式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有 A、B、C、D、E、F、G 七种元素,试按如下所给的条件推断:
①A、B、C 是同一周期的金属元素,已知原子核外有3个电子层,A 的原子半径在所属周期中最大,且原子半径:A>B>C;
②D、E 是非金属元素,它们与氢化合可生成气态氢化物 HD 和 HE,室温下,D 的单质是液体,E 的单质是固体;
③F是地壳中含量最多的元素,G 是非金属性最强的元素
(1)C 离子的结构示意图为________________________ ;E 单质的颜色为_________。
(2)用电子式表示B、D 元素形成的化合物的形成过程:_____________________________ 。
(3)有 G、F 元素参加的置换反应的化学方程式为___________________________ 。
(4)用离子方程式证明D、E 元素的非金属性强弱,并用单线桥表示电子转移的方向和数目:________________________。
(5)用刺孔的 C单质(足量)包裹住2.3gA 单质放于水中,标准状况下,收集到气体的体积最多为_____L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钴、 铜及其化合物在工业上有重要用途, 回答下列问题:
(1) 请补充完基态Co的简化电子排布式: [Ar]_________, Co2+有_______个未成对电子。
(2) Na3[Co(NO2)6]常用作检验K+的试剂, 配位体NO2-的中心原子的杂化形式为________, 空间构型为_____。大π键可用符号![]() 表示, 其中m代表参与形成大π键的原子数, n为各原子的单电子数(形成σ键的电子除外)和得电子数的总和 (如苯分子中的大π键可表示为
表示, 其中m代表参与形成大π键的原子数, n为各原子的单电子数(形成σ键的电子除外)和得电子数的总和 (如苯分子中的大π键可表示为![]() ),则NO2-中大π键应表示为____________。
),则NO2-中大π键应表示为____________。
(3) 配合物[Cu(En)2]SO4的名称是硫酸二乙二胺合铜(Ⅱ), 是铜的一种重要化合物。其中 En 是乙二胺(H2NCH2CH2NH2)的简写。
①该配合物[Cu(En)2]SO4中N、 O、 Cu的第一电离能由小到大的顺序是______________。
②乙二胺和三甲胺[N(CH3)3]均属于胺, 且相对分子质量相近, 但乙二胺比三甲胺的沸点高得多, 原因是______________________________________________________。

(4) 金属Cu晶体中的原子堆积方式如图所示, 其配位数为______, 铜的原子半径为a nm, 阿伏加德罗常数的值为NA, Cu的密度为_________g/cm3(列出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高纯MnCO3是广泛用于电子行业的强磁性材料。MnCO3为白色粉末,不溶于水和乙醇,在潮湿环境下易被氧化,温度高于100℃开始分解。
Ⅰ.实验室以MnO2为原料制备MnCO3
(1)制备MnSO4溶液:
①主要反应装置如图,缓缓通入经N2稀释的SO2气体,发生反应H2SO3+MnO2![]() MnSO4+H2O。下列措施中,目的是加快化学反应速率的是________(填标号)。
MnSO4+H2O。下列措施中,目的是加快化学反应速率的是________(填标号)。
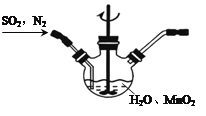
A.MnO2加入前先研磨 B.搅拌 C.提高混合气中N2比例
②已知实验室制取SO2的原理是Na2SO3+2H2SO4(浓)![]() 2NaHSO4+SO2↑+H2O。选择下图所示部分装置与上图装置相连制备MnSO4溶液,应选择的装置有________(填标号)。
2NaHSO4+SO2↑+H2O。选择下图所示部分装置与上图装置相连制备MnSO4溶液,应选择的装置有________(填标号)。
![]()
![]()
![]()
![]()
![]()
![]()
![]()
③若用空气代替N2进行实验,缺点是________。(酸性环境下Mn2+不易被氧化)
(2)制备MnCO3固体:
实验步骤:①向MnSO4溶液中边搅拌边加入饱和NH4HCO3溶液生成MnCO3沉淀,反应结束后过滤;② ……;③在70-80℃下烘干得到纯净干燥的MnCO3固体。
步骤②需要用到的试剂有________。
Ⅱ.设计实验方案
(3)利用沉淀转化的方法证明KSP(MnCO3) < KSP(NiCO3):________。
(已知NiCO3为难溶于水的浅绿色固体)
(4)证明H2SO4的第二步电离不完全:________。[查阅资料表明K2(H2SO4)=1.1×10-2]
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com