
��ҵ��+6�� ��Cr�������ܴ���0.5mg��L-1��Ϊ�˴ﵽ��ˮ�ŷű�����ҵ�ϴ�����![]()
������ҵ��ˮ�м���������NaCl��1��2g��L-1�����������缫���е�⣬����һ��ʱ�����Cr��![]() OH��3��Fe��OH��3�������ɣ��۹��˻��ճ�������ˮ�ﵽ�ŷű����Իش�
OH��3��Fe��OH��3�������ɣ��۹��˻��ճ�������ˮ�ﵽ�ŷű����Իش�
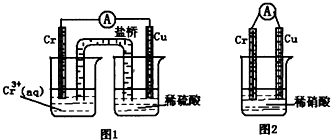
��1��д�����ʱ�ĵ缫��Ӧ������______����______��
![]()
��3����������Cr��OH��3��Fe��OH��3���������������ģ�______��
��4���ܷ缫��Ϊʯī�缫��Ϊʲô��______��
���𰸡���1������Fe-2e��Fe2+������2H++2e��H2����
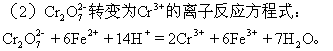
��3����H+�ŵ磬�ƻ���ˮ�ĵ���ƽ![]() �⣬������OH-����Һ�е�Fe3+��Cr3+����Cr��OH��3��Fe��OH��3������
�⣬������OH-����Һ�е�Fe3+��Cr3+����Cr��OH��3��Fe��OH��3������
��4�����ܣ�����ʯī�缫������Cl-�ŵ磬���ܲ�����ԭ��Fe2+��
![]()
�������� ������һ�����ʵ��Ӧ���⡣������������ӵķŵ�˳���ǣ������ӡ������ӡ������ӡ������ӡ��������ں����˷Ƕ��Խ����缫�ŵ�������Һ�������ӷŵ磬��˽�������ӦдΪ��2Cl--2e��Cl2������һ���������Ϊ����Ȼ�����缫�ŵ磬��缫��ӦΪ��Fe-3e��Fe3+�������˵缫���ǹ����ģ���������ĵ缫��ӦӦΪ��Fe-2e��Fe2+����Һ�е�������������������ŵ練ӦӦ�ǣ�2H++2e��H2�������ظ��������Ӧ�������������������ŵ硣
��Һ�д��ھ��������Ե��ظ�������Ӻ;��л�ԭ�Ե��������ӣ��ظ������������������������������ǿ�������ڸ������»�ԭ�ɸ��� �ӡ�
�缫��Ӧ��������ԭ��Ӧ�������������ӣ�ʹˮ��һ�����룬��Һ������������Ũ�ȴ��������Fe3+��Cr3+����Cr��OH��3��Fe��OH��3������
������ʯī�缫����Һ��û�л�ԭ�����ʣ��ظ�������Ӳ��ܱ���ԭ�����Ҳ���ų����ն��ﵽ���۾������á�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����

| NaOH |
| Cl2 |
| �ữ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
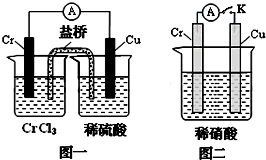 2011��6�£���������½������ʵҵ����˾5000��ֹ�ҵ���ϸ����Ƿ��㵹���µ���������Ⱦ��+6�۸��ױ��������գ����°���+3�۸����ױ��������գ�����С����ҵ������ˮ�Ĵ�������֮һ�ǽ���+6�۸��ķ�ˮ��������ڣ�����������������������NaCl����е�⣺���������ɵ�Fe2+��Cr2O72-������Ӧ�����ɵ�Fe3+��Cr3+����������OH-�������Fe��OH��3��Cr��OH��3������ȥ��
2011��6�£���������½������ʵҵ����˾5000��ֹ�ҵ���ϸ����Ƿ��㵹���µ���������Ⱦ��+6�۸��ױ��������գ����°���+3�۸����ױ��������գ�����С����ҵ������ˮ�Ĵ�������֮һ�ǽ���+6�۸��ķ�ˮ��������ڣ�����������������������NaCl����е�⣺���������ɵ�Fe2+��Cr2O72-������Ӧ�����ɵ�Fe3+��Cr3+����������OH-�������Fe��OH��3��Cr��OH��3������ȥ���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com