
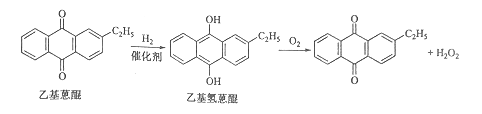
����Ŀ��[��ѧ-ѡ��2����ѧ�뼼��]˫��ˮ��һ����Ҫ����������Ư����������������˫��ˮ���������������䷴Ӧԭ��������������ͼ��ʾ��
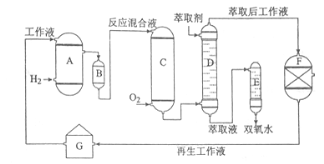
A���⻯��B��������C��������D����ȡ��E.������F.����Һ����װ��G.����Һ����װ��
���������У����һ����������л��ܼ����Ƴɹ���Һ����һ�����¶ȡ�ѹ���ʹ��������½����⻯���پ���������ȡ�������ȹ��յõ�˫��ˮ���ش��������⣺
��1���������Ʊ�˫��ˮ���������ĵ�ԭ����_______��ѭ��ʹ�õ�|ԭ����______�����ƹ���Һʱ�����л��ܼ���������ˮ��ԭ����______��
��2���⻯��A�з�Ӧ�Ļ�ѧ����ʽΪ_______������������C�ķ�Ӧ���Һ�е���Ҫ����Ϊ_______��
��3����ȡ��D�е���ȡ����____��ѡ��������ȡ����ԭ����______��
��4������Һ����װ��F��Ҫ����������H2O2��ԭ����______��
��5��˫��ˮŨ�ȿ���������������KMnO4��Һ�ⶨ���÷�Ӧ�����ӷ���ʽΪ_______��һ��˫��ˮ����������Ϊ27.5%�����ܶ�Ϊ1.10g��cm3������Ũ��Ϊ______mol/L��
���𰸡���1�������������һ������һ��������һ���������������ˮ���������л��ܼ�
��2��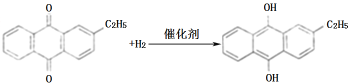 �һ�������
�һ�������
��3��ˮ H2O2����ˮ��ˮ��ȡ���һ�����������ˮ
��4��H2O2�ֽ�ų���������������ϣ�������ը
��5��6H++5H2O2+2MnO4-=2Mn2++5O2��+8H2O ��8.9
��������
�����������1�����ݷ�Ӧԭ����֪���������Ʊ�˫��ˮ���������ĵ�ԭ�����������������ɹ�������ͼ��֪��ѭ��ʹ�õ�ԭ�����һ��������һ����������л��������������ԭ�����һ��������һ���������������ˮ���������л��ܼ����������ƹ���Һʱ�����л��ܼ���������ˮ��
��2�����ݷ�Ӧԭ�����⻯��A�з�Ӧ�Ļ�ѧ����ʽΪ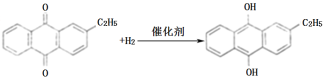 ������������C�ķ�Ӧ���Һ�е���Ҫ����Ϊ�һ���������
������������C�ķ�Ӧ���Һ�е���Ҫ����Ϊ�һ���������
��3����ȡ��D����Ҫ����˫��ˮ���һ�������H2O2����ˮ��ˮ��ȡ���һ�����������ˮ������ѡȡ����ȡ����ˮ��
��4��H2O2�ֽ�ų���������������ϣ�������ը���������Һ����װ��F��Ҫ����������H2O2��
��5��˫��ˮ��������������KMnO4����������ԭ��Ӧ��MnԪ�صĻ��ϼ���+7�۽��͵�+2�ۣ�OԪ�صĻ��ϼ���-1�����ߵ�0�ۣ����ݵ�ʧ�����غ㡢����غ��ԭ���غ���ƽ���÷�Ӧ�����ӷ���ʽΪ6H++5H2O2+2MnO4-=2Mn2++5O2��+8H2O��c=1000��1.10��27.5%��34=8.9mol/L��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л��߷��ӻ��������һ�ֳ��õĹ����߷��Ӳ��ϣ���ṹ��ʽΪ
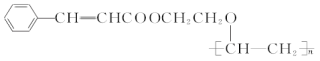 ������ͼ��ʾ��ϵ���Ժϳɼף������Լ�I�����Ҵ��������ڴ������������·�Ӧ�õ���
������ͼ��ʾ��ϵ���Ժϳɼף������Լ�I�����Ҵ��������ڴ������������·�Ӧ�õ���
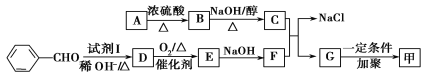
��֪��
a����CH2OH �� ��CH2OH![]() ��CH2OCH2�� �� H2O
��CH2OCH2�� �� H2O
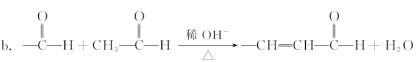
��ش��������⣺
��1������ͼ��ʾA����Է���������80.5��A��������Ԫ�ص���������Ϊ19.88%��̼Ԫ�ص���������Ϊ29.81%������Ϊ��Ԫ�غ���Ԫ�أ���A�ĺ˴Ź������������������շ壬�����֮��Ϊ2��2��1����A�Ľṹ��ʽΪ_______________________________________��
��2���Լ�I��������__________________��B��C�ķ�Ӧ������__________________��
��3��д�����з�Ӧ�Ļ�ѧ����ʽ��
��D��E___________________________________________________________________��
��C��F��G��NaCl_________________________________________________________��
��4��E��һ��ͬ���칹���ˮ����������֣�һ����ʹ��ˮ��ɫ����һ���ڵμӱ�����ˮ���а�ɫ�������ɣ������ʵĽṹ��ʽΪ______________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ԫ�ظ�(Cr)����Һ����Ҫ��Cr3+(����ɫ)��Cr(OH)4(��ɫ)��Cr2O72(�Ⱥ�ɫ)��CrO42(��ɫ)����ʽ���ڣ�Cr(OH)3Ϊ������ˮ�Ļ���ɫ���壬�ش��������⣺
��1��Cr3+��Al3+�Ļ�ѧ�������ơ���Cr2(SO4)3��Һ����μ���NaOH��Һֱ���������ɹ۲쵽��������_________��
��2��CrO42��Cr2O72����Һ�п��ת���������£���ʼŨ��Ϊ1.0 mol![]() L1��Na2CrO4��Һ��c(Cr2O72)��c(H+)�ı仯��ͼ��ʾ��
L1��Na2CrO4��Һ��c(Cr2O72)��c(H+)�ı仯��ͼ��ʾ��

�������ӷ���ʽ��ʾNa2CrO4��Һ�е�ת����Ӧ____________��
����ͼ��֪����Һ��������CrO42��ƽ��ת����__________(��������������С������������)������A�����ݣ��������ת����Ӧ��ƽ�ⳣ��Ϊ__________��
�������¶ȣ���Һ��CrO42��ƽ��ת���ʼ�С����÷�Ӧ����H______0(������������С��������������)��
��3���ڻ�ѧ�����в���K2CrO4Ϊָʾ������AgNO3����Һ�ζ���Һ��Cl������Ag+��CrO42����ש��ɫ������ָʾ����ζ��յ㡣����Һ��Clǡ��������ȫ(Ũ�ȵ���1.0��105 mol��L1)ʱ����Һ��c(Ag+)Ϊ_______ mol![]() L1����ʱ��Һ��c(CrO42)����__________ mol
L1����ʱ��Һ��c(CrO42)����__________ mol![]() L1��(��֪Ag2CrO4��AgCl��Ksp�ֱ�Ϊ2.0��1012��2.0��1010)��
L1��(��֪Ag2CrO4��AgCl��Ksp�ֱ�Ϊ2.0��1012��2.0��1010)��
��4��+6�۸��Ļ����ﶾ�Խϴ���NaHSO3����Һ�е�Cr2O72��ԭ��Cr3+������Ӧ�����ӷ���ʽΪ______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��H2C2O4Ϊ��Ԫ���ᡣ20��ʱ������һ��c��H2C2O4��+ c��HC2O4�C��+ c��C2O42�C��=0.100 mol��L�C1��H2C2O4��NaOH�����Һ����Һ�в����������ʵ���Ũ����pH�ı仯������ͼ��ʾ������ָ����Һ���������ʵ���Ũ�ȹ�ϵһ����ȷ����

A��pH=2.5����Һ�У�c��H2C2O4��+c��C2O42�C����c��HC2O4�C��
B��c��Na+��=0.100 mol��L�C1����Һ�У�c��H+��+c��H2C2O4��=c��OH�C��+c��C2O42�C��
C��c��HC2O4�C��=c��C2O42�C������Һ�У�c��Na+����0.100 mol��L�C1+c��HC2O4�C��
D��pH=7����Һ�У�c��Na+����2c��C2O42�C��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��п���仯������;�㷺������п����п����Ҫ�ɷ���ZnS��Ϊ��Ҫԭ���漰����Ҫ��Ӧ�У� 2ZnS(s) + 3O2(g) = 2ZnO(s) + 2SO2(g) ![]() H1=��930 kJ��mol��1
H1=��930 kJ��mol��1
2C(s) + O2(g) = 2CO(g) ![]() H2=��221 kJ��mol��1
H2=��221 kJ��mol��1
ZnO(s) + CO(g) = Zn(g) + CO2(g) ![]() H3= +198 kJ��mol��1
H3= +198 kJ��mol��1
��1����ӦZnS(s) + C(s) + 2O2(g) = Zn(g) + CO2(g) + SO2(g)��![]() H4= kJ��mol��1��
H4= kJ��mol��1��
��Ӧ�����ɵ�CO2��NH3��ϣ���һ�������·�Ӧ�ϳ����أ�
![]()
���÷�Ӧ��һ���¡������ܱ������ڽ��У��жϷ�Ӧ�ﵽƽ��״̬�ı�־�� ��
a��CO2��H2O(g)Ũ����� b�������������ѹǿ���ٸı�
c��2v(NH3)�� = v(H2O)�� d�������л��������ܶȲ��ٸı�
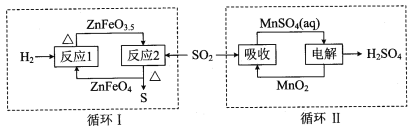
��2������п�ɹ㷺����ӡȾýȾ����ľ�ķ������� ZnSO4���ȷֽ�����и��������ʵ������¶ȱ仯��ϵ��ͼ��ʾ��
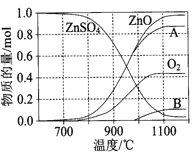
��д��700��~980��ʱ������Ӧ�Ļ�ѧ����ʽ�� ������B�Ļ�ѧʽ�� ��
������п�ֽ����ɵ�SO2����ͼ�е�����ѭ���ɷֱ�õ�S��H2SO4��д��ѭ��I�з�Ӧ2�Ļ�ѧ����ʽ�� ��ѭ��II�е�����������Ӧʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij������ȤС���H2O2�ķֽ�������������ʵ��̽����
��1���±��Ǹ�С���о�Ӱ��������� (H2O2)�ֽ����ʵ�����ʱ�ɼ���һ�����ݣ�
��10mL H2O2��ȡ150mLO2�����ʱ��(��)
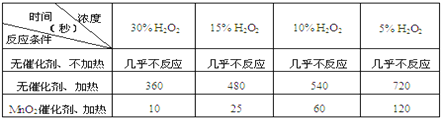
�����о�С������Ʒ���ʱ��������Ũ�ȡ� �� �����ضԹ�������ֽ����ʵ�Ӱ��
��������Ӱ���������ֽ����ʵ���������ѡһ����˵�������ضԷֽ������к�Ӱ�죿 ��
��2����������ͬ���ۼ�״̬��ͬ��MnO2�ֱ���뵽5mL 5%��˫��ˮ�У����ô����ǵ�ľ�����ԡ��ⶨ������£�

��д��H2O2������Ӧ�Ļ�ѧ��Ӧ����ʽ ��
��.ʵ����˵���������õĴ�С�� �йء�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ����һ���������¿���ת��Ϊ���ܡ�
(һ)��������������Ӧ��
�� 2FeBr2 + 3Cl2 = 2FeCl3+2Br2 �� Na2CO3 + 2HCl = 2NaCl + H2O + CO2��
��1������������Ӧ�ı����жϣ�����Ϊ������Ƴ�ԭ��ص��� (�Ӧ���)�������� ��
(��)�����Fe + CuSO4 = FeSO4 + Cu��Ӧ��ѡ�����˵IJ��Ϻ��Լ����һ��ԭ���
��2������ԭ���װ��ͼ������ͼ�б�ע���缫�͵������Һ�����ơ�
��3��д����ԭ��ص缫��Ӧʽ�������� �������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������ˮ�������ᣬ���������Լ���ҽ�÷���������������������һ���Ʊ��������Ƶ�ʵ�鷽�����ش��������⣺
��һ��̼��Ƶ��Ʊ�
��1�����������백ˮ��Ŀ����_______��С����е�������ʹ������������������____��
��2����ͼ��ijѧ���Ĺ��˲���ʾ��ͼ����������淶����______�����ţ���
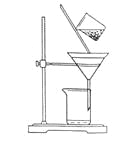
a��©��ĩ�˾���δ�����ձ���
b����������������
c������ֽʪ��ʹ�����©����
d����ֽ��Ե�߳�©��
e���ò�������©������������Լӿ�����ٶ�
(��)�������Ƶ��Ʊ�

��3���������ľ������Ϊ��μ���ϡ���ᣬ����Һ���д����������壬��ʱ��Һ��____�ԣ���������������������������������Һ��У����ȹ��ˡ�����Һ��е�������___________��
��4���������з�Ӧ�Ļ�ѧ����ʽΪ________���÷�Ӧ��Ҫ�ڱ�ԡ�½��У�ԭ����_________��
��5�������˵õ��İ�ɫ�ᾧ����ʹ������ˮ���Ҵ�ϴ�ӣ�ʹ���Ҵ�ϴ�ӵ�Ŀ����_______��
��6���Ʊ��������Ƶ���һ�ַ����ǣ���ʯ��ʯ���պ�ֱ�Ӽ���˫��ˮ��Ӧ�����˺�ɵõ��������Ʋ�Ʒ���ù��շ������ŵ���______����Ʒ��ȱ����_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��[ʵ�黯ѧ]
���������ƣ�Na2S2O5���dz��õĿ����������ڿ�����������ʱ���ֽ⡣ʵ�����Ʊ�����Na2S2O5�ķ������ڲ��Ͻ����£����Ʒ�Ӧ�¶���40�����ң���Na2CO3��������Һ��ͨ��SO2��ʵ��װ������ͼ��ʾ��
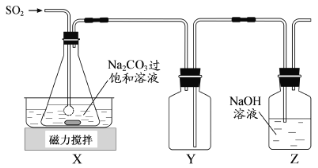
����ҺpHԼΪ4ʱ��ֹͣ��Ӧ����20���������ýᾧ������Na2S2O5�Ļ�ѧ����ʽΪ
2NaHSO3===Na2S2O5+H2O
��1��SO2��Na2CO3��Һ��Ӧ����NaHSO3��CO2�������ӷ���ʽΪ____________________��
��2��װ��Y��������______________________________��
��3����������ķ�ӦҺ����ѹ������ϴ����25����30�����ɻ��Na2S2O5���塣
����ɼ�ѹ����װ�õ���Ҫ�����Dz���©����________________�ͳ����á�
�������ñ���SO2ˮ��Һ����ˮ�Ҵ�ϴ��Na2S2O5�������ñ���SO2ˮ��Һϴ�ӵ�Ŀ����______��
��4��ʵ���Ƶõ�Na2S2O5�����к���һ������Na2SO3��Na2SO4������ܵ�ԭ����______��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com