
下列图示中正确的实验操作是
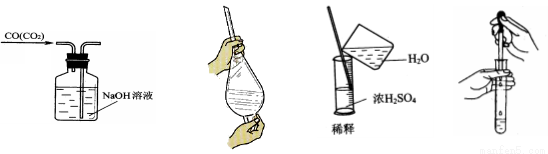
A.除去CO的CO2 B.萃取时振荡混合液
C.稀释浓硫酸 D.向试管中滴加液体
 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案科目:高中化学 来源:2014-2015学年贵州省高二上学期半期考试化学试卷(解析版) 题型:实验题
(14分)I.如下图所示,50mL0.50mol·L-1盐酸与50mL0.55mol·L-1NaOH溶液在装置中进行中
和反应。通过测定反应过程中所放出的热量,可计算中和热,回答下列问题:

(1)图中装置缺少的仪器是 。
(2)下列说法不正确的是 (填序号)。
A.若用50mL0.55mol·L-1Ba(OH)2溶液代替NaOH溶液进行实验,测得的中和热相同
B.若用50mL0.50mol·L-1醋酸溶液代替盐酸进行实验,测得的中和热相同
C.若分别用等浓度的硫酸和Ba(OH)2溶液代替盐酸和NaOH溶液进行实验,测得的中和热相同
D.NaOH溶液稍过量的原因是让盐酸完全反应
II.某学生用0.1mol/L KOH溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:
A.移取20.00mL待测的盐酸溶液注入洁净的锥形瓶,并加入2-3滴酚酞
B.用标准溶液润洗滴定管2-3次
C.把盛有标准溶液的碱式滴定管固定好,调节液面使滴定管尖嘴充满溶液
D.取标准KOH溶液注入碱式滴定管至0刻度以上2-3cm
E.调节液面至0或0刻度以下,记下读数
F.把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点,记下滴定管液面的刻度
完成以下填空:
(1)正确操作的顺序是(用序号字母填写)______________________.
(2)实验中眼睛注视_______________,直至滴定终点。判断到达终点的现象是__________________。
(3)若三次实验所用KOH溶液体积分别为14.98 mL,16.80 mL,15.02 mL则c(HCl)= 。
(4)下列操作中,可能造成测定结果偏高的是 。
A.未用标准液润洗碱式滴定管
B.滴定终点读数时,俯视滴定管中液面刻度,其它操作均正确
C.盛装待测液的锥形瓶用蒸馏水洗过,未用待测液润洗
D.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省四地六校高一上学期第一次月考化学试卷(解析版) 题型:选择题
下列各组物质中,前者为混合物,后者为单质的是
A.Na2CO3·10H2O 、 Na2CO3 B.盐酸 、 液氮
C.石油 、 冰 D.碘酒 、 干冰
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省厦门市高一上学期期中考试化学试卷(解析版) 题型:填空题
(6分)根据题目要求书写化学用语
(1)写出符合SO42—+ Ba2+= BaSO4↓的化学方程式
(2)写出实验室制二氧化碳的离子方程式
(3)氯水滴入硝酸银溶液的化学方程式
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省厦门市高一上学期期中考试化学试卷(解析版) 题型:选择题
已知常温下在溶液中可发生如下两个离子反应:Ce4++ Fe2+=Fe3++ Ce3+
Sn2++ 2Fe3+=2Fe2++ Sn4+,由此可以确定Fe2+、Ce3+、Sn2+三种离子的还原性由强到弱的顺序是
A. Sn2+、Fe2+、Ce3+ B. Sn2+、Ce3+、Fe2+
C. Ce3+、Fe2+、Sn2+ D. Fe2+、Sn2+、Ce3+
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省厦门市高一上学期期中考试化学试卷(解析版) 题型:选择题
四种基本反应类型中,一定是氧化还原反应的是
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省高一9月月考化学试卷(解析版) 题型:选择题
在标准状况下,1体积水溶解700体积氨气,所得溶液密度为0.9g/cm3,这种氨水的物质的量浓度和溶质的质量分数分别为
A.18.4mol·L-1 34.7% B.20.4mol·L-1 38.5%
C.18.4mol·L-1 38.5% D.20.4mol·L-1 34.7%
查看答案和解析>>
科目:高中化学 来源:2014-2015学年陕西省宝鸡市岐山县高一上学期期中质量检测化学试卷(解析版) 题型:实验题
(12分)下图是实验室常用的实验仪器及实验装置图,请据图回答:

(1)写出上图中序号①~④仪器的名称:② ; ③ ;④ ;
(2)仪器①~④中,使用时必须检查是否漏水的有 ;(填仪器序号)
(3)若向II装置中加入碘水和少量CCl4,振荡后静置,会观察到什么现象? ;静置后,再将液体分离的操作是_______________________________;
(4)装置I中冷凝水由 (填a或b)口通入,温度计水银球的位置是 ;
(5)选择下列实验方法分离物质,将分离方法的序号填在横线上。
A.萃取分液法 B.加热分解 C.结晶法 D.分液法 E.渗析法 F.蒸馏法 G.过滤法
①___________分离饱和食盐水和沙子的混合物;
②___________从硝酸钾和氯化钠的混合溶液中获得硝酸钾;
③___________分离水和煤油的混合物;
④___________分离水和酒精。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年辽宁省高二上学期10月月考化学试卷(解析版) 题型:实验题
某酸性工业废水中含有K2Cr2O7。光照下,草酸能将其中的Cr2O72-转化为Cr3+。某课题组研究发现,少量铁明矾[Al2Fe(SO4)4·24H2O]即可对该反应起催化作用。为进一步研究有关因素对该反应速率的影响,探究如下:
(1)在25°C下,控制光照强度、废水样品初始浓度和催化剂用量相同,调节不同的初始pH和一定浓度草酸溶液用量,作对比实验,完成以下实验设计表(表中不要留空格)。
实验编号 | 初始pH | 废水样品体积/mL | 草酸溶液体积/mL | 蒸馏水体积/mL |
① | 4 | 60 | 10 | 30 |
② | 5 | 60 | 10 | 30 |
③ | 5 | 60 |
|
|
测得实验①和②溶液中的Cr2O72-浓度随时间变化关系如图所示。

(2)上述反应后草酸被氧化为 (填化学式)。
(3)实验①和②的结果表明 ;
实验①中0~t1时间段反应速率 (Cr3+)= mol/(L·min) (用代数式表示)。
(Cr3+)= mol/(L·min) (用代数式表示)。
(4)该课题组队铁明矾[Al2Fe(SO4)4·24H2O]中起催化作用的成分提出如下假设,请你完成假设二和假设三:
假设一:Fe2+起催化作用;
假设二: ;
假设三: ;
…………
(5)请你设计实验验证上述假设一,完成下表中内容。(除了上述实验提供的试剂外,可供选择的药品有K2SO4、FeSO4、K2SO4·Al2(SO4)3·2H2O、Al2(SO4)3等。溶液中Cr2O72-的浓度可用仪器测定)
实验方案(不要求写具体操作过程) | 预期实验结果和结论 |
|
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com