
| A、0.1mol?L-1的氢氟酸溶液加水稀释,平衡正向移动,溶液中各离子浓度均减小 |
| B、pH=2的盐酸酸化的FeCl3溶液,稀释10倍后,溶液pH=3 |
| C、在NaHSO4溶液中,c(H+)=c(OH-)+c(SO42-) |
| D、在25℃时,任何水溶液中KW=1×10-14 |


 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案科目:高中化学 来源: 题型:
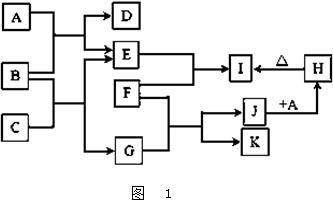 字母A~K各表示一种物质,其转化关系如下图所示,有的反应部分产物已略去.其中E、F、K为单质,其他均为化合物;A、E、K为无色气体,B为淡黄色固体,C为无色液体;F为常见的金属,高温下与某些金属氧化物反应是工业上冶炼金属的方法之一.试回答下列问题:
字母A~K各表示一种物质,其转化关系如下图所示,有的反应部分产物已略去.其中E、F、K为单质,其他均为化合物;A、E、K为无色气体,B为淡黄色固体,C为无色液体;F为常见的金属,高温下与某些金属氧化物反应是工业上冶炼金属的方法之一.试回答下列问题:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
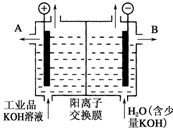 氢氧化钾是重要的工业产品.请回答:
氢氧化钾是重要的工业产品.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数 | Ki=1.7×10-4 | Ki=4.9×10-10 | Ki1=4.3×10-7 Ki2=5.6×10-11 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、500mL溶液中含SO42-、Fe3+总数为NA |
| B、500mL溶液中含0.6NA个SO42- |
| C、1L溶液中含有0.2NA个Fe3+ |
| D、500mL该溶液中SO42-物质的量浓度为0.6mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②④⑥⑧ |
| B、①②⑤⑥⑦ |
| C、②③④⑥⑧ |
| D、③④⑤⑦⑧ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com