
| A、用过滤法 | B、用蒸馏法 |
| C、用萃取法 | D、用分液法 |
科目:高中化学 来源: 题型:

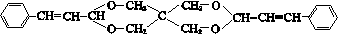
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、可逆反应不可以自发进行 |
| B、催化剂可以加块反应速率,也可增大反应物的转化率 |
| C、当有多个反应参加时,使用催化剂,可增加目标产物的产率 |
| D、H2与O2点燃生成H2O,H2O电解产生H2与O2,说明该反应可逆 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、液溴易挥发,在存放液溴的试剂瓶中应加水封 |
| B、单质硅是将太阳能转变为电能的常用材料 |
| C、能使润湿的淀粉KI试纸变成蓝色的物质一定是Cl2 |
| D、某溶液中加入足量稀盐酸无明显现象,再加入BaCl2溶液产生白色沉淀,该溶液中一定含有SO42-离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、最终得到沉淀的质量大于
| ||
B、该饱和溶液质量百分比浓度为:
| ||
| C、最终所得溶液PH不变 | ||
D、该饱和溶液中溶质物质的量浓度为:
|
查看答案和解析>>
科目:高中化学 来源: 题型:
 用一定浓度的稀盐酸与稀NaOH溶液在如图1所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热.已知强酸与强碱的中和热为57.3KJ/mol,水的比热容为4.2J/(g?℃),有关热量与比热容的计算公式:Q=m×c×△t(Q为热量,m为物质的质量,c为比热容,△t物质温度的变化值)
用一定浓度的稀盐酸与稀NaOH溶液在如图1所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热.已知强酸与强碱的中和热为57.3KJ/mol,水的比热容为4.2J/(g?℃),有关热量与比热容的计算公式:Q=m×c×△t(Q为热量,m为物质的质量,c为比热容,△t物质温度的变化值)查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol CH2=CH2可以与Br2发生加成反应,消耗1 mol Br2 |
| B、苯的邻位二元取代物只有一种,可以说明苯分子不具有碳碳单键和碳碳双键的交替结构 |
| C、甲苯中所有原子都在同一平面内 |
D、苯乙烯( -CH=CH2)与立方烷( -CH=CH2)与立方烷( )互为同分异构体 )互为同分异构体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com