
| A、RCl>RI>R2CrO4 |
| B、RCl>R2CrO4>RI |
| C、R2CrO4>RCl>RI |
| D、R2CrO4>RI>RCl |
| Ksp(RCl) |
| 1.8 |
| Ksp(RI) |
| 1.5 |
| 3 | 4.0×10-12 |
| 3 | 4 |


科目:高中化学 来源: 题型:
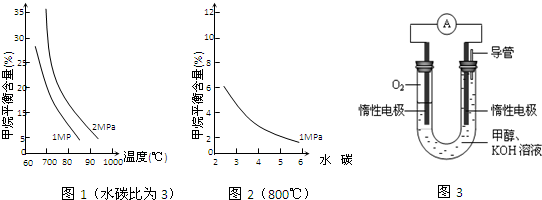
| n(H2O) |
| n(CH4) |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、实验Ⅰ:配置一定物质的量浓度的溶液 |
| B、实验Ⅱ:除去Cl2中的HCl |
| C、实验Ⅲ:用水吸收NH3 |
| D、实验Ⅳ:石油的分馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 与 与 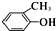 属于同素异形体 属于同素异形体 |
| B、CH3COOH与硬脂酸(C17H35COOH)属于同系物 |
C、 与 与  属于同一种物质 属于同一种物质 |
D、 与 与 属于同分异构体 属于同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH3-CH2-NO2和N2H-CH2-COOH互为同分异构体 |
| B、O2和O3互为同素异形体 |
| C、CH3CH3和CH3CH3CH互为同系物 |
| D、干冰和冰为同一种物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、光化学烟雾是氮氧化物受紫外线照射后产生的O3直接与空气中的一些碳氢化合物作用后生成的一种有毒烟雾 |
| B、石油液化气、汽油和石蜡的主要成分都是碳氢化合物 |
| C、绿色化学的核心是应用化学原理对环境污染进行治理 |
| D、“天宫一号”中使用的碳纤维,是一种新型无机非金属材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、已知a g乙烯气体充分燃烧时生成1 mol CO2和液态水,放出b kJ的热量,则表示乙烯燃烧热的热化学方程式为2C2H4(g)+6O2(g)═4CO2(g)+4H2O(l)△H=-4b kJ?mol-1 |
| B、已知:H2(g)+F2(g)═2HF(g)△H=-270 kJ?mol-1,则1 mol氢气与1 mol氟气反应生成2 mol液态氟化氢放出的热量数值小于270 kJ |
| C、常温常压下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为N2(g)+3H2(g)?2NH3(g)△H=-38.6 kJ?mol-1 |
| D、已知:①C(s,石墨)+O2(g)═CO2(g)△H=-393.5 kJ?mol-1,②C(s,金刚石)+O2(g)═CO2(g)△H=-395.0 kJ?mol-1,则C(s,金刚石)═C(s,石墨)△H=-1.5 kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Mg2++2OH-→Mg(OH)2↓ |
| B、Mg2++2HCO3-+Ca2++2OH-→MgCO3↓+CaCO3↓+2H2O |
| C、Mg2++HCO3-+Ca2++3OH-→Mg(OH)2↓+CaCO3↓+H2O |
| D、Mg2++4HCO3-+2Ca2++4OH-→2MgCO3↓+2CaCO3↓+4H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com