
| m |
| M |
| 1000ρω |
| M |
| m |
| M |
| 1000×1.84×98% |
| 98 |
| 1000mL×1mol/L |
| 18.4mol/L |


 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案科目:高中化学 来源: 题型:
| A、负极发生的反应为:Fe-3e-=Fe3+ |
| B、正极发生的反应为:2H2O+O2+4e-=4OH? |
| C、原电池是将电能转变为化学能的装置 |
| D、钢铁在水下部分比在空气与水交界处更容易腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 3 |
| 2 |

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、垃圾处理常用的方法是卫生填埋、堆肥和焚烧 |
| B、将垃圾分类并回收是处理的发展方向 |
| C、填埋垃圾不需要治理,只需深埋即可 |
| D、垃圾是污染物,不会产生二次污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:
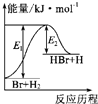
| A、该反应的△H=+(E1-E2)kJ?mol-1 |
| B、加入催化剂,该化学反应的反应热变大 |
| C、反应物的总能量高于生成物的总能量 |
| D、该反应为放热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、15g甲基(-CH3)所含有的电子数是10NA | ||
| B、0.5mol 1,3一丁二烯分子中含有的碳碳双键数为NA | ||
C、标准状况下,1 L戊烷充分燃烧后生成的气态产物的分子数为
| ||
| D、60gSiO2晶体中,含有NA个Si-O键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com