
右图表示金属X、Y以及它们的合金Z分别与足量盐酸反应时产生氢气的情况,其中横坐标表示消耗金属的物质的量,纵坐标表示产物氢气的体积(标准状况)。下列对有关Z的组成的判断,正确的是
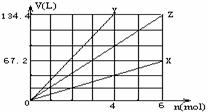
A.n(Na):n(Fe)=2:1 B.n(Mg):n(K)=1:2 C.n(Na):n(Al)=1:3 D.n(K):n(Al)=1:1
科目:高中化学 来源: 题型:阅读理解
| ||
| ||
| ||
| ||
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
(10分)W、X、Y、Z四种短周期元素在元素周期表中的位置如右图所示,其中Z位于ⅦA族。请回答下列问题。
(1)W的原子结构示意图为 。能说明Z的非金属性比X的非金属性强的事实是 (举一例)。
(2)W、Y和氢3种元素所形成的一种化合物,其75%(体积分数)的溶液常用于医疗消毒,该化合物的结构简式为 。用化学方程式表示该化合物在中学实验室的一种用途 。
(3)电解NaZ水溶液时,阴极的电极反应式为 。工业上,以上述反应的阳极产物和Ca(OH)2为原料,制备漂白粉反应的化学方程式为 。
(4)已知:298K时,金属钠与Y2气体反应,生成1 mol Na2Y固体时,放出热量414 kJ;生成1 mol Na2Y2固体时,放出热量511kJ。由Na2Y固体与Y2气体反应生成Na2Y2固体的热化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
(10分)W、X、Y、Z四种短周期元素在元素周期表中的位置如右图所示,其中Z位于ⅦA族。
请回答下列问题。
(1)W的原子结构示意图为 。能说明Z的非金属性比X的非金属性强的事实是 (举一例)。
(2)W、Y和氢3种元素所形成的一种化合物,其75%(体积分数)的溶液常用于医疗消毒,该化合物的结构简式为 。用化学方程式表示该化合物在中学实验室的一种用途 。
(3)电解NaZ水溶液时,阴极的电极反应式为 。工业上,以上述反应的阳极产物和Ca(OH)2为原料,制备漂白粉反应的化学方程式为 。
(4)已知:298K时,金属钠与Y2气体反应,生成1 mol Na2Y固体时,放出热量414 kJ;生成1 mol Na2Y2固体时,放出热量511kJ。由Na2Y固体与Y2气体反应生成Na2Y2固体的热化学方程式为 。
查看答案和解析>>
科目:高中化学 来源:福建省厦门双十中学2011届高三第一次月考化学试题 题型:填空题
(10分)W、X、Y、Z四种短周期元素在元素周期表中的位置如右图所示,其中Z位于ⅦA族。请回答下列问题。
(1)W的原子结构示意图为 。能说明Z的非金属性比X的非金属性强的事实是 (举一例)。
(2)W、Y和氢3种元素所形成的一种化合物,其75%(体积分数)的溶液常用于医疗消毒,该化合物的结构简式为 。用化学方程式表示该化合物在中学实验室的一种用途 。
(3)电解NaZ水溶液时,阴极的电极反应式为 。工业上,以上述反应的阳极产物和Ca(OH)2为原料,制备漂白粉反应的化学方程式为 。
(4)已知:298K时,金属钠与Y2气体反应,生成1 mol Na2Y固体时,放出热量414 kJ;生成1 mol Na2Y2固体时,放出热量511 kJ。由Na2Y固体与Y2气体反应生成Na2Y2固体的热化学方程式为 。
查看答案和解析>>
科目:高中化学 来源:福建省2010-2011学年高三第一次月考化学试题 题型:填空题
(10分)W、X、Y、Z四种短周期元素在元素周期表中的位置如右图所示,其中Z位于ⅦA族。请回答下列问题。
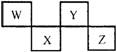
(1)W的原子结构示意图为 。能说明Z的非金属性比X的非金属性强的事实是 (举一例)。
(2)W、Y和氢3种元素所形成的一种化合物,其75%(体积分数)的溶液常用于医疗消毒,该化合物的结构简式为 。用化学方程式表示该化合物在中学实验室的一种用途 。
(3)电解NaZ水溶液时,阴极的电极反应式为 。工业上,以上述反应的阳极产物和Ca(OH)2为原料,制备漂白粉反应的化学方程式为 。
(4)已知:298K时,金属钠与Y2气体反应,生成1 mol Na2Y固体时,放出热量414 kJ;生成1 mol Na2Y2固体时,放出热量511 kJ。由Na2Y固体与Y2气体反应生成Na2Y2固体的热化学方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com