

 ��Ϊģ��������Ӧ��ȷ��ȡ0. 508g�⡢0.736g����������50. 0mL���ܱ������У�����ʹ�䷴Ӧ����ͼ�� WI2(g)�����ʵ�����ʱ��仯��ϵͼ����������I��0��t2ʱ��Σ��ķ�Ӧ�¶�ΪT1������II(��t2��ʼ)�ķ�Ӧ�¶�ΪT2����T2>T1����
��Ϊģ��������Ӧ��ȷ��ȡ0. 508g�⡢0.736g����������50. 0mL���ܱ������У�����ʹ�䷴Ӧ����ͼ�� WI2(g)�����ʵ�����ʱ��仯��ϵͼ����������I��0��t2ʱ��Σ��ķ�Ӧ�¶�ΪT1������II(��t2��ʼ)�ķ�Ӧ�¶�ΪT2����T2>T1����


 ]��
]�� 2OH-+Cl2��+H2��
2OH-+Cl2��+H2�� 2HCl+O2����ClO-+Cl-+2H+= Cl2��+H2O��
2HCl+O2����ClO-+Cl-+2H+= Cl2��+H2O�� H++OH-��HClO
H++OH-��HClO H++ClO-����ȷ��B. ����ˮ��ͨ��SO2��������Ӧ��Cl2��SO2��2H2O=H2SO4��2HCl��������H2SO4��HCl��û��Ư���ԡ����Ư�����ü�����C������ˮ��ͨ��������ƽ�⣺Cl2+H2O
H++ClO-����ȷ��B. ����ˮ��ͨ��SO2��������Ӧ��Cl2��SO2��2H2O=H2SO4��2HCl��������H2SO4��HCl��û��Ư���ԡ����Ư�����ü�����C������ˮ��ͨ��������ƽ�⣺Cl2+H2O  H++Cl-+HClO�����ƶ���c(H+) ����HClO
H++Cl-+HClO�����ƶ���c(H+) ����HClO H++ClO-�����ƶ���c(ClO-) ��С��c( H��)/c(ClO��)������D����ˮϡ����ˮ����Һ�е�H+��ClO-��Cl-����Ũ�ȼ�С��������c(H+)��c(OH-)=Kw.����c(OH-)������E����ˮϡ����ˮ������Cl2+H2O
H++ClO-�����ƶ���c(ClO-) ��С��c( H��)/c(ClO��)������D����ˮϡ����ˮ����Һ�е�H+��ClO-��Cl-����Ũ�ȼ�С��������c(H+)��c(OH-)=Kw.����c(OH-)������E����ˮϡ����ˮ������Cl2+H2O  H++Cl-+HClO�����ƶ�������������c(H+) ��С����ˮ���������ü���������ˮ�ĵ���ƽ��������Ӧ�����ƶ�����ȷ��F������ˮ�м���������NaOH��������ӦCl2+NaOH= NaCl+NaClO����ǡ����ȫ��Ӧ����c(Na��)=c(Cl�� )+c(ClO��)����ȷ��������ȷѡ��ΪA��E��F����2���ȼҵ�����������䷴Ӧ�����ӷ���ʽΪ2Cl-+2H2O
H++Cl-+HClO�����ƶ�������������c(H+) ��С����ˮ���������ü���������ˮ�ĵ���ƽ��������Ӧ�����ƶ�����ȷ��F������ˮ�м���������NaOH��������ӦCl2+NaOH= NaCl+NaClO����ǡ����ȫ��Ӧ����c(Na��)=c(Cl�� )+c(ClO��)����ȷ��������ȷѡ��ΪA��E��F����2���ȼҵ�����������䷴Ӧ�����ӷ���ʽΪ2Cl-+2H2O 2OH-+ Cl2��+H2��.��3���ɵ���ƽ�ⳣ��H2CO3>HClO>HCO3-����֪��H2CO3>HClO�����84����Һ¶���ڿ����з�����Ӧ���йػ�ѧ����ʽNaClO+CO2+ H2O=HClO+NaHCO3��2HClO
2OH-+ Cl2��+H2��.��3���ɵ���ƽ�ⳣ��H2CO3>HClO>HCO3-����֪��H2CO3>HClO�����84����Һ¶���ڿ����з�����Ӧ���йػ�ѧ����ʽNaClO+CO2+ H2O=HClO+NaHCO3��2HClO 2HCl+O2������84����Һ����������Ũ���ᣩ���ʹ�ÿ��ܻᷢ����Ӧ��ClO-+Cl-+2H+= Cl2��+H2O�����ж�������Cl2�����ж�����4������Ϊ�����¶ȣ�WI2��ƽ�⺬�����ͣ�˵�������¶ȣ���ѧƽ�����淴Ӧ�����ƶ�������ƽ���ƶ�ԭ���������¶ȣ���ѧƽ�������ȷ�Ӧ�����ƶ����淴Ӧ����Ϊ���ȷ�Ӧ����������ӦΪ���ȷ�Ӧ����˦�H <0. �ڴӷ�Ӧ��ʼ��t1ʱ���ڵ�ƽ����Ӧ����v(I2) =v(WI2)= ��c/��t=1.80��10-3mol/0.05L��t1min="0.036/t1mol/(L��min)" .��A. ʹ�ò����ĵ�W��I2������Ӧ��ȡ����WI2������Ӧ�ﵽƽ��������¶ȣ�ƽ�������ƶ������ܲ��������ĵ���W����˿����ø÷�Ӧԭ�������ᴿ�١���ȷ��B. ����W�ǹ��壬Ũ�Ȳ���ı䣬���Ը÷�Ӧ��ƽ�ⳣ������ʽ��
2HCl+O2������84����Һ����������Ũ���ᣩ���ʹ�ÿ��ܻᷢ����Ӧ��ClO-+Cl-+2H+= Cl2��+H2O�����ж�������Cl2�����ж�����4������Ϊ�����¶ȣ�WI2��ƽ�⺬�����ͣ�˵�������¶ȣ���ѧƽ�����淴Ӧ�����ƶ�������ƽ���ƶ�ԭ���������¶ȣ���ѧƽ�������ȷ�Ӧ�����ƶ����淴Ӧ����Ϊ���ȷ�Ӧ����������ӦΪ���ȷ�Ӧ����˦�H <0. �ڴӷ�Ӧ��ʼ��t1ʱ���ڵ�ƽ����Ӧ����v(I2) =v(WI2)= ��c/��t=1.80��10-3mol/0.05L��t1min="0.036/t1mol/(L��min)" .��A. ʹ�ò����ĵ�W��I2������Ӧ��ȡ����WI2������Ӧ�ﵽƽ��������¶ȣ�ƽ�������ƶ������ܲ��������ĵ���W����˿����ø÷�Ӧԭ�������ᴿ�١���ȷ��B. ����W�ǹ��壬Ũ�Ȳ���ı䣬���Ը÷�Ӧ��ƽ�ⳣ������ʽ��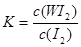 ������C����˿�����¶�Խ�ߣ��ṹƽ���ƶ�ԭ����֪:��˿��������WI2�ͻ������ƶ������������W�����³�������˿�ϡ���ȷ����5������Ksp(AgI)< Ksp(AgI).�������Ȳ����ij���ΪAgI���ڻ��ǰn(K+)=(5mL+5mL)��10-3L/mL��0.1mol/L=0.001mol;n(Ag+)=n(NO3-)=0.006L��0.1mol/L=0.0006mol;n(Cl-)=n(I-)=0.005L��0.1mol/L=0.0005mol;�ڻ����Һ��K+��NO3-�����ģ�������Ӧ��Ag++I-=AgI����Ag++Cl-=AgCl��.�������ĵ��������ʵ�������ȷ����Һ�����ӵ�Ũ�ȴ�С��ϵΪ��c(K+)> c(NO3-)> c(Cl-)> c(Ag+)> c(I-).
������C����˿�����¶�Խ�ߣ��ṹƽ���ƶ�ԭ����֪:��˿��������WI2�ͻ������ƶ������������W�����³�������˿�ϡ���ȷ����5������Ksp(AgI)< Ksp(AgI).�������Ȳ����ij���ΪAgI���ڻ��ǰn(K+)=(5mL+5mL)��10-3L/mL��0.1mol/L=0.001mol;n(Ag+)=n(NO3-)=0.006L��0.1mol/L=0.0006mol;n(Cl-)=n(I-)=0.005L��0.1mol/L=0.0005mol;�ڻ����Һ��K+��NO3-�����ģ�������Ӧ��Ag++I-=AgI����Ag++Cl-=AgCl��.�������ĵ��������ʵ�������ȷ����Һ�����ӵ�Ũ�ȴ�С��ϵΪ��c(K+)> c(NO3-)> c(Cl-)> c(Ag+)> c(I-).

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��������ά���ϳ���ά���ά�����л��߷��ӻ����� |
| B��̫���ܵ�ؿ����ù������������Ӧ�������ڽ��ܻ��� |
| C��������ˮΪ֮��������ˮ����˵����ͬ������ˮ�ͱ���ˮ�������� |
| D����¯�г�����CaSO4����Na2CO3��Һ���ݺ��������ܽ��ȥ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������ý�屨����ij���е����ܼ��Ƕ����彡���������� |
| B�����ʯ����Ȼ����Ӳ������ |
| C�����á�84������Һ�Ի����������� |
| D��NO������ij���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
A��MnO2+4HCl(Ũ) MnCl2+2H2O+Cl2�� MnCl2+2H2O+Cl2�� |
B��2HCl+Ca(OH)2 CaCl2+2H2O CaCl2+2H2O |
C��5Cl2+I2+6H2O 10HCl+2HIO3 10HCl+2HIO3 |
D��2KClO3 2KCl+3O2�� 2KCl+3O2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��


| A����ͼ��:���MnO2����,�����ȫ�������� |
| B����ͼ��:ʪ�����ɫ������ɫ,֤��Cl2��Ư���� |
| C����ͼ��:������ɫ�Ĺ���,֤��Cl2��ǿ������ |
| D����ͼ��:���պ���Ͳ�����������С,˵��������Cl2�����˼ӳɷ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���ӵ�ʳ���м�����ǵ���� |
| B��������ɱ��������84����Һ�ijɷ���Һ�� |
| C��������������Һ������ˮ������ˮ |
| D����ɫ�۾����������ĵ�������Ҫ�õ��廯�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��Ư�۵ijɷ�Ϊ������� |
| B��ʵ���ҿ���Ũ������ﰱ�� |
| C��ʵ���ҿ���NaOH��Һ����NO2��HCl���� |
| D��Al2(SO4)3�ɳ�ȥ���Է�ˮ�����Է�ˮ�е��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��71g��������Ʒ��1Ħ������ |
| B��22.4L��������Ʒ������74g |
| C��37g��������Ʒ������NaOH��ȫ��Ӧ����Na37Cl��Na37ClO3���������ͻ�ԭ��������֮��Ϊ5:1 |
| D��0.1Ħ��������������ˮ�γ�1000mL��Һ����Һ��c(Cl-)+ c(ClO-)=0.1mol��L |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com