
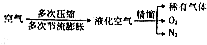
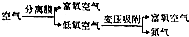
分析 (1)碳氢耗氧法需要其它燃料除去氧气,造成资源浪费;
(2)制备N2的三种方法均以空气为原料,①需要燃料和氧气反应而除去氧气,②③中采用物理方法除去氧气;
(3)电解法制氢气是将电能转化为化学能;
(4)目前工业生产中,制备H2仍然主要来自水煤气法,而不采用电解法,因为要考虑经济效益.
解答 解:(1)碳氢耗氧法需要其它燃料燃烧而除去氧气,造成资源浪费,且反应后生成的气体也是混合物,要除杂,操作麻烦,故答案为:浪费资源、操作麻烦;
(2)制备N2的三种方法均以空气为原料,①需要燃料和氧气反应而除去氧气,②③中采用物理方法除去氧气,所以涉及化学反应的是①,故答案为:①;
(3)电解法制氢气中是通过电能将水分解得到氢气,所以是将电能转化为化学能,故答案为:电能转化为化学能;
(4)目前工业生产中,制备H2仍然主要来自水煤气法,而不采用电解法,因为要考虑经济效益,成本越低越好,故选BD.
点评 本题考查物质制备,为高频考点,涉及物质分离和提纯、能量转化等知识点,是将化学理论应用于生产实际中,需要学生充分利用化学知识灵活解答问题,题目难度不大.


科目:高中化学 来源: 题型:解答题
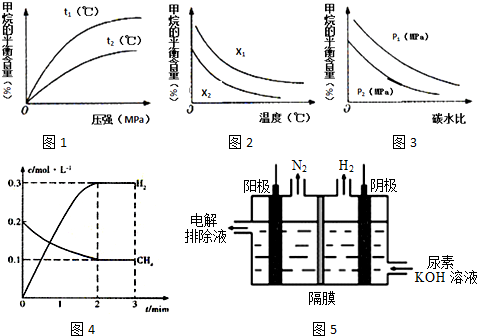
| t/min | n(CH4)/mol | n(H2O)/mol | n(CO)/mol | n(H2)/mol |
| t1 | 0.18 | 0.38 | 0.22 | 0.66 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 简单阳离子的氧化性:Z>X | |
| B. | 气态氢化物的稳定性:M>Y | |
| C. | 简单离子半径由大到小的顺序是:M>Y>Z | |
| D. | 在X2M与Z2M的溶液中,水的电离程度,前者大于后者 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3COOH溶液与Zn反应放出H2 | |
| B. | 0.1 mol/L CH3COONa溶液的pH大于7 | |
| C. | CH3COOH溶液与Na2CO3反应生成CO2 | |
| D. | 0.1 mol/L CH3COOH溶液可使紫色石蕊变红 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.80 | B. | 0.85 | C. | 0.90 | D. | 0.93 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
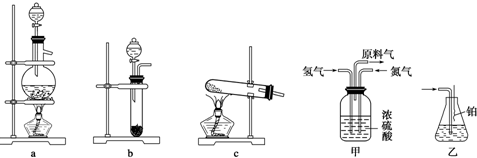
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com