
分析 (1)浓H2SO4的物质的量浓度c=$\frac{1000ρω}{M}$;根据溶液稀释前后物质的量不变即c(稀)V(稀)=c(浓)V(浓)计算所需浓硫酸的体积;
(2)根据所需浓硫酸的体积选择量筒的规格,为减少误差选择略大于所需浓硫酸体积且规格相近的量筒;
(3)浓硫酸溶于水放出大量的热,应防止酸液飞溅;
(4)移液时用玻璃棒引流,注意冷却后再转移到容量瓶中;
(5)加水至距刻度1-2cm处,改用胶头滴管加水,使溶液的凹液面正好跟刻度相平.
解答 解:(1)浓H2SO4的物质的量浓度c=$\frac{1000ρω}{M}$=$\frac{1000×1.84×98%}{98}$mol/L=18.4mol/L;根据稀释定律,稀释前后溶质的物质的量不变,设浓硫酸的体积为xmL,所以xmL×18.4mol/L=500mL×0.5mol/L,解得:x≈13.6,所以量取的浓硫酸体积是13.6mL,故答案为:13.6;
(2)所需浓硫酸的体积为13.6mL,所以选择15mL量筒,量取时发现量筒不干净,用水洗净后直接量取,将导致量筒残留一部分水,实际量取液体体积偏小,浓度偏低,故答案为:15;偏低;
(3)浓硫酸稀释的方法为:稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入盛有水的烧杯中,同时用玻璃棒不断搅拌,以使热量及时地扩散,防止浓硫酸飞溅;切不可把水注入浓硫酸中;故答案为:烧杯;防止浓硫酸飞溅;
(4)根据溶液的配置步骤可知,将冷却后的溶液沿着玻璃棒注入500mL容量瓶中,并用50mL蒸馏水洗涤烧杯2~3次,洗涤液要转移到容量瓶中,摇匀,如未冷却就转移,则所配溶液体积偏小,浓度会偏高,若未洗涤烧杯,则所配溶液的浓度无影响,
故答案为:玻璃棒;500mL容量瓶;2~3;偏高;无影响;.
(5)加水至距刻度1-2cm处,改用胶头滴管加水,使溶液的凹液面正好跟刻度相平,摇匀,故答案为:1-2cm;胶头滴管;凹液面正好跟刻度相平.
点评 本题考查一定物质的量浓度溶液配制,为高频考点,侧重于学生的分析、计算和实验能力的考查,题目涉及物质的量浓度有关计算、仪器的选择等,难度不大.


科目:高中化学 来源: 题型:选择题

| A. | 该同学的实验目的是分离氯化钠、氯化钙 | |
| B. | 上图括号内的操作步骤均为加热蒸发 | |
| C. | 按此实验方案可得到较纯净的NaCl固体 | |
| D. | 按此实验方案可得到较纯净的CaCl2固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化石燃料的直接利用,促进了低碳经济的发展 | |
| B. | 新材料的研制和应用,提高了人们的生活品质 | |
| C. | 合成药物的研发和使用,促进了医疗卫生事业的发展 | |
| D. | 化肥的合理使用提高了农作物产量,缓解了人类粮食危机 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

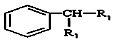 $\stackrel{KMnO_{4}/H+}{→}$
$\stackrel{KMnO_{4}/H+}{→}$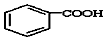
 (-R1、R2表示氢原子或烃基)
(-R1、R2表示氢原子或烃基) ,C的结构简式为CH3CH2OH,
,C的结构简式为CH3CH2OH,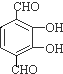 、
、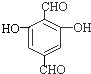 .
. ,反应类型是取代反应.
,反应类型是取代反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在101kPa下,1g物质完全燃烧所放出的热量叫做该物质的热值 | |
| B. | 把FeCl3的水溶液加热蒸干可得到FeCl3固体 | |
| C. | 用25mL碱式滴定管量取20.00mL高锰酸钾溶液 | |
| D. | 太阳能电池是把太阳能转化为内能的装置 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 950 mL,76 g | B. | 500 mL,80 g | C. | 1000 mL,80 g | D. | 1000 mL,76 g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com