
 Mn2++Cl2↑+2H2O;
Mn2++Cl2↑+2H2O; Mn2++Cl2↑+2H2O;
Mn2++Cl2↑+2H2O;

科目:高中化学 来源: 题型:
| 95~100℃ |
| 111~140 |
| 物质 | S | CS2 | CCl4 | S2Cl2 |
| 沸点/℃ | 445 | 47 | 77 | 137 |
| 熔点/℃ | 113 | -109 | -23 | -77 |

| ||
| ||


查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
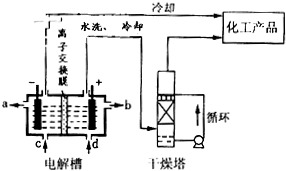
| ||
| ||
| △ |
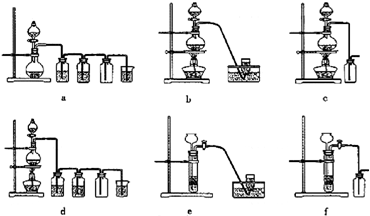
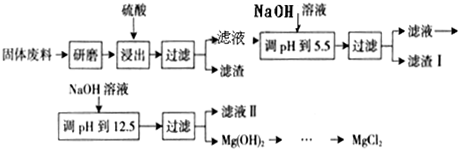
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| PH | 3.2 | 5.2 | 12.4 |
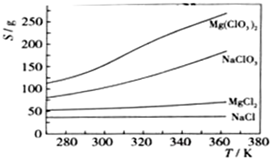
查看答案和解析>>
科目:高中化学 来源:学习周报 化学 人教课标高一版(必修1) 2009-2010学年 第19~26期 总第175~182期 人教课标版 题型:022
物质分离的三类操作
(1)过滤和蒸发(分别如图1、图2所示)

过滤是将
________分离的一种方法.如粗盐提纯、氯化钾和二氧化锰的分离.过滤时应注意:①一贴:将滤纸折叠好放入漏斗,加少量蒸馏水润湿,使滤纸紧贴漏斗内壁;②二低:滤纸边缘应略低于漏斗边缘,加入漏斗中液体的液面应略低于滤纸的边缘;③三靠:向漏斗中倾倒液体时,烧杯的夹嘴应与玻璃棒接触,玻璃棒的底端应和三层滤纸处轻轻接触,漏斗颈的末端应与接受器的内壁相接触.蒸发是将
________的方法,结晶是溶质从溶液中析出晶体的过程.该方法可以用来分离和提纯几种可溶性的固体混合物.结晶的原理是________,从而使晶体析出.加热蒸发皿使溶液蒸发时,要用玻璃棒不断搅动溶液,原因是________.当蒸发皿中出现较多的固体时要停止加热.(2)蒸馏和萃取(分别如图3、图4所示)

这两种方法主要用于液体间的分离.
蒸馏和分馏用于分离
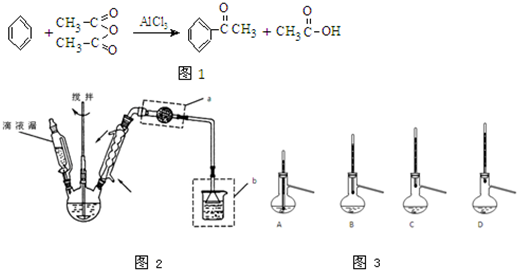
________.如蒸馏水的制备、酒精和水的分离、从普通白酒中提取无水酒精等.在蒸馏时,要用石棉网,目的是________;使用碎瓷片是要________;温度计的水银球不能插入液体中,而要与支管口持平,以测量________的温度;冷凝器中水的流向是________,防止因水流不匀(或水流中出现气泡)而使冷凝管炸裂,且冷凝充分.萃取的原理是
________.萃取剂的选择原则是:①与原溶液中的溶剂互不相溶、互不反应,且密度相差较大;②溶质在萃取剂中的溶解度大于在原溶剂中的溶解度;③溶质与萃取剂易于分离.如用CCl4从碘水中提取碘.萃取后的溶液,我们一般要结合分液操作.分液是将________液体混合物进行分离的方法.如汽油和水的分离.(3)洗气(如图5所示)
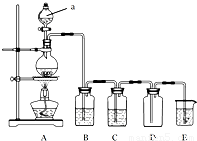
洗气常用于气体混合物的分离、除杂.根据气体性质的不同,我们可以将气体通过盛有一定除杂试剂的洗气瓶或干燥管,如实验室制备氯气时一般利用盛有饱和食盐水、浓硫酸的洗气瓶分别除去氯化氢、水蒸气.

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com