
【题目】溴化亚铜(CuBr)常用作有机合成原料和反应催化剂等,它是一种不溶于水的白色结晶粉末,受热或见光易分解,接触空气会被缓慢氧化成绿色粉末。制备CuBr的实验步骤如下:
步骤1:在如图所示的三颈烧瓶中加入45gCuSO4·5H2O、19gNaBr、150mL煮沸过的蒸馏水,60℃时不断搅拌,以适当流速通入SO22小时。
步骤2:溶液冷却后倾去上层清液,在避光的条件下过滤。
步骤3:依次用溶有少量SO2的水、溶有少量SO2的乙醇、纯乙醚洗涤。
步骤4:将获得的产品经系列干燥剂干燥后,再进行真空干燥。

请根据上述制备步骤回答有关问题:
(1)制备中用到的SO2在实验室中通常是用浓硫酸和亚硫酸钠为原料来制备的,在制备SO2时装置可以选择下图中的____________(填装置编号),发生反应的化学方程式为____________。
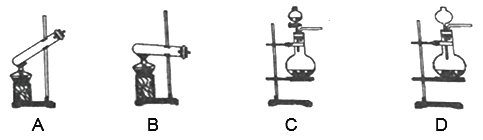
(2)步骤1中:①所用蒸馏水需提前煮沸处理,这样做的目的是____________。
②为控制反应在60℃进行可采取的措施是________________。
③三颈烧瓶中反应生成CuBr的离子方程式为_____________。
④判断反应已经完成的现象是______________。
(3)步骤2在过滤时需要避光的原因是___________。
(4)步骤3中用到的洗涤剂水、乙醇中均“溶有少量SO2”的原因是____________。
(5)欲利用上述装置烧杯中的吸收液(经检测主要含Na2SO3、NaHSO3等)制取较纯净的Na2SO3·7H2O晶体。需用到以下试剂:SO2(贮存在钢瓶中)、100g20%NaOH溶液、乙醇等。请将下列实验步骤补充完整。
①向烧杯中继续通入SO2至溶液饱和;②____________;③加入少量维生素C溶液(抗氧化剂),蒸发浓缩,冷却结晶;④______________;⑤放真空干燥箱中干燥。
【答案】 C H2SO4+Na2SO3═Na2SO4+H2O+SO2↑ 除去水中的O2 60℃水浴加热 2Cu2++2Br-+SO2+2H2O═2CuBr↓+SO42-+4H+ 溶液蓝色完全褪去 防止CuBr见光分解 防止CuBr被氧化 然后向烧杯中加入100g20%NaOH溶液 过滤,然后用乙醇洗涤产品2—3次
【解析】(1)制备SO2用固体与液体不加热,故选C装置;反应为 H2SO4+Na2SO3═Na2SO4+H2O+SO2↑;(2),步骤1中:①CuBr接触空气会被缓慢氧化成绿色粉末,所用蒸馏水需提前煮沸处理,这样做的目的是除去水中的O2,防止氧化CuBr;②控制反应在100℃以下常用水浴加热,为控制反应在60℃进行可采取的措施是60℃水浴加热;③SO2作还原剂,三颈烧瓶中反应生成CuBr的离子方程式为2Cu2++2Br-+SO2+2H2O═2CuBr↓+SO42-+4H+ ;④Cu2+ 溶液呈蓝色,判断反应已经完成的现象是溶液蓝色完全褪去;(3)溴化亚铜(CuBr)常用作有机合成原料和反应催化剂等,它是一种不溶于水的白色结晶粉末,受热或见光易分解,步骤2在过滤时需要避光的原因是防止CuBr见光分解;(4)步骤3中用到的洗涤剂水、乙醇中均“溶有少量SO2”的原因是保持还原性条件,防止CuBr被氧化;(5)吸收液主要含Na2SO3、NaHSO3,向烧杯中继续通入SO2至溶液饱和,将Na2SO3转化为NaHSO3,根据钠守恒,溶液中NaHSO3为0.5mol,②然后向烧杯中加入100g20%NaOH溶液,将NaHSO3再转化为Na2SO3,加入少量维生素C溶液(抗氧化剂),蒸发浓缩,冷却结晶;过滤,然后用乙醇洗涤产品2—3次,除去表面的杂质,放真空干燥箱中干燥。


 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案科目:高中化学 来源: 题型:
【题目】某有机物的结构简式如图,下列说法正确的是( )
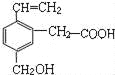
A. 该有机物的分子式为C11H15O3
B. 该有机物不能发生取代反应
C. 1 mol该物质与足量的钠反应可以生成1 mol氢气
D. 1 mol该有机物可以与1 mol碳酸钠发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在极性分子中,正电荷重心同负电荷重心间的距离称偶极长,通常用d表示。极性分子的极性强弱同偶极长和正(或负)电荷重心的电量(q)有关,一般用偶极距(μ)来衡量。分子的偶极矩定义为偶极长和偶极上一端电荷电量的乘积,即μ=d·q。试回答以下问题:
(1)HCl、CS2、H2S、SO2四种分子中μ=0的是____。
(2)对硝基氯苯、邻硝基氯苯、间硝基氯苯,三种分子的偶极矩由大到小的排列顺序是________。
(3)实验测得:μ(PF3)=1.03德拜;μ(BCl3)=0。由此可知,PF3分子是____构型,BCl3分子是____构型。
(4)冶癌药Pt(NH3)2Cl2具有平面四边形结构,Pt处在四边形中心,NH3和Cl分别处在四边形的4个角上。已知该化合物有两种异构体。棕黄色者μ>0,淡黄色者μ=0。试画出两种异形体的构型图。
构型图:淡黄色____________________,棕黄色____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上以铬铁矿(含有Cr2O3,FeO、Al2O3、SiO2等成分)为主要原料生产重铬酸钠晶体(Na2Cr2O7·2H2O),其主要工艺流程如下:
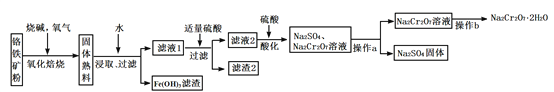
提示:熟料中含有Na2CrO4、NaFeO2等成分。
回答下列问题:
(1)将铬铁矿粉碎的目的是_____________________________ 。
(2)氧化焙烧时,生成Na2CrO4的化学方程式是__________。
(3)滤渣2中除Al(OH)3外还有__________(填化学式)。
(4)加入硫酸酸化的目的是__________________________。
(5)根据下图,请将操作a补充完整:________________,洗涤,干燥。
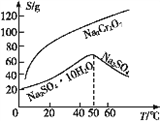
(6)控制105~110℃,向较浓的Na2Cr2O7溶液中加入KCl固体发生复分解反应,立即析出K2Cr2O7晶体。能生成K2Cr2O7晶体的原因是_____________。
(7)向Na2Cr2O7酸性溶液中加入过量FeSO4溶液,生成Cr3+和 Fe3+,再加入过量的强碱溶液生成铁铬氧体沉淀(CrxFe3-xO4)。加入过量强碱生成铁铬氧体沉淀的离子方程式是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物E(结构简式为 )是合成消毒剂α——萜品醇(结构简式为
)是合成消毒剂α——萜品醇(结构简式为 )的中间体。由甲苯经一系列变化制取E的流程如下:
)的中间体。由甲苯经一系列变化制取E的流程如下:

请回答下列问题:
(1)化合物E中含有的官能团名称为________,α—萜品醇的分子式为_________,甲苯的结构简式为_____。
(2)反应I的化学方程式为____________。
(3)反应II的反应类型是__________________。
(4)反应III的试剂与条件为__________________。
(5)写出一种符合下列条件的有机物的结构简式_____________。
①是化合物D的一种同分异构体;②能与NaHCO3反应;③能与新制氢氧化铜浊液在加热条件下反应生成红色固体;④在核磁共振氢谱上有5个峰。
(6)下面是由化合物E合成一种α—萜品醇的流程的一部分,请将其中有G生成H的几步流程补充完整(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件).________________。

提示:
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中不宜用物理性质区别的是( )
A. Na2CO3 和 CaCO3 固体 B. 酒精和汽油
C. 氯化铵和硝酸铵晶体 D. 碘和高锰酸钾固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】离子液体在有机合成、无机合成等方面有着重要应用。咪唑是合成“离子液体”的一种原料,其结构如图所示。下列有关咪唑说法不正确的是
![]()
A. 化学式C3H4N2
B. 分子中含有一种非极性键和两种极性键
C. 可以发生取代、加成、氧化反应
D. 一氯取代物的同分异构体共有4种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式的书写正确的是
A.铁和稀硫酸反应 2Fe + 6H+ == 2Fe3+ + 3H2↑
B.向硫酸钠溶液中滴加氯化钡溶液Ba2+ + SO42― == BaSO4↓
C.氯水加入到溴化钾溶液中Br―+ Cl2 == Br2 + Cl―
D.碳酸钙溶于稀盐酸 CO32― + 2H+ == H2O + CO2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com