
| 阳离子 | Ag+ Na+ |
| 阴离子 | NO3- SO42- Cl- |

分析 (1)接通电源,经过一段时间后,测得乙中C电极质量增加了27克,说明C电极是阴极,连接C电极的电源电极为负极;C电极上质量增加,析出金属单质,所以乙装置中含有银离子,电解乙装置中电解质溶液,溶液的pH值减小,所以阳极上析出氢氧根离子,根据离子的放电顺序判断电解质;电解时,甲装置中溶液的pH值增大,说明阴极上氢离子放电,阳极上放电能力比氢氧根离子强的离子放电,据此判断电解质;
(2)电解硝酸银溶液时,阳极上氢氧根离子放电,阴极上银离子放电,同时生成硝酸,写出相应的电池反应式;
(3)根据电解方程式计算生成的氢氧化钠的浓度,进而计算溶液的pH;
(4)在燃料电极的正极上是氧气发生得电子的还原反应;
(5)电解硫酸钠溶液,实质电解水,加相应质量的水恢复原样,结合电子守恒计算.
解答 解:(1)接通电源,经过一段时间后,测得乙中C电极质量增加了27克,说明C电极是阴极,所以连接阴极的电极M是原电池的负极;电解时,甲装置中溶液的pH值增大,说明阳极上是放电能力大于氢氧根离子的离子放电,根据表格知,为氯离子,氯离子和银离子能生成沉淀,所以甲装置电解质溶液是氯化钠溶液;电解时,装置乙中pH值减小,说明阳极上是氢离子放电,溶液中含有的阴离子是含氧酸根离子,阴极上析出金属,所以含有银离子,该电解质溶液是硝酸银溶液.
故答案为:负;NaCl;
(2)根据(1)推导知道甲溶液是氯化钠,乙溶液是硝酸银,丙溶液只能是硫酸钠,乙中c电极质量增加了,所以c电极是阴极,所以d是阳极,e是阴极,f是阳极,乙中C电极质量增加了27克,根据Ag+e-=Ag,所以转移电子是$\frac{27g}{105g/mol}$=0.25mol,f电极反应为:4OH--4e-=O2↑+2H2O,转移电子0.25mol,所以产生氧气是$\frac{1}{4}×0.25mol$×22.4L/mol=1.4L,故答案为:1.4L;
(3)乙溶液是硝酸银,电解硝酸银溶液的电解方程式为:4AgNO3+2H2O$\frac{\underline{\;通电\;}}{\;}$4Ag+O2↑+4HNO3,故答案为:4AgNO3+2H2O$\frac{\underline{\;通电\;}}{\;}$4Ag+O2↑+4HNO3;
(4)电解甲溶液的电极反应式为:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑,当转移电子0.25mol,生成氢氧化钠的物质的量是0.25mol,所以氢氧化钠的浓度是:$\frac{0.25mol}{25L}$=0.01mol/L,所以溶液的pH=12,故答案为:12;
(5)丙溶液是硫酸钠,电解硫酸钠溶液实质是电解水,电解质在电解以后要想复原,符合的原则是:出什么加什么,所以要加入水才能复原,当转移电子0.25mol,消耗水的物质的量是$\frac{0.25mol×2}{4}$=0.125mol,质量是0.125mol×18g/mol=2.25g,故答案为:2.25g;H2O.
点评 本题考查了原电池和电解池原理,明确“C电极上质量的变化”的意思是解本题的关键,根据原电池和电解质各电极上发生反应的类型即可解答本题,难度不大.


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:选择题
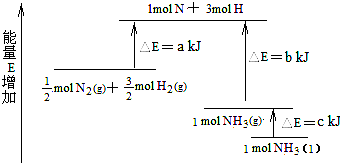
| A. | N2(g)+H2(g)=NH3(l)△H=+(b+c-a)kJ•mol-1 | |
| B. | N2(g)+3H2(g)=2NH3(g)△H=+2(b-a)kJ•mol-1 | |
| C. | N2(g)+3H2(g)=2NH3(l)△H=-2(b+c-a)kJ•mol-1 | |
| D. | N2(g)+H2(g)=NH3(g)△H=+(a+b)kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | S | B. | C | C. | Cl | D. | F |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 肯定存在的离子 | 肯定没有的离子 | |
| 化学式或离子符号 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.6 mol SO2+0.3 mol O2+0.4 mol SO3 | |
| B. | 4.0 mol SO2+1.0 mol O2 | |
| C. | 2.0 mol SO2+1.0 mol O2+2.0 mol SO3 | |
| D. | 3.0 mol SO2+1.0 mol O2+1.0 mol SO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCl、NO2、N2、粉尘 | B. | CO2、Cl2、N2、雾 | C. | SO2、NO2、CO、烟尘 | D. | CO2、NO、NH3、H2S |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(NH4+)>c(SO42-)>c(H+)>c(OH-) | B. | c(SO42-)>c(NH4+)>c(OH-)>c(H+) | ||
| C. | c(NH4+)>c(SO42)>c(OH-)>c(H+) | D. | c(SO42-)>c(H+)>c(NH4+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
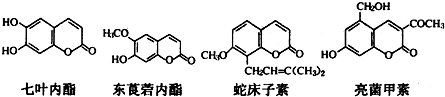
| A. | 七叶内酯与东茛菪内酯互为同系物 | |
| B. | 四种化合物含有的官能团种类完全相同 | |
| C. | l mol上述四种物质与足量氢氧化钠溶液反应,消耗氢氧化钠最多的是亮菌甲素 | |
| D. | 它们都能使溴的四氯化碳溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 有关柠檬烯的分析正确的是( )
有关柠檬烯的分析正确的是( )| A. | 柠檬烯的一氯代物有9种 | |
| B. | 柠檬烯和丁基苯(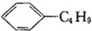 )互为同分异构体 )互为同分异构体 | |
| C. | 柠檬烯的分子中所有的碳原子可能在同一个平面上 | |
| D. | 一定条件下,柠檬烯可以发生加成、取代、氧化等反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com