
| A. | C与Si位于同一主族,且干冰与SiO2都是酸性氧化物,所以二者晶体类型相同 | |
| B. | NaCl和AlCl3均为强电解质,二者在熔融状态下都能导电 | |
| C. | 从晶体类型上来看物质的熔沸点,其规律是:原子晶体>离子晶体>分子晶体 | |
| D. | 第二周期非金属元素的气态氢化物溶于水后,水溶液均为酸性 |
分析 A.二氧化碳是分子晶体、二氧化硅是原子晶体;
B.氯化铝是分子晶体,熔融状态下以分子存在;
C.原子晶体的熔沸点与共价键有关,离子晶体熔沸点与离子键有关,分子晶体熔沸点与分子间作用力有关,晶体熔沸点:原子晶体>离子晶体>分子晶体;
D.第二周期非金属元素的气态氢化物氨气溶于水后溶液呈碱性.
解答 解:A.二氧化碳晶体的构成微粒是分子、二氧化硅晶体的构成微粒是原子,所以二氧化碳是分子晶体、二氧化硅是原子晶体,二者晶体类型不同,故A错误;
B.氯化铝是分子晶体,熔融状态下以分子存在,所以熔融状态下氯化铝不导电,故B错误;
C.原子晶体的熔沸点与共价键有关,离子晶体熔沸点与离子键有关,分子晶体熔沸点与分子间作用力有关,晶体熔沸点:原子晶体>离子晶体>分子晶体,金属晶体熔沸点差异性较大,故C正确;
D.第二周期非金属元素的气态氢化物氨气溶于水后溶液呈碱性,HF的水溶液呈酸性,故D错误;
故选C.
点评 本题考查晶体类型判断、晶体熔沸点大小比较、氢化物水溶液酸碱性等知识点,为高频考点,明确物质构成微粒及物质性质是解本题关键,注意规律中的反常现象,一般来说非金属氢化物的水溶液呈酸性,但氨气水溶液呈碱性,易错选项是D.


科目:高中化学 来源: 题型:解答题
| pH | NaH2PO4溶液体积/mL | Na2HPO4溶液体积/mL |
| 5.7 | 93.5 | 6.5 |
| 5.8 | 92 | 8 |
| 5.9 | 90 | 10 |
| 6.0 | 87.7 | 12.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
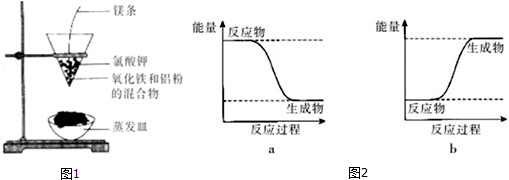
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 将铁片和碳棒按图示方式插入硫酸铜溶液中,电流计指针发生偏转.下列针对该装置的说法,正确的是( )
将铁片和碳棒按图示方式插入硫酸铜溶液中,电流计指针发生偏转.下列针对该装置的说法,正确的是( )| A. | 碳棒是负极 | |
| B. | 该装置能将电能转化为化学能 | |
| C. | 外电路中电流由铁片流出经过电流计流向碳棒 | |
| D. | 该装置的总反应为:Fe+Cu2+=Fe2++Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 能发生氧化、取代、加成反应 | |
| B. | 分子中含有2个手性碳原子 | |
| C. | 1 mol该化合物与足量浓溴水反应,最多消耗3 mol Br2 | |
| D. | 1 mol该化合物与足量NaOH溶液反应,最多消耗5 mol NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯发生加聚反应制得聚乙烯高分子材料 | |
| B. | 用甲烷与氯气制备一氯甲烷 | |
| C. | 用石灰石和稀盐酸反应制得二氧化碳 | |
| D. | 用苯和液溴为原料制取溴苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氟的原子半径比氯的原子半径小 | B. | 氟化氢比氯化氢稳定 | ||
| C. | 氟的最高价是+7价 | D. | 氟气的氧化性比氯气的强 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com