
【题目】下列元素处于周期表第三周期的是
A. 硅 B. 氢 C. 碳 D. 氮
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】已知:实验室可供选择的用于去除气体杂质的试剂有:浓硫酸、无水氯化钙、五氧化二磷、碱石灰(主要成分为NaOH和CaO) 
①实验室用如图1所示装置进行纯净干燥的氢气还原氧化铁实验.a装置名称为 , 方框B内应选用如图2装置(填“Ⅰ”或“Ⅱ”),选用的除杂试剂为(填试剂名称).
②实验室常用36.5%浓盐酸(ρ=1.2gcm﹣3)配制稀盐酸,若要配制500mL,0.5molL﹣1稀盐酸,需用量筒取用浓盐酸mL.
③写出装置C中发生反应的化学方程式并用单线桥标明电子的转移 . 实验结束时应该采取的操作是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“低碳循环”引起各国的高度重视,已知煤、甲烷等可以与水蒸气反应生成以CO和H2为主的合成气,合成气有广泛应用。试回答下列问题:
(1)高炉炼铁是CO气体的重要用途之一,其基本反应为:
FeO(s)+CO(g) ![]() Fe(s)+CO2(g) ΔH>0。
Fe(s)+CO2(g) ΔH>0。
已知在1100 ℃时,该反应的化学平衡常数K=0.263。
①温度升高,化学平衡移动后达到新的平衡,此时平衡常数K值________(填“增大”、“减小”或“不变”);
②1100 ℃时测得高炉中,[CO2]=0.025 mol·L-1,[CO]=0.1 mol·L-1,则在这种情况下,该反应向______进行(填“左”或“右”),判断依据是__________________________。
(2)目前工业上也可用CO2来生产燃料甲醇,有关反应为:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1,现向体积为1 L的密闭容器中,充入1 mol CO2和3 mol H2,反应过程中测得CO2和CH3OH(g)的浓度随时间的变化如图所示。
CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1,现向体积为1 L的密闭容器中,充入1 mol CO2和3 mol H2,反应过程中测得CO2和CH3OH(g)的浓度随时间的变化如图所示。
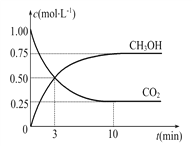
①从反应开始到平衡,氢气的平均反应速率v(H2)=____。
②反应达到平衡后,下列措施能使![]() 增大的是_____(填符号)。
增大的是_____(填符号)。
A.升高温度 B.再充入H2 C.再充入CO2
D.将H2O(g)从体系中分离 E.充入He(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的分类正确的是( )
碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 | |
A | Na2CO3 | H2SO4 | Cu2(OH)2CO3 | Fe2O3 | SO3 |
B | NaOH | HCl | NaCl | Na2O | CO |
C | NaOH | NaHSO4 | CaF2 | MgO | SO2 |
D | KOH | HNO3 | NaHCO3 | CaO | CO2 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮的氧化物(NOx)是大气污染物之一,工业上在一定温度和催化剂条件下用NH3将NOx还原生成N2,某同学在实验室中对NH3与NOx反应进行了探究。回答下列问题:
(1)氨气的制备

①氨气的发生装置可以选择上图中的________,反应的化学方程式为______________。
②预收集一瓶干燥的氨气,选择上图中的装置,其连接顺序为:发生装置→______(按气流方向,用小写字母表示)。
(2)氨气与二氧化氮的反应将上述收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好)。在一定温度下按图示装置进行实验。

操作步骤 | 实验现象 | 解释原因 |
打开K1,推动注射器活塞,使X中的气体缓慢通入Y管中 | ①Y管中_____________ | ②反应的化学方程式 ____________ |
将注射器活塞退回原处并固定,待装置恢复到室温 | Y管中有少量水珠 | 生成的气态水凝集 |
打开K2 | ③_______________ | ④______________ |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室有少量汞不慎撒落,处理方法是将硫黄粉撒在汞的表面,发生反应的化学方程式为Hg+S=HgS,该反应属于( )
A.置换反应B.化合反应C.分解反应D.复分解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,错误的是
A、化学反应必然伴随能量变化
B、需加热才能发生的化学反应一定是吸热反应
C、化学反应中的能量变化主要是由化学键的断裂和形成引起的
D、反应物与生成物总能量的相对大小决定反应是吸热或放热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,向一个容积不变的容器中,加入3molSO2和2molO2 及固体催化剂,使之反应。2SO2(g) + O2 (g) ![]() 2SO3 (g) ;△H=-196.6kJ/mol。平衡时容器内气体压强为起始时的90%。此时。
2SO3 (g) ;△H=-196.6kJ/mol。平衡时容器内气体压强为起始时的90%。此时。
Ⅰ、加入3molSO2和2molO2 发生反应,达到平衡时,放出的热量为 ___________ 。
Ⅱ、保持同一反应温度,在相同的容器中,将起始物质的量改为amolSO2、bmolO2、cmolSO3(g),欲使平衡时SO3的体积分数为2/9 ,
①达到平衡时,Ⅰ与Ⅱ放出的热量________(填序号)。
A、一定相等 B、前者一定小 C、前者大于或等于后者 D.无法判断
②a、b、c必须满足的关系是(一个用a、c表示,另一个用b、c表示)__________、______。
③欲使起始时反应表现为向正反应方向进行,a的取值范围是:_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方案能达到目的的是( )
A.用排水集气法收集HCl气体
B.用燃烧的木条检验N2和CO2
C.用KSCN溶液检验溶液中的Fe3+
D.用丁达尔效应鉴别Na2CO3溶液和NaHCO3溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com