
����Ŀ����������ѧ���������ҹ����в��Ų����������������ƣ�Na2S2O8������SΪ��6�ۣ�ȥ����ˮ�е��������[As(V)]���о��ɹ����䷴Ӧ����ģ����ͼ��ʾ���谢���ӵ�������ֵΪNA��Ksp[Fe(OH)3]=2.7��10��39������������ȷ���ǣ� ��
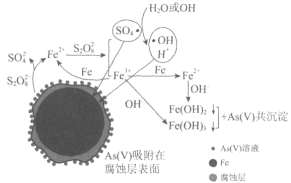
A.1mol��������(Na2S2O8)��2NA��������
B.��56gFe�μӷ�Ӧ������NA��S2O82-����ԭ
C.�����£��м����Fe(OH)3����ˮ���ñ�����Һ��c(Fe3+)Ϊ2.7��10��18mol��L��1
D.pHԽС��Խ������ȥ����ˮ�е��������
���𰸡�C
��������
A.�������ƵĽṹ��ͼ��ʾ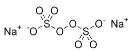 ����������ؿ�������ֻ��1����������A�����
����������ؿ�������ֻ��1����������A�����
B.һ��![]() ��һ��
��һ��![]() ��Ӧ��������
��Ӧ��������![]() ��һ��
��һ��![]() ���ù���ת��2�����ӣ�����
���ù���ת��2�����ӣ�����![]() ��Ҫ��
��Ҫ��![]() ��Ӧ���
��Ӧ���![]() �����ɻ������1mol���μӷ�ӦҪ����1.5mol
�����ɻ������1mol���μӷ�ӦҪ����1.5mol![]() ��B�����
��B�����
C.����![]() ��ע�����Һ���Լ���pH�ӽ�7����
��ע�����Һ���Լ���pH�ӽ�7����![]() �����뷽�̼��ɽ��
�����뷽�̼��ɽ��![]() Ϊ
Ϊ![]() ��C����ȷ��
��C����ȷ��
D.��Ϊ����ǽ�����ת��Ϊ���������ģ�����Һ�ļ���ԽǿԽ������������D�����
����ѡC��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ԷϾ�п�̵�س���������ѡ���ĺ��̷���(MnO2��MnOOH��MnO������Fe��Pb�ȣ�Ϊԭ���Ʊ��ߴ�MnCl2��xH2O��ʵ���̵��������á��乤���������£�
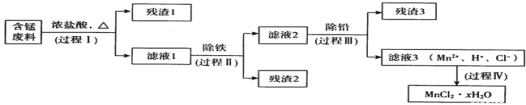
����a:Mn�Ľ������ǿ��Fe��Mn2+�����������±Ƚ��ȶ���pH����5.5ʱ�ױ�O2������
����b�������������������pH
Mn��OH��2 | Pb��OH��2 | Fe��OH��3 | |
��ʼ����ʱ | 8.1 | 6.5 | 1.9 |
��ȫ����ʱ | 10.1 | 8.5 | 3.2 |
ע���������ӵ���ʼŨ��Ϊ0.1 mol��L-l
(1)����I��Ŀ���ǽ����̡���������Һ1�к��е�������ΪMn2+��Fe3+��Pb2+��H+��
��MnO2��Ũ���ᷴӦ�����ӷ���ʽ��____________��
�ڼ�����Һ1��ֻ��Fe3+����Fe2+�IJ����������ǣ��ֱ�ȡ����������Һ1���Թ��У�һ��__________����һ�� ________________��
��Fe3+��Fe2+ת�����ɣ����ܷ����ķ�Ӧ�У�
a. 2Fe2++Cl2= 2Fe3++2Cl- b.4Fe2++O2+4H+=4Fe3++2H2O
c������ д��c�����ӷ���ʽ��____________________��
(2)���̢��Ŀ���dz��������������ַ�����
i����ˮ��������Һ1��ϡ�ͣ��ټ�����10%�İ�ˮ�����ˡ�
ii�����շ�������ҺlŨ���õ��Ĺ�����290�決�գ���ȴ��ȡ�������ˮ�ܽ⡢���ˣ���Һ�ټ������ữ������pH��
��֪�������з�������Ҫ��ӦΪ2FeCl3+3O2![]() 2Fe2O3+3Cl2������ʱMnCl2��PbCl2�������仯��
2Fe2O3+3Cl2������ʱMnCl2��PbCl2�������仯��
�ٰ�ˮ������ʱ����ҺpHӦ������__________֮�䡣
�����ַ����Ƚϣ���ˮ��������ȱ����____________��
(3)���̢��Ŀ���dz�Ǧ��������Լ���____________��
(4)���̢����ù����е�x�IJⶨ���£�ȡm1g��Ʒ�����ڵ�����Χ�м�����ʧȥȫ���ᾧˮʱ��������������m2g����x=________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ԭ�ӻ�ԭ���ţ��밴Ҫ��ѡ��������д������Ҫ����л���Ľṹ��ʽ����CH3����OH����CHO����COOH����Br����H����CH2CH3��![]()
��l�����ӽṹΪ����������ǣ�___��
��2����ʹFeCl3��Һ����ɫ���ǣ�___��
��3����NaOH�Ҵ���Һ���ܷ�����ȥ��Ӧ���ǣ�____��
��4��1mol���л�����������������Һ��Ӧ����4molAg���ɵ��ǣ�___��
��5����Է���������60���ܺ�NaHCO3��Ӧ�ų�CO2���ǣ�___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʵ��ⶨij������Ʒ��ֻ����Na2O2��Na2CO3���ֳ�ȡ����Ʒ13.1g������ˮ��ַ�Ӧ�����1.12L����״���£����壬������Һ���Ϊ500mL���Լ��㣺
��1������Ʒ����Na2O2����������Ϊ_________��
��2����Ӧ����Һ��Na+�����ʵ���Ũ��Ϊ_________mol/L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��Z��M��N�Ƕ�����Ԫ�أ���ԭ���������ε�������֪X�������������Ǵ�����������3����X��Mͬ���壬Y��ͬ��������Ԫ����ԭ�Ӱ뾶���Z��N�����γ�ZN2�ͻ�����ش��������⣺
(1)Ԫ��N�����ڱ��е�λ��_______���������������Ļ�ѧʽΪ________��
(2)�õ���ʽ��ʾZN2���γɹ���________��
(3)Z���ڵ�����ȼ�գ�Z�ڵ�����ȼ�յIJ�����ˮ��Ӧ�ɲ���һ��ʹʪ���ɫʯ����ֽ���������塣д��Z�ڵ����е�ȼ�ղ�����ˮ��Ӧ�Ļ�ѧ����ʽ��______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͬѧ���Ѿ�ѧϰ��ͬλ�ء�ͬϵ�ͬ�������塢ͬ���칹�壬����������Щ�����������г��˼������ʣ��뽫���ʵĺ��������д���±��С�
��![]() ��
��![]()
��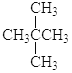 ��
��![]()
��CH4��CH3CH2CH3���ܽ��ʯ��ʯī����뭡����밣���16O��17O��18O�����Ҵ�(CH3CH2OH)�ͼ���(CH3OCH3)��������(O2)�����(O3)��
��� | ͬλ�� | ͬϵ�� | ͬ�������� | ͬ���칹�� |
��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ���Ǵ�������ʡ����������������������֮��Ĺ�ϵ����������ԲȦ���������������ѡ���У�����ȷָ���١��ڡ��ۡ��ܡ����������������ǣ� ��
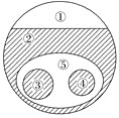
A.�ٵ��ʡ��ۻ�����
B.�ڼ��������
C.�ܼ�ݺ���������
D.�ܺ����������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A.��ҵ�ϳ��õ��NaCl��Һ�Ʊ�������
B.��ҽ����̼����������θ������һ��ҩ��
C.����������������ȼ�տ������Ȼ�����
D.����þȼ��ʱ����ҫ�۵İ⣬��˳����������źŵ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I���ݱ������ҹ����Ϻ��������������еĿ�ȼ��(�����ˮ����)�Բɻ�óɹ���������һ����Ҫ�Ļ���ԭ�ϡ�
��1����������������������ʵ���Ҫ��ʽ����������������������֣�
ˮ����������CH4(g)��H2O(g) ![]() CO(g)��3H2(g)����H1����205.9 kJ��mol��1�� ��
CO(g)��3H2(g)����H1����205.9 kJ��mol��1�� ��
CO(g)��H2O(g) ![]() CO2(g)��H2(g)����H2����41.2 kJ��mol��1����
CO2(g)��H2(g)����H2����41.2 kJ��mol��1����
������̼������CH4(g)��CO2(g) ![]() 2CO(g)��2H2(g)����H3����
2CO(g)��2H2(g)����H3����
��Ӧ���Է����е�������______________����H3��________kJ��mol��1��
��.���Ĺ̶�һֱ�ǿ�ѧ���о�����Ҫ���⣬�ϳɰ������˹��̵��Ƚϳ���ļ�������ԭ��ΪN2 (g)��3H2 (g) ![]() 2NH3(g)��
2NH3(g)��
��2���ڲ�ͬ�¶ȡ�ѹǿ����ͬ���������£���ʼN2��H2 �ֱ�Ϊ0.1 mol��0.3 molʱ��ƽ��������а����������(��)����ͼ��ʾ��

�����У�p1��p2 ��p3 �ɴ�С��˳����____________���÷�Ӧ��H _______0(����>����<����������)��
�����ֱ���vA(N2)��vB(N2)��ʾ�ӷ�Ӧ��ʼ����ƽ��״̬A��Bʱ�Ļ�ѧ��Ӧ���ʣ���vA(N2)________vB(N2)(����>����<����������)��
������250 �桢p1 Ϊ105 Pa�����£���Ӧ�ﵽƽ��ʱ���������Ϊ1 L�����������B��N2 �ķ�ѹp(N2)Ϊ_______Pa (��ѹ����ѹ�����ʵ�������������һλС��)��
��.�����������(S2O42-)Ϊý�飬ʹ�ü�ӵ绯ѧ��Ҳ�ɴ���ȼú�����е�NO��װ����ͼ��ʾ��

��3�����������ĵ缫��ӦʽΪ___________��
��NO����ת�������Ҫ����ΪNH4+����ͨ��ʱ��·��ת����0.3 mol e�������ͨ����������������յ�NO�ڱ�״���µ����Ϊ________mL��
��.��4�������£���a mol��L-1�Ĵ�����b mol��L-1Ba(OH)2 ��Һ�������ϣ���ַ�Ӧ����Һ�д���2c(Ba2+)=c(CH3COO-)����û����Һ�д���ĵ��볣��Ka=___________(�ú�a��b�Ĵ���ʽ��ʾ)��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com