
| A. | 1molC质量是12 g•mol-1 | |
| B. | 22.4L H2的物质的量是1mol | |
| C. | 将60gNaOH溶于1L水中,所得溶液中NaOH的物质的量浓度是1.5mol•L-1 | |
| D. | NaCl的摩尔质量是58.5 g•mol-1 |
分析 A.质量的单位为g,g/mol为摩尔质量的单位;
B.没有告诉在标准状况下,不能使用标准状况下的气体摩尔体积;
C.将60gNaOH溶于1L水中,所得溶液的体积不是1L;
D.氯化钠的相对分子量为58.5,结合相对分子质量与摩尔质量的关系判断.
解答 解:A.1molC的质量为:12g/mol×1mol=12g,故A错误;
B.不是标准状况下,题中数据无法计算氢气的物质的量,故B错误;
C.将60gNaOH溶于1L水中,所得溶液体积不是1L,所得溶液的浓度不是1.5mol/L,故C错误;
D.NaCl的相对分子质量为58.5,则其摩尔质量是58.5 g•mol-1,故D正确;
故选D.
点评 本题考查了物质的量的计算,题目难度不大,明确标准状况下气体摩尔体积的使用条件为解答关键,注意掌握物质的量与摩尔质量、气体摩尔体积之间的关系为解答关键,C为易错点,注意水的体积不等于溶液体积.


 一课一练课时达标系列答案
一课一练课时达标系列答案科目:高中化学 来源: 题型:选择题
| A. | 地壳中金属元素的含量 | B. | 金属的延展性 | ||
| C. | 金属的导电性 | D. | 金属活动性及冶炼的难易程度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu+2FeCl3═CuCl2+2FeCl2 | |
| B. | 2NaHCO3 $\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑ | |
| C. | Cl2+2KI═2KCl+I2 | |
| D. | 2CuSO4+2H2O $\frac{\underline{\;通电\;}}{\;}$2Cu+2H2SO4+O2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将铜插入硝酸银溶液中:Cu+Ag+═Cu2++Ag | |
| B. | Ca( HCO3)2 溶液与过量 NaOH 溶液反应:HCO3-+OH-+Ca2+═CaCO3↓+H2O | |
| C. | 用食醋除水垢:CaCO3+2CH3COOH═Ca2++2CH3COO-+CO2↑+H2O | |
| D. | 稀硫酸和Ba(OH)2溶液反应:H++SO42-+Ba 2++OH-═BaSO 4↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 物质 | X | Y | Z |
| 初始浓度/mol•L-1 | 0.1 | 0.2 | 0 |
| 平衡浓度/mol•L-1 | 0.05 | 0.05 | 0.1 |
| A. | 反应达到平衡时,X的转化率为50% | |
| B. | 反应可表示为X+3Y?2Z,平衡常数为1600 | |
| C. | 其他条件不变时,增大压强可使平衡常数增大 | |
| D. | 改变温度可以改变该反应的平衡常数 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
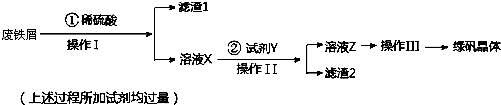
| 氢氧化钠质量(g) | 氯化钠质量(g) | |
| ① | 2.40 | 3.51 |
| ② | 2.32 | 2.34 |
| ③ | 3.48 | 3.51 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浊液a中存在沉淀溶解平衡:AgCl(s)?Ag+(aq)+Cl-(aq) | |
| B. | 滤液b中不含有Ag+ | |
| C. | ③中颜色变化说明AgCl转化为AgI | |
| D. | 实验可以证明AgI比AgCl更难溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| t/s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
| A. | 反应在前50 s的平均速率为v(PCl3)=0.0016mol•L-1•s-1 | |
| B. | 保持其他条件不变,升高温度,平衡时,c(PCl3)=0.11mol•L-1,则反应的△H>0 | |
| C. | 相同温度下,起始时向容器中充入1.0 molPCl5、0.20 molPCl3和0.20 molCl2,达到平衡前v(正)>v(逆) | |
| D. | 相同温度下,起始时向容器中充入2.0 molPCl3、2.0 molCl2,达到平衡时,PCl3的转化率小于80% |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com