
分析 n(O2)=$\frac{0.224L}{22.4L/mol}$=1.000×10-2mol,
设样品中Ag2O2的物质的量为x,Ag2O 的物质的量为y
$\left\{\begin{array}{l}{248g/mol×x+232g/mol×y=2.588g}\\{x+\frac{y}{2}=1.000×1{0}^{-2}}\end{array}\right.$
x=9.500×10-3mol
y=1.000×10-3mol
解答 解:n(O2)=$\frac{0.224L}{22.4L/mol}$=1.000×10-2mol,
设样品中Ag2O2的物质的量为x,Ag2O 的物质的量为y
$\left\{\begin{array}{l}{248g/mol×x+232g/mol×y=2.588g}\\{x+\frac{y}{2}=1.000×1{0}^{-2}}\end{array}\right.$
解之得:x=9.500×10-3mol;y=1.000×10-3mol,答:Ag2O和Ag2O2的物质的量分别为:n(Ag2O)=0.001mol、n(Ag2O2)=0.0095mol.
点评 本题考查根据方程式计算,注意根据质量守恒和元素守恒分析计算,侧重对学生分析思维能力的考查,比较简单.


 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 12gNaHSO4晶体中所含阴离子数目为0.2NA | |
| B. | 23g金属钠与足量O2反应时,转移电子数目一定为NA | |
| C. | 1L 0.1mol/L的NaHCO3溶液中,HCO3-、CO32-离子数之和为0.1NA | |
| D. | 标准状况下,11.2L CCl4中含有C-Cl键的数目为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
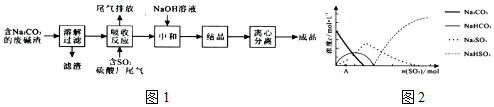
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷中的任意三个原子都不共面 | |
| B. | CH2Cl2是纯净物说明甲烷是四面体结构而不是正方形结构 | |
| C. | 天然气、沼气、坑道气的主要成分均是甲烷 | |
| D. | 丙烷和甲烷一样能与氯气发生取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
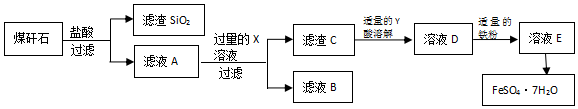
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在卤代烃中直接加入稀硝酸酸化的AgNO3溶液,产生白色沉淀 | |
| B. | 加入NaOH的乙醇溶液,加热后加入AgNO3溶液,产生白色沉淀 | |
| C. | 加蒸馏水,充分搅拌后,加入AgNO3溶液,产生白色沉淀 | |
| D. | 加入NaOH溶液,加热一段时间后冷却,加入稀硝酸酸化,然后加入AgNO3溶液,产生白色沉淀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com