
X元素的阳离子和Y元素的阴离子具有相同的核外电子结构,则下列关系正确的是( )
A.原子序数:X<Y
B.原子半径:r(X)<r(Y)
C.离子半径:r(X)>r(Y)
D.原子最外层电子数:X<Y
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案 口算心算速算应用题系列答案
口算心算速算应用题系列答案科目:高中化学 来源: 题型:
小明等同学为了探究酸、碱、盐溶液的导电性,设计了如下实验:
①在5只250 mL烧杯中分别加入浓度为0.1 mol·L-1的盐酸、CH3COOH溶液、NaOH溶液、NaCl溶液、氨水各150 mL。
②在5种溶液中分别放入相同规格的石墨电极,按下图连接好。
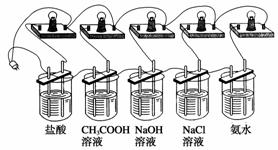
③接通电源,仔细观察现象。
现象1:五个灯泡都亮起来。
结论:_________________________________________________________________。
现象2:盐酸、氯化钠、氢氧化钠溶液对应的灯泡较亮,醋酸、氨水对应的灯泡较暗。
结论:__________________________________________________________________
________________________________________________________________________。
思考:
(1)酸、碱、盐溶液导电与金属导电的原理是否相同,为什么?
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
(2)同学们为了探究不同电解质之间电离能力的差异,设计了上述实验,通过观察灯泡的明亮程度,判断电解质的电离能力大小,为此必须控制其他能影响灯泡亮度的一些因素,使之保持一致,从而不影响灯泡的明亮程度。在本实验中,采取了哪些主要措施来控制其他因素对灯泡亮度的影响?(写出三条即可)_______________________________________
______________。
(3)小明同学根据现象2得出一个结论:氯化氢、氯化钠、氢氧化钠是强电解质,醋酸、一水合氨是弱电解质。你同意他这个观点吗?为什么?___________________________
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
(4)为了进一步探究氯化氢等化合物是强电解质,小红同学在老师的帮助下测定了0.1 mol·L-1的盐酸中的氢离子浓度,通过对结果的分析,即可得出结论。说明氯化氢是强电解质的理由是:测得溶液中的氢离子浓度________ 0.1 mol·L-1(选填“>”、“<”或“=”)。
(5)同学们在实验的基础上,进一步查阅资料得知:一般来说,________________
是强电解质,________________________________________是弱电解质。根据以上结论推测:如果将上述实验中的醋酸和氨水混匀,然后分别盛放在原来的烧杯中。接通电源,可以观察到的现象是________(填字母代号)。
A.与混合前无任何区别
B.5只灯泡都亮起来,亮度完全相同
C.只有盐酸、氯化钠、氢氧化钠溶液对应的灯泡亮起来,另外两只不亮
D.5只灯泡都亮起来,盐酸、氯化钠、氢氧化钠溶液对应的灯泡较亮,另外两只略暗,但明显比混合前明亮
查看答案和解析>>
科目:高中化学 来源: 题型:
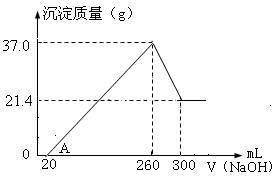
将Fe2O3 、Al2O3 两种固体混合物溶于100mL稀硫酸中,向反应后的溶液中缓慢加入NaOH溶液,加入NaOH溶液的体积与生成沉淀的质量关系如图所示,试回答:
⑴A点坐标(20,0),0到A点的离子反应方程式为
⑵原混合物中Fe2O3的质量是 g
⑶所用NaOH溶液物质的量浓度为多少?
解题过程:
⑷稀硫酸物质的量浓度为多少?
解题过程:
查看答案和解析>>
科目:高中化学 来源: 题型:
下列判断正确的是( )
A.可用水来检验Na2O粉末中是否含有Na2O2
B.可用CO2来检验Na2O粉末中是否含有Na2O2
C.可利用在空气中加热的方法除去Na2O中的Na2O2
D.将足量的Na2O2、Na2O分别加到酚酞试液中,最终溶液均为红色
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有湿润的有色布条的广口瓶,可观察到的现象是____________________________________。
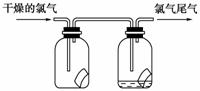
(2)为防止氯气尾气污染空气,实验室通常用________溶液吸收多余的氯气,原理是(用化学方程式表示)____________________________。根据这一原理,工业上常用廉价的石灰乳吸收工业氯气尾气制得漂白粉,漂白粉的有效成分是________(填化学式),长期露置于空气中的漂白粉,加稀盐酸后产生的气体是________(用字母代号填)。
A.O2 B.Cl2
C.CO2 D.HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
有甲、乙、丙、丁四种液体,它们分别为Fe(OH)3胶体、硅酸胶体、As2S3胶体、NaOH溶液。现将有关实验现象记录如下:
①电泳:甲液体的阳极周围颜色变浅,阴极周围颜色变深。②将一束光通过乙液体,无丁达尔现象。③将乙慢慢地加入到丙溶液中,先出现凝聚,后液体变清。试推断甲为________,乙为______________,丙为____________,丁为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应的离子方程式书写正确的是 ( )
A.大理石和盐酸的反应: CO32ˉ+ 2H+ = CO2↑+ H2O
B.向氯化铝溶液中加入过量氨水: Al3+ + 4NH3?H2O = AlO2ˉ+ 2H2O + 4NH4+
C.氯气与氢氧化钠溶液反应:Cl2 + OHˉ = Clˉ + HClO
D.电解饱和食盐水:2Clˉ+ 2H2O  2OHˉ + Cl2↑+ H2↑
2OHˉ + Cl2↑+ H2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com