
 .
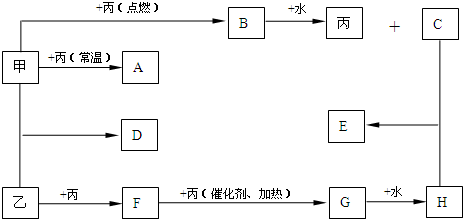
.分析 甲、乙、丙为短周期元素的单质,通常状况下,甲、乙为固态,丙为气态,B 的相对分子质量比 A 大16,甲在丙中点燃生成B,B和水反应生成单质丙和C,能和水反应生成单质的短周期元素化合物只有Na2O2,所以丙是O2,C是氢氧化钠,B是Na2O2,化合物A和氧气反应生成Na2O2,则A是Na2O,钠和氧气反应生成Na2O,则甲是钠,固体单质乙能与氧气发生两步氧化得G,且G能与水反应生成H,则可推知乙为S,F为SO2,G为SO3,H为H2SO4,硫酸与氢氧化钠反应生成E为Na2SO4,甲、乙反应生成D为Na2S,据此答题.
解答 解:甲、乙、丙为短周期元素的单质,通常状况下,甲、乙为固态,丙为气态,B 的相对分子质量比 A 大16,甲在丙中点燃生成B,B和水反应生成单质丙和C,能和水反应生成单质的短周期元素化合物只有Na2O2,所以丙是O2,C是氢氧化钠,B是Na2O2,化合物A和氧气反应生成Na2O2,则A是Na2O,钠和氧气反应生成Na2O,则甲是钠,固体单质乙能与氧气发生两步氧化得G,且G能与水反应生成H,则可推知乙为S,F为SO2,G为SO3,H为H2SO4,硫酸与氢氧化钠反应生成E为Na2SO4,甲、乙反应生成D为Na2S,
(1)D为Na2S,D 的电子式为 ,
,
故答案为: ;
;
(2)上述物质中,能跟水反应,且在反应中既作氧化剂又作还原剂的是Na2O2,
故答案为:Na2O2;
(3)F 和丙反应的化学方程式为2SO2+O2$?_{△}^{催化剂}$2SO3,
故答案为:2SO2+O2$?_{△}^{催化剂}$2SO3.
点评 本题以元素化合物的推断为载体考查了元素化合物的性质,此题的突破口之一为“B+H2O→丙+C”,联想我们学过的反应中,化合物与水反应能生成单质的只有Na2O2,从而推断出其它物质,难度较大.


科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加 AgNO3 溶液,生成白色沉淀,加稀盐酸沉淀不消失,可确定有 Cl- 存在 | |
| B. | 加 BaCl2 溶液,生成白色沉淀,加稀盐酸沉淀不消失,可确定有 SO42- 存在 | |
| C. | 加盐酸,生成的气体能使澄清石灰水变浑浊,可确定有大量CO32-存在 | |
| D. | 通入 Cl2 后,溶液变为黄色,加入淀粉溶液后溶液变蓝,可确定有I- 存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 记载中的反应属于置换反应 | B. | CuSO4溶液呈中性 | ||
| C. | 记载中L含了湿法炼铜的原理 | D. | 每生成1mol铜转移2mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com