
| A、电池正极的电极反应式为:2 MnO2(s)+H2O(1)+2e-═Mn2O3(s)+2OH-(aq) |
| B、外电路中每通过0.2mol电子,锌的质量理论上减小6.5g |
| C、电池工作时,电子由正极通过外电路流向负极 |
| D、电池工作时,锌极发生氧化反应 |
| 0.2mol |
| 2 |


科目:高中化学 来源: 题型:
| A、成都加快建设地铁、轻轨,减少汽车尾气排放,符合“低碳经济”要求 |
| B、绿色化学的核心是应用化学原理对环境污染进行治理 |
| C、用浸泡过高锰酸钾溶液的硅土吸收水果释放的乙烯,有利于水果保鲜 |
| D、明矾水溶液中的氢氧化铝胶体能吸附水中悬浮物,达到净水目的 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙醇和乙酸能发生酯化反应,只要一种反应物过量酯化反应就能进行彻底 |
| B、乙醇、乙酸和乙酸乙酯三者的混合液可用分液的方法将三者分离 |
| C、煤的气化和煤的干馏都发生了化学变化,而石油的分馏属于物理变化 |
| D、苯不能使酸性高锰酸钾溶液褪色,因此苯不能发生氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③⑤⑥ | B、①②④⑤ |
| C、①②③④ | D、只有①③⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用N2浓度的减少表示的平均反应速率为0.2 mol?L-1?s-1 |
| B、2 s时N2的转化率为40% |
| C、2 s时混合气体中n(N2)?n(H2)?n(NH3)=3:9:4 |
| D、2 s 时NH3的浓度为0.4 mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2、I2、HI 平衡混合气体加压后颜色变 |
| B、配制FeSO4溶液时在溶液中加入稀硫酸 |
| C、合成氨工业采用高温条件 |
| D、工业制硫酸中,SO2氧化成SO3,往往需使用催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
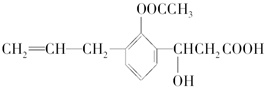
| A、①②③④⑥ | B、②④⑥ |
| C、②④⑤⑥ | D、①③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 弱酸的化学式 | CH3COOH | HCN | H2S |
| 电离常数(25℃) | 1.6×10-5 | 4.9×10-10 | K1=1.3×10-7 K2=7.1×10-15 |
| A、等物质的量浓度的各溶液pH关系为:pH(CH3COONa)>pH(Na2S)>pH(NaCN) |
| B、a mol/LHCN溶液与b mol/LNaOH溶液等体积混合,所得溶液中c(Na+)>c(CN-),则a和b的大小关系不确定 |
| C、某浓度的NaCN溶液的pH=d,则其中由水电离出的c(H+)=10-dmol/L |
| D、NaHS和Na2S的混合溶液中,一定存在c(Na+)+c(H+)=c(OH-)+c(HS-)+c(S2-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向0.01 mol?L-1醋酸溶液中加水,溶液中水电离产生的c(H+) 将减小 | ||
| B、将水加热,KW增大,pH不变,仍呈中性 | ||
| C、向水中加入少量碳酸氢钠固体,溶液的c(H+) 增大,KW不变 | ||
D、c(H+)=
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com