
Ģ¼ŗĶµŖµÄ»ÆŗĻĪļÓėČĖĄąÉś²ś”¢Éś»īĆÜĒŠĻą¹Ų”£
£Ø1£©ŌŚŅ»ŗćĪĀ”¢ŗćČŻĆܱÕČŻĘ÷ÖŠ·¢Éś·“Ó¦£ŗ Ni(s)+4CO(g) 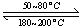 Ni(CO)4(g)£¬
Ni(CO)4(g)£¬ H<0”£ĄūÓĆøĆ·“Ó¦æÉŅŌ½«“ÖÄų×Ŗ»ÆĪŖ“æ¶Č“ļ99£®9£„µÄøß“æÄų”£¶ŌøĆ·“Ó¦µÄĖµ·ØÕżČ·µÄŹĒ ?? (Ģī×ÖÄø±ąŗÅ)”£
H<0”£ĄūÓĆøĆ·“Ó¦æÉŅŌ½«“ÖÄų×Ŗ»ÆĪŖ“æ¶Č“ļ99£®9£„µÄøß“æÄų”£¶ŌøĆ·“Ó¦µÄĖµ·ØÕżČ·µÄŹĒ ?? (Ģī×ÖÄø±ąŗÅ)”£
A£®Ōö¼ÓNiµÄĮææÉĢįøßCOµÄ×Ŗ»ÆĀŹ£¬NiµÄ×Ŗ»ÆĀŹ½µµĶ
B£®ĖõŠ”ČŻĘ÷ČŻ»ż£¬Ę½ŗāÓŅŅĘ£¬ H¼õŠ”
H¼õŠ”
C£®·“Ó¦“ļµ½Ę½ŗāŗ󣬳äČėCOŌŁ“Ī“ļµ½Ę½ŗāŹ±£¬COµÄĢå»ż·ÖŹż½µµĶ
D£®µ±4v[Ni(CO)4]=v(CO)Ź±»ņČŻĘ÷ÖŠ»ģŗĻĘųĢåĆÜ¶Č²»±äŹ±£¬¶¼æÉĖµĆ÷·“Ó¦ŅŃ“ļ»ÆŃ§Ę½ŗāדĢ¬
£Ø2£©COÓėÄų·“Ó¦»įŌģ³ÉÄų“߻ƼĮÖŠ¶¾”£ĪŖ·ĄÖ¹Äų“߻ƼĮÖŠ¶¾£¬¹¤ŅµÉĻ³£ÓĆSO2½«COŃõ»Æ£¬¶žŃõ»ÆĮņ×Ŗ»ÆĪŖµ„ÖŹĮņ”£
ŅŃÖŖ£ŗC(s)+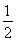 O2(g)=CO(g)??
O2(g)=CO(g)??  H=-Q1 kJ
H=-Q1 kJ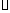 mol-1
mol-1
C(s)+ O2(g)=CO2(g)???  H=-Q2 kJ
H=-Q2 kJ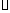 mol-1
mol-1
S(s)+O2(g)=SO2(g)????  H=-Q3 kJ
H=-Q3 kJ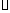 mol-1
mol-1
ŌņSO2(g)+2CO(g)=S(s)+2CO2(g)??  H=????????? ”£
H=????????? ӣ
£Ø3£©½šŹōŃõ»ÆĪļæɱ»Ņ»Ńõ»ÆĢ¼»¹ŌÉś³É½šŹōµ„ÖŹŗĶ¶žŃõ»ÆĢ¼”£Ķ¼28£Ø3£©ŹĒĖÄÖÖ½šŹōŃõ»ÆĪļ£ØCr2O3”¢SnO2”¢PbO2”¢Cu2O)±»Ņ»Ńõ»ÆĢ¼»¹ŌŹ±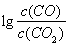 ÓėĪĀ¶Č£Øt£©µÄ¹ŲĻµĒśĻßĶ¼”£
ÓėĪĀ¶Č£Øt£©µÄ¹ŲĻµĒśĻßĶ¼”£
700oCŹ±£¬ĘäÖŠ×īÄѱ»»¹ŌµÄ½šŹōŃõ»ÆĪļŹĒ???????? (Ģī»ÆѧŹ½)£¬ÓĆŅ»Ńõ»ÆĢ¼»¹ŌøĆ½šŹōŃõ»ÆĪļŹ±£¬Čō·“Ó¦·½³ĢŹ½ĻµŹżĪŖ×ī¼ņÕūŹż±Č£¬øĆ·“Ó¦µÄĘ½ŗā³£Źż(K)ŹżÖµµČÓŚ ?????????? ”£
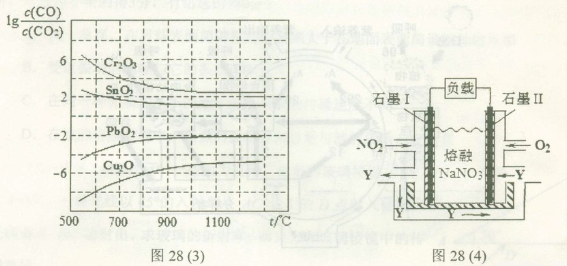
£Ø4£©NO2”¢O2ŗĶČŪČŚNaNO3æÉÖĘ×÷Č¼ĮĻµē³Ų£¬ĘäŌĄķČēÉĻĶ¼28£Ø4£©ĖłŹ¾”£øƵē³ŲŌŚŹ¹ÓĆ¹ż³ĢÖŠŹÆÄ«Iµē¼«ÉĻÉś³ÉŃõ»ÆĪļY£¬Ęäµē¼«·“Ó¦Ź½ĪŖ?????????????? ”£
ČōøĆČ¼ĮĻµē³ŲŹ¹ÓĆŅ»¶ĪŹ±¼äŗ󣬹²ŹÕ¼Æµ½20mol Y£¬ŌņĄķĀŪÉĻŠčŅŖĻūŗıź×¼×“æöĻĀŃõĘųµÄĢå»żĪŖ?? ??? L”£
£Ø1£©C? £Ø3·Ö£©
£Ø2£©£(2Q2£2Q1£Q3) kJ”¤mol£1»ņ£Ø2Q1£2Q2£«Q3£©kJ”¤mol£1?? £Ø3·Ö£©
£Ø3£©Cr2O3??? £Ø3·Ö£©? 10£12? £Ø3·Ö£©
£Ø4£©NO2£«NO3££e££½N2O5? £Ø2·Ö£©?? 224 £Ø3·Ö£©
”¾½āĪö”æ
ŹŌĢā·ÖĪö£ŗ£Ø1£©NiĪŖ¹ĢĢ壬Ōö¼ÓNiµÄĮæ£¬Ę½ŗā²»ŅĘ¶Æ£¬ COµÄ×Ŗ»ÆĀŹŗĶNiµÄ×Ŗ»ÆĀŹ²»±ä£¬“ķĪó£»B”¢?H²»ŹÜŃ¹ĒæµÄÓ°Ļģ£¬ĖłŅŌĖõŠ”ČŻĘ÷ČŻ»ż£¬?H²»±ä£¬“ķĪó£»C”¢·“Ó¦“ļµ½Ę½ŗāŗ󣬳äČėCO£¬ČŻĘ÷µÄŃ¹ĒæŌö“ó£¬ÓŠĄūÓŚĘ½ŗāĻņÕż·“Ó¦·½ĻņŅĘ¶Æ£¬ĖłŅŌŌŁ“Ī“ļµ½Ę½ŗāŹ±£¬COµÄĢå»ż·ÖŹż½µµĶ£¬ÕżČ·£»D”¢ŅņĪŖƻӊÖøĆ÷ŹĒÕż·“Ó¦ĖŁĀŹ»¹ŹĒÄę·“Ó¦ĖŁĀŹ£¬ĖłŅŌµ±4v[Ni(CO)4]=v(CO)²»ÄÜĖµĆ÷·“Ó¦ŹĒ·ńĘ½ŗā£¬“ķĪó”£
£Ø2£©øł¾ŻøĒĖ¹¶ØĀÉ£¬ŅŃÖŖµÄ3øö·“Ó¦ÓėŅŖĒóµÄ·“Ó¦·Ö±š¶Ō±ČCO”¢CO2ŗĶSO2æɵĆ?H=”Ŗ2?H1+2?H2”Ŗ?H3=£(2Q2£2Q1£Q3) kJ”¤mol£1»ņ£Ø2Q1£2Q2£«Q3£©kJ”¤mol£1??
£Ø3£©700”ꏱ£¬Cr2O3·“Ó¦µÄ ×ī“ó£¬ĖµĆ÷COµÄ×Ŗ»ÆĀŹ×īŠ”£¬Ņņ“Ė×īÄѱ»»¹ŌµÄ½šŹōŃõ»ÆĪļŹĒCr2O3£»øł¾ŻĒśĻßæÉÖŖ700”ꏱ£¬Cr2O3·“Ó¦µÄ
×ī“ó£¬ĖµĆ÷COµÄ×Ŗ»ÆĀŹ×īŠ”£¬Ņņ“Ė×īÄѱ»»¹ŌµÄ½šŹōŃõ»ÆĪļŹĒCr2O3£»øł¾ŻĒśĻßæÉÖŖ700”ꏱ£¬Cr2O3·“Ó¦µÄ =4£¬Ōņc(CO)/c(CO2)=104£¬øł¾ŻCO»¹ŌCr2O3µÄ»Æѧ·½³ĢŹ½£ŗ3CO+Cr2O3
=4£¬Ōņc(CO)/c(CO2)=104£¬øł¾ŻCO»¹ŌCr2O3µÄ»Æѧ·½³ĢŹ½£ŗ3CO+Cr2O3 3CO2+2CræÉÖŖĘ½ŗā³£ŹżK=c3(CO2)/c3(CO)= 10£12?
3CO2+2CræÉÖŖĘ½ŗā³£ŹżK=c3(CO2)/c3(CO)= 10£12?
£Ø4£©NO2ŌŚøŗ¼«ÉĻŹ§Č„µē×ÓÉś³ÉµÄŃõ»ÆĪļĪŖN2O5£¬ĖłŅŌµē¼«·“Ó¦Ź½ĪŖNO2£«NO3££e££½N2O5 £»øĆČ¼ĮĻµē³ŲµÄ×Ü·“Ó¦ĪŖ£ŗ4NO2+O2 = 2N2O5£¬ŹÕ¼ÆN2O5¹²20mol£¬ŌņĻūŗÄO2ĪŖ10mol£¬ŌŚ±ź×¼×“æöĻĀµÄĢå»żĪŖ224L”£
æ¼µć£ŗ±¾Ģāæ¼²é»ÆŃ§Ę½ŗāŅĘ¶Æ”¢øĒĖ¹¶ØĀÉ”¢Ę½ŗā³£ŹżµÄ¼ĘĖć”¢Č¼ĮĻµē³Ų”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ

c(N
| ||
| c(NH3?H2O) |
| c(NH3?H2O) |
| c(OH-) |
| c(OH-) |
| c(H+) |

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŌĶĮĄķ½ā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2012-2013ѧğø£½ØŹ¦“óø½ÖŠøßČż£ØÉĻ£©ĘŚÖŠ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com