
五种短周期元素的某些性质如下表所示:
元素代号 | X | W | Y | Z | Q |
原子半径(×10-12 m) | 37 | 99 | 66 | 104 | 154 |
主要化合价 | +1 | -1、+7 | -2 | -2、+6 | +1 |
下列说法正确的是( )
A.由Q与Y形成的化合物中只存在离子键
B.Z与X之间形成的化合物具有还原性
C.X、Y元素组成的化合物的沸点高于X、Z元素组成化合物的沸点是由于Y非金属性比Z强
D.Y、Q、W三种元素组成化合物的水溶液一定显碱性
B
【解析】
试题分析:根据表格中元素的性质可知:X是H;W是Cl;Y是O;Z是S;Q是Na。A.由Q与Y形成的化合物可能是Na2O,也可能是Na2O2,Na2O中只存在离子键,而Na2O2中存在离子键、非极性共价键,错误;B.Z与X之间形成的化合物H2S由于S元素处于该元素的最低化合价,所以具有还原性,正确;C.X、Y元素组成的化合物的沸点高于X、Z元素组成化合物的沸点是由于Y形成的化合物的分子之间除了存在分子间作用力外还存在氢键,增加了分子之间的相互吸引力,错误;D.Y、Q、W三种元素组成化合物可能是NaClO,也可能是NaClO4. NaClO是强碱弱酸盐,水解使溶液显碱性,而NaClO4则是强酸强碱盐,水溶液显中性,错误。
考点:考查元素及化合物的推断、性质的应用和判断的知识。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2015届宁夏银川市高三上学期期中考试化学试卷(解析版) 题型:选择题
化学在生产和日常生活中有着重要的应用,下列说法不正确的是
A.MgO、Al2O3可用于制作耐高温材料
B.Si可用作太阳能电池材料
C.工业上采用电解水法制氢气,解决能源短缺
D.氢氧化铝用于治疗胃酸过多
查看答案和解析>>
科目:高中化学 来源:2015届天津一中高三化学9月考化学试卷(解析版) 题型:选择题
以下说法正确的是()
A.某吸热反应能自发进行,因此该反应是熵增反应
B.常温下Na与足量O2反应生成Na2O随温度升高生成Na2O的速率逐渐加快
C.放热反应速率总是大于吸热反应速率
D.1gH2完全燃烧生成水蒸气时放出热量为121kJ,完全断裂1mol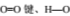 键吸收热量为496kJ、463kJ,则断裂1mol H-H键时吸收热量为902kJ
键吸收热量为496kJ、463kJ,则断裂1mol H-H键时吸收热量为902kJ
查看答案和解析>>
科目:高中化学 来源:2015届四川省2015届高三9月理综化学试卷(解析版) 题型:选择题
有4种混合溶液,分别由等体积0.1mol/L的2种溶液混合而成: ①CH3COON与HCl②CH3COONa与NaOH ③H3COONa与NaCl ④H3COONa与NaHCO3。下列各项排序正确的是
A.pH: ②>③>④>① B. c(CH3COO-):②>④>③>①
C.溶液中c(H+): ①>③>②>④ D.c(CH3COOH): ①>④>③>②
查看答案和解析>>
科目:高中化学 来源:2015届四川省高三第三次理综考试化学试卷(解析版) 题型:填空题
(12分)人体血液里Ca2+离子的浓度一般采用mg/mL来表示。加适量的草酸铵[(NH4)2C2O4]溶液,可析出草酸钙(CaC2O4)沉淀,将此草酸钙沉淀洗涤后溶于强酸可得草酸(H2C2O4),再用KMnO4溶液滴定,使草酸转化成CO2逸出。试回答:
(1)现需要80 mL 0.02 mol·L-1标准KMnO4溶液来进行滴定,则配制溶液时需要的玻璃仪器有烧杯、玻璃棒和______________________;配制时, KMnO4溶液应用强酸酸化,本实验选择________作酸化剂。若选择HNO3酸化,则结果可能________(填“偏大”“偏小”或“不变”)。
(2)草酸与酸性KMnO4溶液反应的离子方程式为_______________________________。
(3)滴定时,根据现象_______________________________________,即可确定反应达到终点。
(4)滴定的实验数据如下所示:
实验编号 | 待测血液的体积/mL | 滴入KMnO4溶液的体积/mL |
1 | 20.00 | 11.95 |
2 | 20.00 | 13.00 |
3 | 20.00 | 12.05 |
经过计算,血液样品中Ca2+离子的浓度为________mg/mL。
查看答案和解析>>
科目:高中化学 来源:2015届四川省资阳市高三一诊理综化学试卷(解析版) 题型:实验题
(14分)硫酸亚锡(SnSO4)是一种重要的能溶于水的硫酸盐,广泛应用于镀锡工业。某研究小组设计SnSO4制备路线如下:

查阅资料:
I、酸性条件下,锡在水溶液中有Sn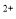 、Sn
、Sn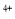 两种主要存在形式,Sn
两种主要存在形式,Sn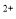 易被氧化。
易被氧化。
Ⅱ、SnCl2易水解生成碱式氯化亚锡[Sn(OH)C1]。
回答下列问题:
(1)操作1的步骤为 、 、过滤、洗涤、干燥。对沉淀进行洗涤的方法是 。
(2)SnCl2粉末需加浓盐酸进行溶解,请结合必要的化学方程式及化学反应原理解释原因: 。
(3)加入Sn粉的作用有两个:①调节溶液pH;② 。
(4)SnSO4还可在酸性条件下用作双氧水的去除剂,发生反应的离子方程式是: 。
(5)该小组通过下列方法测定所用锡粉的纯度(杂质不参与反应):取质量为m的锡粉溶于稀硫酸中,向生成的SnSO4中加入过量的Fe2(SO4)3溶液,用物质的量浓度为c的K2Cr2O7标准溶液滴定生成的Fe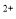 (已知酸性环境下Cr2O
(已知酸性环境下Cr2O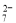 可被还原为Cr
可被还原为Cr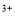 ),共用去K2Cr2O7溶液的体积为V。则锡粉中锡的质量分数是 。(Sn的摩尔质量为M,用含m、c、V、M的代数式表示)
),共用去K2Cr2O7溶液的体积为V。则锡粉中锡的质量分数是 。(Sn的摩尔质量为M,用含m、c、V、M的代数式表示)
查看答案和解析>>
科目:高中化学 来源:2015届四川省资阳市高三一诊理综化学试卷(解析版) 题型:选择题
下列关于阿佛加德罗常数的说法正确的是
A.1 L 0.1 mol/L FeCl3溶液完全水解得到的Fe(OH)3胶体微粒数小于0.1 NA
B.一定条件下的密闭容器中,6.4 g SO2可被氧气氧化得到SO3的分子数为0.1 NA
C.常温下18 g铝放入足量浓硫酸中转移电子数2 NA
D.0.1 NA的NO在一密闭容器中与足量氧气完全反应,得到0.1 mol NO2
查看答案和解析>>
科目:高中化学 来源:2015届四川省绵竹市高三上学期第二次月考化学试卷(解析版) 题型:填空题
(10分)硅在地壳中的含量较高,硅及其化合物的开发由来已久,在现代生活中有广泛应用.回答下列问题:
(1)陶瓷、水泥和玻璃是常用的传统的无机非金属材料,其中生产普通玻璃的主要原料有 .
(2)高纯硅是现代信息、半导体和光伏发电等产业都需要的基础材料.工业上提纯硅有多种路线,其中一种工艺流程示意图及主要反应如图:
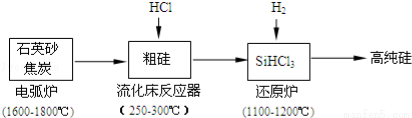
①工业上用石英砂和焦炭在电弧炉中高温加热到1600℃﹣1800℃除生成粗硅外,也可以生产碳化硅,则在电弧炉内可能发生的反应的化学方程式为 .
②在流化床反应的产物中,SiHCl3大约占85%,还有SiCl4、SiH2Cl2、SiH3Cl等,粗硅生成SiHCl3的化学反应方程式 .
(3)有关物质的沸点数据如下表,提纯SiHCl3的主要工艺操作依次是沉降、冷凝和 ;SiHCl3极易水解,其完全水解的产物为 .
物质 | Si | SiCl4 | SiHCl3 | SiH2Cl2 | SiH3Cl | HCl | SiH4 |
沸点/℃ | 2355 | 57.6 | 31.8 | 8.2 | ﹣30.4 | ﹣84.9 | ﹣111.9 |
(4)还原炉中发生的化学反应为: .
(5)氯碱工业可为上述工艺生产提供部分原料,这些原料是 .
查看答案和解析>>
科目:高中化学 来源:2015届四川省成都高新区高三11月统一检测化学试卷(解析版) 题型:选择题
已知A、B为单质,C为化合物, ,能实现上述转化关系的是
,能实现上述转化关系的是
①若C溶于水后得到强碱溶液,则A可能是Na
②若C的溶液遇Na2CO3放出CO2气体,则A可能是H2
③若C的溶液中滴加KSCN溶液显红色,则B可能为Fe
④若C的溶液中滴加NaOH溶液有蓝色沉淀生成,则B可能为Cu
A.①② B.②④ C.①③ D.③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com