
����Ŀ����������(ClO2)��һ����ˮ�����ȷ����й㷺Ӧ�õĸ�Ч��ȫ��������������Cl2��Ȳ��������������DZ��Σ�����л��ȴ����֪: ClO2Ũ�ȹ��������ֽ⣬�����ᱬը�����������Ʊ�ClO2�ķ���:
��1������һ��������
�����������ƺ�ϡ����Ϊԭ���Ʊ�����Ӧԭ��Ϊ5NaClO2+4HCl=5NaCl+4ClO2��+2H2O��
�ٸ÷�Ӧ���������ͻ�ԭ�������ʵ���֮����_______________________��
���о�����������Ӧ��ʼʱ����Ũ�Ƚϴ��������������Cl2�������ӷ���ʽ���Ͳ���Cl2��ԭ��__________________________________________________��
��2�������������ỹԭ��
��������Һ���ò��ᣨH2C2O4����ԭ�����Ƶķ������Ʊ�ClO2
��д���Ʊ�ClO2�����ӷ���ʽ��__________________________________________��
�����ⷨ��ȣ��ò��ỹԭ���Ʊ�ClO2���ص���____________________����������������漰������̵İ�ȫ�ԡ�
��3����֪: ClO2��I-��ԭΪClO2-��Cl-��ת��������ҺpH �Ĺ�ϵ��ͼ��ʾ����pH<2.0 ʱ��ClO2-Ҳ�ܱ�I- ��ȫ��ԭΪCl-����Ӧ���ɵ�I2��Na2S2O3 ��Ӧ�ķ���ʽ: 2Na2S2O3+ I2= Na2S4O6 + 2NaI����ClO2����������ˮ�к���ClO2��ClO2-���ⶨ����ˮ��ClO2��ClO2-�ĺ���������������:
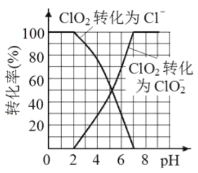
��������ֹ��ȷ����ˮ����ClO2�ĺ���Ϊa mol/L��
���õζ�������ClO2-�ĺ������������Ӧ��ʵ�鲽��:
����1: ȷ��ȡV mL ����ˮ��������ƿ�С�
����2: ����ˮ����pHС��2��
����3: ����������KI ���壬��ַ�Ӧ��
����4: ��������������Һ����c mol/L Na2S2O3 ��Һ�ζ����յ㣬����Na2S2O3 ��ҺV1 mL��
���������������ݣ���ø�����ˮ��ClO2-��Ũ��Ϊ___________mol/L( �ú���ĸ�Ĵ���ʽ��ʾ)��
���𰸡�1��4 4H++ClO2-+3Cl-=2Cl2��+2H2O 2ClO3 - + H2C2O4+ 2H+ =2ClO2�� + 2CO2�� + 2H2O ���ɵ�CO2��ClO2��ϡ������ ![]()
��������
(1)5NaClO2+4HCl�T5NaCl+4ClO2��+2H2O�У�ClԪ�صĻ��ϼ���+3����Ϊ-1�ۣ�+3������Ϊ+4�ۣ���1molNaClO2�õ�������4molNaClO2ʧȥ������ȣ�
�ڷ�Ӧ��ʼʱ����Ũ�Ƚϴ��������������Cl2������������ԭ��Ӧ��
(2) ����������Һ���ò��ᣨH2C2O4����ԭ�����Ƶķ������Ʊ�ClO2ʱ��ͬʱ�������ɶ�����̼��ˮ��
�ڵ�ⷨ������ClO2Ũ�ȹ��ߣ���ClO2Ũ�ȹ��������ֽ⣬�����ᱬը���ݴ˷�����
(3)����4��Na2S2O3�ζ���Һ��I2������2��Ҫ����pHʹClO2��I����ΪI2���ɵ���ת���غ�ɵã�2ClO25I2������ClO2��������I2�����ʵ���������2Na2S2O3+I2=Na2S4O6+2NaI��������Һ��I2�����ʵ������ټ���ClO2�������ɵ�I2�����ʵ������ɵ���ת���غ�ɵã�ClO22I2������ClO2�����ʵ���������������Ũ�ȡ�
(1)��1mol NaClO2�õ�������4mol NaClO2ʧȥ������ȣ���÷�Ӧ���������ͻ�ԭ�������ʵ���֮����1:4���ʴ�Ϊ��1:4��
������Ӧ��ʼʱ����Ũ�Ƚϴ��������������Cl2�������ӷ���ʽ���Ͳ���Cl2��ԭ��Ϊ4H++ClO2-+3Cl-=2Cl2��+2H2O���ʴ�Ϊ��4H++ClO2-+3Cl-=2Cl2��+2H2O��
(2) ����������Һ���ò��ᣨH2C2O4����ԭ�����Ƶķ������Ʊ�ClO2ʱ��ͬʱ�������ɶ�����̼��ˮ�����ӷ���ʽΪ��2ClO3 - + H2C2O4+ 2H+ =2ClO2�� + 2CO2�� + 2H2O���ʴ�Ϊ��2ClO3 - + H2C2O4+ 2H+ =2ClO2�� + 2CO2�� + 2H2O��
�ڵ�ⷨ������ClO2Ũ�ȹ��ߣ���ClO2Ũ�ȹ��������ֽ⣬�����ᱬը�����ò��ỹԭ���Ʊ�ClO2ʱ�����ɵ�CO2��ClO2��ϡ�����ã������������ȫ�ԣ��ʴ�Ϊ�����ɵ�CO2��ClO2��ϡ�����ã�
(3) VmL��Һ�У�ClO2�����ʵ���Ϊ=V��103L��amol/L=aV��103mol���ɵ���ת���غ�ɵã�2ClO25I2��ClO2��������I2�����ʵ���=2.5aV��103mol������Na2S2O3�����ʵ���=V1��103L��cmol/L=cV1��103mol����2Na2S2O3+I2=Na2S4O6+2NaI����Һ��I2�����ʵ���=0.5cV1��103mol��ClO2�������ɵ�I2�����ʵ���=0.5cV1��103mol2.5aV��103mol=(0.5cV12.5aV)��103mol���ɵ���ת���غ�ɵã�ClO22I2����ClO2�����ʵ���=![]() ��(0.5cV12.5aV)��103mol����
��(0.5cV12.5aV)��103mol���� ��
��
�ʴ�Ϊ��![]() ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ƣ�NaNO2)��ۿ���ʳ��������ζ����һ�ֳ��õķ�������ij��ѧ��ȤС�������ͼ��ʾװ�ã�ʡ�Լг�װ�ã��Ʊ�NaNO2��̽�������ʡ�
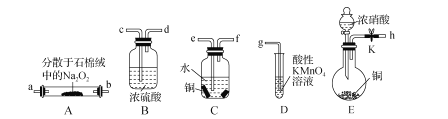
��֪����2NO+Na2O2=2NaNO2��
��NaNO2�ױ�����������NO�ܱ����Ը��������Һ����ΪNO3-��
��HNO2Ϊ���ᣬ�����´��ڷ�Ӧ3HNO2=HNO3+2NO+H2O��
�ش��������⣺
��1��װ��E��ʢ��ͭƬ������������_____�����װ��E�����Եķ�����_____��
��2������ʵ��װ���У��������ӵĺ���˳��Ϊh-_____��
��3��װ��D������KMnO4��Һ��������_____�������ӷ���ʽ��ʾ����
��4����Ӧ������ȡ������Ʒ����ϡ�����У��۲쵽��ʵ������Ϊ_____��
��5���ⶨ��ˮ�����������ƺ�����ȡ1000mLˮ������ƿ�У���������50.00mL0.001mol/L���Ը��������Һ����ַ�Ӧ����0.001mol��L-1��������Һ�ζ�ʣ��ĸ�����أ��յ�ʱ���IJ�������Һ115.00mL����ˮ��NaNO2�ĺ���Ϊ_____mg��L-1������ȡ��Ʒ�ڿ����з���ʱ���������ⶨ���_____������ƫ������ƫ����������Ӱ��������
�йط�Ӧ���£�
5NO2-+2MnO4-+6H+=5NO3-+2Mn2++3H2O��5C2O42-+2MnO4-+16H+=2Mn2++10CO2��+8H2O��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������F��һ��ҩ��ϳɵ��м��壬F��һ�ֺϳ�·�����£�
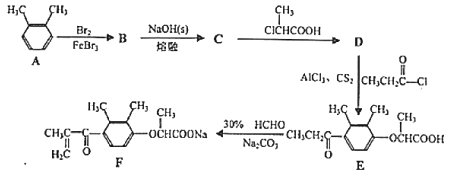
��֪��
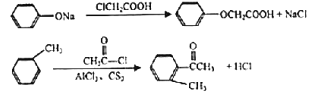
�ش��������⣺
��1��![]() ������Ϊ____��
������Ϊ____��
��2��D�к��������ŵ�����Ϊ____��
��3��B��C�ķ�Ӧ����ʽΪ____��
��4��D��E�ķ�Ӧ����Ϊ____��
��5��C��ͬ���칹���ж��֣����б�����������ONa��2����CH3��ͬ���칹�廹��____�֣�д���˴Ź�������Ϊ3��壬�����֮��Ϊ6:2:1��ͬ���칹��Ľṹ��ʽ____��
��6�����������ƣ� ����һ�ָ�Ч����ҩ��ο����Ϻϳ�·���е������Ϣ�������
����һ�ָ�Ч����ҩ��ο����Ϻϳ�·���е������Ϣ�������![]() Ϊԭ�ϣ�����ԭ����ѡ���ϳ����������Ƶĺϳ�·�ߡ�________________
Ϊԭ�ϣ�����ԭ����ѡ���ϳ����������Ƶĺϳ�·�ߡ�________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ϊ0.1 mol/L�������ΪV0��HX��HY���ֱ��ˮϡ�������V��pH��lg![]() �ı仯��ϵ��ͼ��ʾ������������ȷ����
�ı仯��ϵ��ͼ��ʾ������������ȷ����

A.a��b�������Һ�У�c��X-��=c��Y-��
B.��ͬ�¶��£����볣��K(HX)��d��a
C.��Һ��ˮ�ĵĵ���̶ȣ�d��c��b��a
D.lg![]() =2ʱ����ͬʱ������Һ�壨�����ǻӷ�������
=2ʱ����ͬʱ������Һ�壨�����ǻӷ�������![]() ��С
��С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������(H2N2O2)��һ�ֶ�Ԫ�ᡣ�����£���10 mL 0.01 mol��L��1��H2N2O2��Һ�еμ�0.01 mol��L��1��NaOH��Һ�����H2N2O2��ҺpH��NaOH��Һ����Ĺ�ϵ��ͼ��ʾ������˵������ȷ����
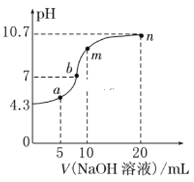
A.��a�㵽n��ˮ�ĵ���̶���������
B.a��ʱ��c(H2N2O2)>c(Na��)
C.m��ʱ��c(OH��)��c(N2O22-)��c(H2N2O2)��c(H��)
D.m�㵽n�㣬![]() ��ֵ����
��ֵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ������һ���ܵó���Ӧ���۵���
ѡ�� | A | B | C | D |
װ�û���� | ȡ��֧�Թܸ�����4 mL 0.01 mol/L�IJ�����Һ���ֱ�μ�2 mL 0.1 mol/L��0.2 mol/L�ĸ��������Һ |
|
| ��ֱ�ʢ��5 mL 0.1 mol/L�������������Һ���Թ��еμ�5 mL 0.1 mo/L��������Һ��һ��ʱ��ֱ������ˮ����ˮ�С� |
���� | ��ɫ���۲���ɫ��ʱ�� | ��������ƣ��ұ�������� | �Թ����ȳ��ֵ���ɫ���壬����ֻ�ɫ���� | �Թ���Һ����������ˮ�����ȳ��ֻ��� |
���� | ������������ʱ����Ӧ��Ũ��Խ��Ӧ����Խ�� | �����ԣ�Cl2>Br2>I2 | �ܽ�ȣ�AgCl>AgBr>AgI | ����˵���¶�Խ�ߣ�����Խ�� |
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������������������֣���ͼ�����е�һ�ַ�����������ȷ���ǣ� ��

A.��ͼ��ʾ����������������������
B.��բ����������������ԭ��Ӧ
C.��������a����բ�ţ������缫��b
D.�����缫�ϵķ�Ӧ��O2+2H2O+4e=4OH��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)���Ⱦ�Բ���ڶ�ά�ռ���������У����γ����ò�ͷ����ò㣬��ͼ1��ʾ�İ뾶��ȵ�Բ��������У�A����________�㣬��λ����________��B����________�㣬��λ����________��
(2)�������ò�һ��һ�������ά�ռ���ѻ����õ���ͼ2��ʾ��һ�ֽ�������ľ�����������Ϊ�������ѻ��������־����У�����ԭ�ӵ���λ����________��ƽ��ÿ��������ռ�е�ԭ����Ŀ��________��

(3)�����ϱ�����ֻ���ǵľ����е�ԭ�Ӿ�����ͼ2��ʾ�Ķѻ���ʽ����λ��Ԫ�����ڱ��ĵ�________���ڵ�__________�壬Ԫ�ط�����________��������Ӳ�ĵ����Ų�ʽ��________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ��A���ܷ�����ͼ��ʾ��һϵ��ת����

��֪����E���Ӽ�ɷ������Ϸ�Ӧ���ɻ�״������C6H8O4���Խ���������⣺
��1��д��A��E�Ľṹ��ʽ__��__��
��2���ڷ�Ӧ�٩�������ȡ����Ӧ����__��
��3��д�����з�Ӧ�Ļ�ѧ����ʽ��
��Ӧ��__��
��Ӧ��__��
��Ӧ��__��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com