
£Ø12·Ö£©¼īŹ½Ģ¼ĖįĆ¾[Ņ»°ćŅŌxMgCO3?yMg(OH)2?zH2O±ķŹ¾]ĆܶȊ”£¬¼øŗõ²»ČÜÓŚĖ®£¬µ«ŌŚĖ®ÖŠŅżĘšĒįĪ¢µÄ¼īŠŌ·“Ó¦”£²»ČÜÓŚŅŅ“¼£¬³£ĪĀĻĀ²»»į·Ö½ā£¬ŹĒĻš½ŗÖĘĘ·µÄÓÅĮ¼ĢīĮĻ”£¹¤ŅÕĮ÷³ĢČēĻĀĶ¼£ŗ

£Ø1£©»Ų“šĻĀĮŠĪŹĢā£ŗ
¢ŁÉśŹÆ»ŅŹĒŅŌŹÆ»ŅŹÆÓė½¹Ģæ»ģŗĻģŃÉÕÉś³É£¬½¹ĢæµÄ×÷ÓĆŹĒ£ŗ ”£
¢ŚĒāŃõ»ÆĆ¾½¬ŅŗÓėCO2·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ
ӣ
¢Ū¼īŹ½Ģ¼ĖįĆ¾ÓĆŅŅ“¼Ļ“µÓµÄÄæµÄŹĒ£ŗ ”£
£Ø2£©ŅŃÖŖ£ŗ¼īŹ½Ģ¼ĖįĆ¾·Ö½ā·“Ó¦·½³ĢŹ½ĪŖ£ŗ
xMgCO3?yMg(OH)2?zH2O 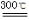 £Øx+y£©MgO+xCO2”ü+£Øy+z£©H2O
£Øx+y£©MgO+xCO2”ü+£Øy+z£©H2O
ijĶ¬Ń§½«46.6g¼īŹ½Ģ¼ĖįĆ¾ŃłĘ·ÖĆÓŚÓ²ÖŹ²£Į§¹ÜÖŠ³ä·Ö×ĘÉÕÖĮŗćÖŲ£¬²ŠĮō¹ĢĢåÖŹĮæĪŖ20.0g£¬½«²śÉśµÄĘųĢåĻČĶعż×ćĮæµÄÅØĮņĖį£¬ŌŁĶعż×ćĮæµÄ¼īŹÆ»Ņ£¬¼īŹÆ»ŅÖŹĮæŌöÖŲ17.6g”£øł¾ŻŹµŃé²ā¶ØµÄŹż¾Ż£¬Č·¶Ø¼īŹ½Ģ¼ĖįĆ¾[xMgCO3”¤yMg(OH)2?zH2O]µÄ»ÆѧŹ½£ØŅŖĒ󊓳ö¼ĘĖć¹ż³Ģ£©”£
£Ø1£©¢Ł×÷Č¼ĮĻ”¢Ģį¹©ÄÜĮæ £Ø2·Ö£©
¢Ś Mg(OH)2+2CO2 = Mg(HCO3)2 £Ø2·Ö£©
¢Ū³żČ„±ķĆęŌÓÖŹ”¢¼õÉŁ¹ĢĢåµÄĖšŗÄ £Ø2·Ö£©
£Ø2£©ÓÉĢāŅāµĆ£ŗ
n(Mg2+)=20.0g/40g”¤mol-1=0.5mol £Ø1·Ö£©
n(CO2)=17.6g/44g”¤mol-1= 0.4mol £Ø1·Ö£©
¾ŻŌŖĖŲŹŲŗćµĆ£ŗ
m(MgCO3)=0.4mol”Į84g”¤mol-1=33.6g£Ø1·Ö£©
m£ŪMg(OH)2£Ż=(0.5mol-0.4mol)=5.8g£Ø1·Ö£©
n(H2O)=44.6g-33.6g-5.8g/18g”¤mol-1=0.4mol£Ø1·Ö£©
x:y:z=4:1:4
Ōņ¼īŹ½Ģ¼ĖįĆ¾µÄ»ÆѧŹ½ĪŖ£ŗ4MgCO3”¤Mg(OH)2”¤4H2O£Ø1·Ö£©£ØĘäĖü¹ż³ĢŗĻĄķŅ²øų·Ö£©
”¾½āĪö”æ
ŹŌĢā·ÖĪö£ŗ£Ø1£©¢ŁCaCO3øßĪĀ·Ö½āÉś³ÉCaOŗĶCO2£¬ĖłŅŌ½¹ĢæµÄ×÷ÓĆŹĒ£ŗ×÷Č¼ĮĻ”¢Ģį¹©ÄÜĮ攣
¢Śøł¾ŻĮ÷³ĢĶ¼£¬CO2ÓėMg(OH)2·“Ó¦ŗóµÄ²śĪļ¾Ń¹ĀĖµĆµ½Mg(HCO3)2£¬ĖłŅŌCO2ÓėMg(OH)2·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗMg(OH)2+2CO2 = Mg(HCO3)2
¢ŪŅņĪŖ¼īŹ½Ģ¼ĖįĆ¾ŌŚĖ®ÖŠŅżĘšĒįĪ¢µÄ¼īŠŌ·“Ó¦£¬²»ČÜÓŚŅŅ“¼£¬ĖłŅŌÓĆŅŅ“¼Ļ“µÓæÉŅŌ³żČ„±ķĆęŌÓÖŹ”¢¼õÉŁ¹ĢĢåµÄĖšŗÄ”£
£Ø2£©²ŠĮō¹ĢĢåĪŖCaO£¬¼īŹÆ»ŅĪüŹÕCO2£¬ÖŹĮæŌö¼ÓĮæĪŖCO2µÄÖŹĮ棬æÉµĆ£ŗ
n(Mg2+)=20.0g/40g”¤mol-1=0.5mol £Ø1·Ö£©
n(CO2)=17.6g/44g”¤mol-1= 0.4mol £Ø1·Ö£©
¾ŻŌŖĖŲŹŲŗćµĆ£ŗ
m(MgCO3)=0.4mol”Į84g”¤mol-1=33.6g£Ø1·Ö£©
m£ŪMg(OH)2£Ż=(0.5mol-0.4mol)=5.8g£Ø1·Ö£©
n(H2O)=44.6g-33.6g-5.8g/18g”¤mol-1=0.4mol£Ø1·Ö£©
x:y:z=4:1:4
Ōņ¼īŹ½Ģ¼ĖįĆ¾µÄ»ÆѧŹ½ĪŖ£ŗ4MgCO3”¤Mg(OH)2”¤4H2O£Ø1·Ö£©
æ¼µć£ŗ±¾Ģāæ¼²é»ÆѧĮ÷³ĢµÄ·ÖĪö”¢»Æѧ·½³ĢŹ½µÄŹéŠ“”¢Ļ“µÓ·½·Ø”¢»Æѧ¼ĘĖć”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014½ĖÕŹ”µŚ¶žŃ§ĘŚĘŚÖŠæ¼ŹŌø߶ž»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
Ė®µÄµēĄėĘ½ŗāĒśĻßČēĶ¼ĖłŹ¾£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
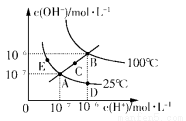
A£®Ķ¼ÖŠĪåµćKW¼äµÄ¹ŲĻµ£ŗB>C>A£½D£½E
B£®Čō“ÓAµćµ½Dµć£¬æɲÉÓĆŌŚĖ®ÖŠ¼ÓČėÉŁĮæĖįµÄ·½·Ø
C£®Čō“ÓAµćµ½Cµć£¬æɲÉÓĆĪĀ¶Č²»±äŹ±ŌŚĖ®ÖŠ¼ÓČėŹŹĮæNaOH¹ĢĢåµÄ·½·Ø
D£®Čō“¦ŌŚBµćŹ±£¬½«pH£½2µÄĮņĖįÓėpH£½12µÄKOHµČĢå»ż»ģŗĻŗó£¬ČÜŅŗĻŌÖŠŠŌ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014½ĖÕŹ”µŚ¶žŃ§ĘŚĘŚÖŠæ¼ŹŌøßŅ»»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠ»ÆѧÓĆÓļµÄŹéŠ“£¬ÕżČ·µÄŹĒ
A£®µŖĘųµÄµē×ÓŹ½£ŗ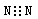 B£®ĮņĄė×ӵĽį¹¹Ź¾ŅāĶ¼£ŗ
B£®ĮņĄė×ӵĽį¹¹Ź¾ŅāĶ¼£ŗ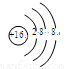
C£®äå»ÆÄʵĵē×ÓŹ½£ŗ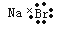 D£®Ė®·Ö×ÓµÄĒņ¹÷Ä£ŠĶ£ŗ
D£®Ė®·Ö×ÓµÄĒņ¹÷Ä£ŠĶ£ŗ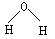
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014½ĖÕŹ”»“°²ŹŠøßČżµŚČż“Īµ÷ŃŠ²āŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠ±ķŹ¾¶ŌÓ¦»Æѧ·“Ó¦µÄĄė×Ó·½³ĢŹ½ÕżČ·µÄŹĒ
A£®ĻņĢś·ŪÖŠ¼ÓČė×ćĮæĻ”ĻõĖį£ŗ2Fe£«6H+£½2Fe3£«£«3H2”ü
B£®ĻņAlCl3ČÜŅŗÖŠµĪ¼ÓÅØ°±Ė®ÖĮ¹żĮæ£ŗAl3+£«4OH££½AlO2££«2H2O
C£®ĻņNaIO3ČÜŅŗÖŠ¼ÓČėŹŹĮæNaHSO3ČÜŅŗ£ŗIO3££«3HSO3££½I££«3SO42££«3H+
D£®ĻņNH4HCO3ČÜŅŗÖŠµĪ¼Ó¹żĮæNaOHČÜŅŗ£ŗNH4+£«HCO3££«2OH££½CO32££«NH3”¤H2O
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014½ĖÕŹ”»“°²ŹŠøßČżµŚČż“Īµ÷ŃŠ²āŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŗĖ·“Ó¦¶ŃĶس£Ź¹ÓĆ235UŗĶ239Pu×÷ĪŖŌĮĻ£¬ŃŠ¾æŗĶæŖ·¢ŗĖÄÜæÉŅŌ¼õÉŁ¶Ō»ÆŹÆČ¼ĮĻµÄŅĄĄµ”£ĻĀĮŠÓŠ¹ŲĖµ·ØÕżČ·µÄŹĒ
A£®239Pu±Č235UŌ×ÓŗĖÄŚ¶ą4øöÖŠ×Ó
B£®ŗĖ·“Ó¦¶ŃÖŠŹ¹ÓƵÄÖŲĖ®ÓėĖ®»„ĪŖĶ¬Ī»ĖŲ
C£®ŹÆÓĶ”¢ĢģČ»ĘųµČ»ÆŹÆČ¼ĮĻŹōÓŚæÉŌŁÉśÄÜŌ“
D£®ŗĻĄķŹ¹ÓĆŗĖÄÜæÉÓŠŠ§¼õÉŁĪĀŹŅĘųĢåµÄÅÅ·Å
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014½ĖÕŹ”»“°²ŹŠøßČż5ŌĀŠÅĻ¢¾ķ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠŅĄ¾ŻĻą¹ŲŹµŃéµĆ³öµÄ½įĀŪÕżČ·µÄŹĒ
A£®ĻņČÜŅŗXÖŠµĪ¼ÓŃĪĖįĪŽĆ÷ĻŌĻÖĻó£¬ŌŁµĪ¼ÓBaCl2ČÜŅŗÓŠ°×É«³Įµķ£¬ŌņXÖŠŗ¬ÓŠSO42£
B£®ĻņNaAlO2ČÜŅŗÖŠµĪČėNaHCO3ČÜŅŗÓŠ°×É«³Įµķ£¬ŌņAlO2£½įŗĻH+ÄÜĮ¦±ČCO32£Ēæ
C£®Ļņ1 mL 1% NaOHČÜŅŗ¼ÓČė2 mL 2%µÄCuSO4ČÜŅŗ£¬Õńµ“ŗóµĪ¼Ó0.5 mL5%ĘĻĢŃĢĒČÜŅŗ£¬¼ÓČČ£¬Ī“³öĻÖŗģÉ«³Įµķ”£Ö¤Ć÷ĘĻĢŃĢĒÖŠ²»ŗ¬Č©»ł
D£®¼ģŃéij²¹ĢśŅ©Ę¬£ØÖ÷ŅŖ³É·ÖĪŖŃĒĢś»ÆŗĻĪļ£©ŹĒ·ńŃõ»Æ±äÖŹ£¬Ź¹ÓĆĀČĖ®ŗĶĮņĒč»Æ¼ŲČÜŅŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014½ĖÕŹ”»“°²ŹŠøßČż5ŌĀŠÅĻ¢¾ķ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
¼×”¢ŅŅ”¢±ū”¢¶”ĖÄÖÖĪļÖŹÖŠ£¬¼×”¢ŅŅ”¢±ū¾łŗ¬ÓŠĻąĶ¬µÄijÖÖŌŖĖŲ£¬ĖüĆĒÖ®¼ä¾ßÓŠČēĻĀĶ¼×Ŗ»Æ¹ŲĻµ”£ĻĀĮŠÓŠ¹ŲĪļÖŹµÄĶʶĻÕżČ·µÄŹĒ

A£®Čō¼×ĪŖ½¹Ģ棬Ōņ¶”æÉÄÜŹĒO2
B£®Čō¼×ĪŖFe£¬Ōņ¶”æÉÄÜŹĒCl2
C£®Čō¼×ĪŖAlCl3£¬Ōņ¶”æÉÄÜŹĒNH3
D£®Čō¼×ĪŖNaHCO3£¬Ōņ¶”æÉÄÜŹĒHCl
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014½ĖÕŹ”ŗ£ĆÅŹŠµŚŅ»Ń§ĘŚĘŚÄ©½Ģѧ֏Įæµ÷ŃŠøßŅ»»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
»ÆѧÓėæĘѧ”¢¼¼Źõ”¢Éē»į”¢»·¾³”¢Éś»īµČĆÜĒŠĻą¹Ų”£ĻĀĮŠÓŠ¹ŲĖµ·ØÖŠ“ķĪóµÄŹĒ
A£®Ņŗ°±æÉÓĆ×÷ÖĘĄä¼Į
B£®Š”ĖÕ“ņÓĆÓŚÖĪĮĘĪøĖį¹ż¶ą
C£®Ć÷·ÆæÉÓĆÓŚ×ŌĄ“Ė®µÄɱ¾śĻū¶¾
D£®¹čĖįÄĘÓĆÓŚÖʱø¹č½ŗŗĶľ²Ä·Ą»š¼ĮµÄŌĮĻ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014½ĖÕŹ”ĪŽĪżŹŠøßŅ»ĻĀŃ§ĘŚĘŚÄ©æ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
¶ĢÖÜĘŚŌŖĖŲX”¢Y”¢ZŌŚŌŖĖŲÖÜĘŚ±ķÖŠµÄĪ»ÖĆĻĀĶ¼ĖłŹ¾£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ

A£®X”¢Y”¢ZČżÖÖŌŖĖŲÖŠ£¬µ„ÖŹŌŚ³£ĪĀĻĀ¾łĪŖĘųĢ¬
B£®ZµÄĒā»ÆĪļµÄĪČ¶ØŠŌ±ČYµÄĒæ
C£®YµÄ×īøßÕż»ÆŗĻ¼ŪĪŖ+5
D£®YµÄµ„ÖŹµÄČŪµć±ČZµÄµĶ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com