
| A. | 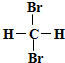 和 和 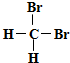 是同一物质 是同一物质 | |
| B. | 1866年凯库勒提出了苯的单、双键交替的正六边形平面结构,解释了苯的部分性质,但它不能解释的事实是邻二溴苯只有一种. | |
| C. | 某有机物化学式为C3H6O2,其核磁共振氢谱有三个峰,其强度比为3:2:1,则该有机物的结构简式一定是CH3CH2COOH | |
| D. | 在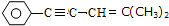 分子中一定共面的碳原子最多为9个,可能共面的碳原子最多为12个 分子中一定共面的碳原子最多为9个,可能共面的碳原子最多为12个 |
分析 A.甲烷为正四面体结构,二溴甲烷没有同分异构体;
B.若为苯的单、双键交替的正六边形平面结构,则邻二溴苯有2种;
C.化学式为C3H6O2,其核磁共振氢谱有三个峰,其强度比为3:2:1,可能为:CH3CH2COOH,CH3COCH2OH,HCOOCH2CH3;
D.依据苯环和乙炔、乙烯结构分析.
解答 解:A.甲烷为正四面体结构,二溴甲烷没有同分异构体,故A正确;
B.若为苯的单、双键交替的正六边形平面结构,则邻二溴苯有2种,则苯的单、双键交替的正六边形平面结构,解释了苯的部分性质,但它不能解释的事实是邻二溴苯只有一种,故B正确;
C.化学式为C3H6O2,其核磁共振氢谱有三个峰,其强度比为3:2:1,可能为:CH3CH2COOH,CH3COCH2OH,HCOOCH2CH3,故C错误;
D.苯环所有原子共面,乙炔线性结构4个原子共线,乙炔中2个碳原子一定在苯环确定的平面上,乙烯平面型结构,图中碳碳碳双键,与碳碳三键通过单键相连,单键可以旋转,所有一定与三键、苯环确定的平面在同一平面的只有一个,所有一定共面的碳原子最多为9个,可能共面的碳原子最多为12个,故D正确;
故选C.
点评 本题考查了有机化合物知识,熟悉有机物结构特点是解题关键,注意分析原子共面、共线时应把握甲烷、苯、乙烯、乙炔等基本有机物解题,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 一个 | B. | 二个 | C. | 三个 | D. | 四个 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 人们研究金星大气成分,发现金星大气中有一种称之为羰基硫(COS)的分子,已知羰基硫分子中所有原子的最外层都满足8电子结构,结合已学知识,判断有关说法正确的是( )
人们研究金星大气成分,发现金星大气中有一种称之为羰基硫(COS)的分子,已知羰基硫分子中所有原子的最外层都满足8电子结构,结合已学知识,判断有关说法正确的是( )| A. | 羰基硫属于非极性分子 | |
| B. | 羰基硫的电子式为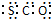 | |
| C. | 羰基硫的沸点比CO2低 | |
| D. | 羰基硫分子中三个原子处于同一直线上 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
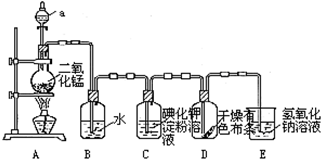
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、Ba2+、Cl-、NO3- | B. | Pb2 +、Hg2 +、S2 -、SO42 - | ||
| C. | NH4+、H+、S2O32-、PO43- | D. | ClO-、Al3 +、Br-、CO32 - |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
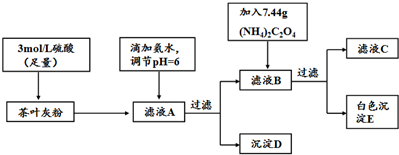
| 离子 | Ca2+ | Fe3+ |
| 完全沉淀时的pH | 13 | 3.7 |
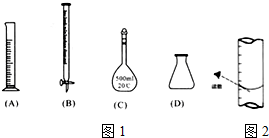
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com