
【题目】化学在人类社会发展中发挥着重要作用,下列事实不涉及化学反应的是
A.利用废弃的秸秆生产生物质燃料乙醇B.利用石油生产塑料、化纤等高分子材料
C.利用基本的化学原料生产化学合成药物D.利用蒸馏法从海水中分离出淡水
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】氧化铅( PbO)是黄色固体。实验室用草酸在浓硫酸作用下分解制备CO,其原理为:H2C2O4![]() CO↑+CO2↑+H2O。某课题组同学设计实验探究CO 还原氧化铅并检验氧化产物(已知CO能使银氨溶液产生黑色沉锭)的装置如图所示。下列说法正确的是
CO↑+CO2↑+H2O。某课题组同学设计实验探究CO 还原氧化铅并检验氧化产物(已知CO能使银氨溶液产生黑色沉锭)的装置如图所示。下列说法正确的是
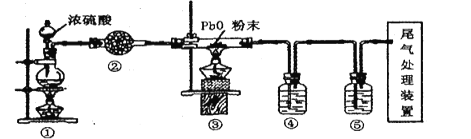
A. 装置②④⑤中的试剂依次为碱石灰、银氨溶液、澄清石灰水
B. 实验时,先点燃装置①处酒精灯,当装置⑤中产生连续气泡且有明显现象后再点燃装置③处酒精灯
C. 实验完毕时,先熄灭装置①处酒精灯,再熄灭装置③处酒精灯
D. 尾气处理可选用点燃、气袋收集、NaOH 溶液吸收等方法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢化钙(CaH2)是一种常用的储氢材料,也是登山运动员常用的能源提供剂,需要密封保存,遇水反应生成氢氧化钙和氢气。某研究性学习小组模拟生产企业制取氢化钙。
(实验)
用锌粒和稀硫酸反应制得干燥、纯净的氢气,再与金属钙在加热的条件下直接化合,即可制得CaH2。
(1)下列有关该实验的说法正确的是_____________________________________。
a.其他条件相同时,粗锌制取氢气的速率比纯锌快
b.加热时,必须通入氮气作为保护气,以防止空气的干扰
c.可以用浓硫酸或碱石灰对H2进行干燥除杂
d.开始实验时,应先通入H2,后给金属钙加热
e.停止实验时,应先停止通入H2,后停止加热
(提出假设)
(2)由于实验中操作不当,金属钙或氢化钙都可能被氧化;该小组甲同学对反应后的固体产物成分提出如下假设:
假设1:含有Ca和CaH2;
假设2:含有CaH2和CaO;
假设3:含有__________________。
(设计实验方案,验证假设)
(3)定性实验用化学方法鉴别Ca与CaH2,请设计实验完成下表中内容。
实验步骤 | 预期现象和结论 |
取少量固体样品,____________________________________________________________________。 | _______________________________________________。 |
(4)定量实验测定Ca和CaH2混合物中CaH2的质量分数。
①取m1 g样品与水完全反应,利用如图装置测定生成的气体体积时,在________时进行收集(填字母)。
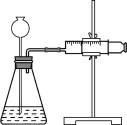
a.刚开始有气泡
b.气泡连续均匀
c.气体经过验纯后,再收集
②如果装置气密性良好,操作正确,乙同学认为:由于液体加入,导致气体的体积测定_____________(填“偏高”“偏低”或“无影响”),则计算出氢化钙的质量分数_____________(填“偏高”“偏低”或“无影响”)。
(反思与交流)
(5)登山运动员常用氢化钙作为能源提供剂,与氢气相比,其优点是氢化钙是固体,携带方便。既然金属钙与水反应也能生成氢气,为什么还要将金属钙制备成氢化钙呢?你的观点是_______________________________________________________________________________________________________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面两种气体的分子数一定相等的是( )
A. 氮气和一氧化碳的质量相等,密度不同
B. 氮气和一氧化碳体积相等
C. 在温度相同、体积相等的条件下氧气和氮气
D. 在压强相同、体积相等的条件下氧气和氮气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关仪器的使用正确的是
A.手持试管给试管内的物质加热
B.用滴管滴加液体时滴管应垂直悬垂在容器上方且不能触及容器内壁
C.用天平称量药品时用手直接拿砝码
D.用燃着的酒精灯去点燃另一盏酒精灯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语表达正确的是:
A. HCl 的电子式:![]() B. F-结构示意图:
B. F-结构示意图: ![]()
C. H2 燃烧的热化学方程式: 2H2 (g) + O2 (g) = 2H2O (g) △H = - 571.6 kJ·mol-1D. Cl2 与水反应的离子方程式: Cl2 + H2O = 2H+ +Cl- + ClO-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过渡元素铁可形成多种配合物,如:[Fe(CN)6]4-、Fe(SCN)3等。
(1)Fe2+基态核外电子排布式为______。
(2)科学研究表明用TiO2作光催化剂可将废水中CN-转化为OCN-、并最终氧化为N2、CO2。OCN-中三种元素的电负性由大到小的顺序为_______。
(3)与CN-互为等电子体的一种分子为______(填化学式);1mol Fe(CN)63-中含有σ键的数目为______。
(4)铁的另一种配合物Fe(CO)5熔点为-20.5℃,沸点为103℃,易溶于CCl4,据此可以判断Fe(CO)5晶体属于_______(填晶体类型)。
(5)铁铝合金的一种晶体属于面心立方结构,其晶胞可看成由8个小体心立方结构堆砌而成。已知小立方体如图所示。该合金的化学式为_______。
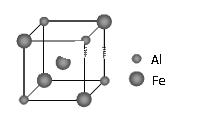
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能正确表示下列反应的离子反应方程式为( )
A. Ba(OH)2溶液中加入少量NaHCO3溶液:HCO3-+Ba2++OH-=BaCO3![]() +H2O
+H2O
B. 向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42-沉淀完全:3Ba2++3SO42-+2Al3++6OH-═2BaSO4↓+2Al(OH)3↓
C. NH4HCO3稀溶液与过量的KOH溶液反应:HCO3-+OH-=CO32-+H2O
D. 醋酸除去水垢:2H++CaCO3=Ca2++CO2↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气净化器中发生的反应为2NO(g)+2CO(g)![]() N2(g)+2CO2(g)。一定温度下,在三个体积均为1.0L恒容密闭容器中发生上述反应,测得有关实验数据如下:
N2(g)+2CO2(g)。一定温度下,在三个体积均为1.0L恒容密闭容器中发生上述反应,测得有关实验数据如下:
容器 | 温度/(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | ||||
NO | CO | N2 | CO2 | N2 | CO2 | ||
I | 400 | 0.2 | 0.2 | 0 | 0 | 0.12 | |
II | 400 | 0.4 | 0.4 | 0 | 0 | ||
III | 300 | 0 | 0 | 0.1 | 0.2 | 0.075 | |
下列说法正确是
A. 容器I中达到平衡所需时间2s,则v(N2)=0.06 molL-1·s-1
B. 该反应的ΔS<0、ΔH<0
C. 达到平衡时,体系中c(CO)关系:c(CO,容器II)>2c(CO,容器I)
D. 若起始时向I中充入NO、CO、N2、CO2各0.1mol,开始时V正>V逆
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com