
| 选项 | 实验操作 | 实验目的或结论 |
| A | 向某盐溶液中加入AgNO3溶液,产生白色沉淀;加入浓NaOH溶液加热,生成使湿润红色石蕊试纸变蓝的气体 | 该盐一定是NH4Cl |
| B | 向浓硝酸中加入足量铜片充分反应,所得气体显红棕色 | 该气体是纯净的NO2 |
| C | 常温下,向浓度均为0.01mol/L的Na2CO3和Na2SO4的混合溶液中滴加1~2滴BaCl2溶液,滤出的沉淀不溶于盐酸 | 说明常温下Ksp(BaCO3)>Ksp(BaSO4) |
| D | 向Na2O2与水反应后所得溶液中加少量MnO2 | 检验Na2O2与水反应的中 间产物为H2O2 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.与硝酸银反应生成的白色沉淀可能为硫酸银;
B.Cu与浓硝酸反应生成二氧化氮,所反应进行,浓硝酸变为稀硝酸,Cu与稀硝酸反应生成NO;
C.滤出的沉淀不溶于盐酸,沉淀为硫酸钡;
D.若中间产物为过氧化氢,加少量MnO2作催化剂,分解生成气体.
解答 解:A.与硝酸银反应生成的白色沉淀可能为硫酸银,则盐可能为硫酸铵,故A错误;
B.Cu与浓硝酸反应生成二氧化氮,所反应进行,浓硝酸变为稀硝酸,Cu与稀硝酸反应生成NO,且二氧化氮与四氧化二氮存在化学平衡,则气体不是纯净的NO2,故B错误;
C.滤出的沉淀不溶于盐酸,沉淀为硫酸钡,碳酸钡溶于盐酸,则说明常温下Ksp(BaCO3)>Ksp(BaSO4),故C正确;
D.若中间产物为过氧化氢,加少量MnO2作催化剂,分解生成气体,则该实验可检验Na2O2与水反应的中间产物为H2O2,故D正确;
故选CD.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、离子检验、Ksp比较、氧化还原反应等为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.


科目:高中化学 来源: 题型:选择题
| 元素代号 | 元素的性质或原子结构 |
| W | M层上的电子数为4 |
| X | 常温下,其单质为双原子分子,其氢化物的水溶液显碱性 |
| Y | L层电子数为次外层电子数的3倍 |
| Z | 元素最高正价是+7价 |
| A. | 原子半径:W>X>Y | |
| B. | 化合物WY2不溶于水 | |
| C. | 由X、Y和氢三种元素形成的所有化合物中只含共价键 | |
| D. | 最高价氧化物对应水化物的酸性:W<Z |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 某学习小组依据氧化还原反应:2Ag++Cu═Cu2++2Ag设计成的原电池如图所示,则负极发生的电极反应为Cu-2e-═Cu2+;当反应进行到一段时间后取出电极材料,测得某一电极增重了5.4g,则该原电池反应共转移了的电子数目是0.05NA.
某学习小组依据氧化还原反应:2Ag++Cu═Cu2++2Ag设计成的原电池如图所示,则负极发生的电极反应为Cu-2e-═Cu2+;当反应进行到一段时间后取出电极材料,测得某一电极增重了5.4g,则该原电池反应共转移了的电子数目是0.05NA.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | A | B | C | D |
| 实验样品 | Na2CO3 | 氯水 | NaCl固体 | 乙醇 |
| 实验数据 | 5.26mL | pH=2.3 | 10.3g | 78.3℃(沸点) |
| 实验仪器 | 酸式滴定管 | 广泛pH试纸 | 托盘天平 | 体温计 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 44 g由CO2和N20组成的混合气体中的氧原子数为2NA | |
| B. | 1 mol由异丁烷和正丁烷组成的混合物中含有的共价键数目为13NA | |
| C. | 2 mol SO2与2 molO2充分反应生成的SO2分子数为NA | |
| D. | 100 mL 12 mol•L-1浓盐酸与足量MnO2反应,转移的电子数为0.6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
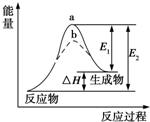
| A. | 该反应的反应热△H=E2-E1 | |
| B. | 催化剂能改变反应的焓变 | |
| C. | 催化剂能降低反应的活化能 | |
| D. | a、b分别对应无催化剂和有催化剂的能量变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 温室效应--减少化石燃料使用,开发清洁能源 | |
| B. | 土壤污染--科学灌溉,合理使用农药和化肥 | |
| C. | 白色污染--杜绝生产塑料袋,从根源上治理 | |
| D. | 水体污染--节约用水,减少污水排放 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com