

| A. | 0.082 | B. | 0.072 | C. | 0.072MPa-1 | D. | 0.082 MPa-1 |
分析 由图可知,A点乙烯的平衡转化率为20%,设起始量n(H2O)=n(C2H4)=1mol,转化的乙烯为0.2mol,则:
C2H4(g)+H2O(g)═C2H5OH(g)
起始量(mol):1 1 0
转化量(mol):0.2 0.2 0.2
平衡量(mol):0.8 0.8 0.2
压强之比等于物质的量之比,计算乙烯、水蒸气、乙醇蒸气分压,再根据Kp=$\frac{p({C}_{2}{H}_{5}OH)}{p({C}_{2}{H}_{4})×p({H}_{2}O)}$计算.
解答 解:由图可知,A点乙烯的平衡转化率为20%,设起始量n(H2O)=n(C2H4)=1mol,转化的乙烯为0.2mol,则:
C2H4(g)+H2O(g)═C2H5OH(g)
起始量(mol):1 1 0
转化量(mol):0.2 0.2 0.2
平衡量(mol):0.8 0.8 0.2
压强之比等于物质的量之比,则p(C2H4)=p(H2O)=7.8MPa×$\frac{0.8mol}{1.8mol}$=7.8MPa×$\frac{4}{9}$,p(C2H5OH)=7.8MPa×$\frac{1}{9}$,则Kp=$\frac{p({C}_{2}{H}_{5}OH)}{p({C}_{2}{H}_{4})×p({H}_{2}O)}$=$\frac{7.8MPa×\frac{1}{9}}{7.8MPa×\frac{4}{9}×7.8MPa×\frac{4}{9}}$=0.072MPa-1,
故选:C.
点评 本题考查化学平衡计算,涉及平衡常数计算,关键是计算各组分反应,注意平衡常数单位问题,难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:多选题
| A. | 将溶解溶质的烧杯内的液体倒入容量瓶后,未洗涤烧杯就进行定容. | |
| B. | 定容时,液面超过容量瓶颈上的刻度线,用胶头滴管将过量的液体吸出 | |
| C. | 定容摇匀后,发现瓶内液面略低于瓶颈刻度线 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

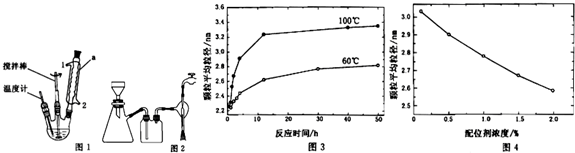
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解饱和食盐水可制得金属钠 | B. | 海水提溴涉及到氧化还原反应 | ||
| C. | 海带提碘只涉及物理变化 | D. | 海水提镁不涉及复分解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 78g由Na2S和Na2O2组成的固体混合物,含有的阴离子数为NA | |
| B. | 标准状况下,22.4L CCl4中含有的分子数为NA | |
| C. | 将1mol FeCl3水解制成胶体,所得胶体中含有的胶体粒子数为NA | |
| D. | 1mol/L NaOH溶液中含有的Na+数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸性溶液中:Fe2+、ClO-、SO42-、Na+ | |
| B. | pH=13的无色溶液中:K+、NO3-、Al3+、CO32- | |
| C. | 澄清透明溶液中:Fe3+、Ba2+、Na+、Cl- | |
| D. | 加入铝粉后产生大量氢气的溶液中:NH4+、Na+、NO3-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com